
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
实验编号 | 室温下,试管中所加试剂及其用量/mL | 溶液褪至无色所需时间/min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是__________________________。
(2)利用实验1中的数据,计算用KMnO4表示的化学反应速率为_____________。(溶液混合前后体积变化可忽略)
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化的趋势如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的实际趋势如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
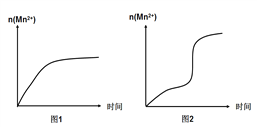
①该小组同学提出的假设是_____________。
②请你帮助该小组同学完成实验方案,并填写表中空白
实验编号 | 室温下,试管中所加试剂及其用量 | 再向试管中加入某种固体 | 溶液褪至无色所需时间/min | |||
0.6mol/L H2C2O4溶液 | H2O | 3mol/L 稀H2SO4溶液 | 0.05mol/L KMnO4溶液 | |||
4 | _____________ | 2.0 | 2.0 | 3.0 | MnSO4 | t |
③若该小组同学提出的假设成立,t_____________1.5(填“大于”、“小于”或“等于”)。
【答案】 其他条件不变时,增大H2C2O4浓度(或增大反应物浓度),加快化学反应速率 1.0×10-2mol/(L·min) 生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用) 3.0 小于
【解析】(1)三个实验中改变的是草酸用量,其他物质不变,所以研究的是草酸浓度对反应速率的影响。
(2)褪色时间为1.5min;高锰酸钾初始浓度为3×0.05/(3+2+2+3)=0.015mol/L;所以速率为:0.015÷1.5=1.0×10-2mol/(L·min)
(3)根据实验图像,得到反应速率先加快后减慢,结合课本上的对应实验,得出硫酸锰对反应起到催化作用。进行实验时应注意其他条件不变,所以溶液总体积应该为10mL,所以草酸加3mL。如果催化反应,时间当然比1.5min小。


科目:高中化学 来源: 题型:
【题目】现有一瓶A和B的混合液,已知A和B的某些性质如下:
物质 | 分子式 | 熔点℃ | 沸点℃ | 密度gcm-3 | 水溶性 |
A | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
B | C4H8O2 | -84 | 77 | 0.90 | 可溶 |
由此,分离A和B的最佳方法是
A.萃取B.升华C.分馏D.分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有HCO3﹣、SO32﹣、Na+、CH3COO﹣等四种离子,向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积不变)( )
A.CH3COO﹣B.SO32﹣C.Na+D.HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定实验中取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
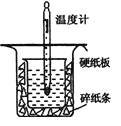
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是__________,除此之外,装置中的一个明显错误是_____________。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量_______(填“相等”或“不相等”)
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(3)近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),通过以上数据计算中和热ΔH=_______( 结果保留小数点后一位)。
(4)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A,B,C,D,E,F,G七种元素为元素周期表中短周期元素,其原子序数依次增大.A的质量数等于其质子数;B原子的最外层电子数是其电子层数的2倍;D的最外层电子数是其电子层数的3倍;E,F,G三种元素同周期且它们的最高价氧化物的水化物两两反应生成均盐和水,E,F,G的最外层电子数之和为10.回答下列问题.
(1)元素D、F的名称、;
(2)C元素在周期表中的位置;
(3)用电子式表示D,E两元素形成的1:1的化合物的形成过程其中含有的化学键的类型
(4)写出分别由A,D,E,G四种元素组成的两种化合物反应的化学方程式;
(5)写出E、F的最高价氧化物的水化物反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A. 生成了一种强酸弱碱盐B. 弱酸溶液和强碱溶液反应
C. 强酸溶液和弱碱溶液反应D. 一元强酸溶液和一元强碱溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(s)+Y(g)![]() W(g)+Z(g)(正反应是放热反应),在一定体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如图所示。下列条件的改变与图中情况相符的是( )
W(g)+Z(g)(正反应是放热反应),在一定体积不变的容器中反应达到平衡后,改变条件,反应速率(v)随时间变化的情况如图所示。下列条件的改变与图中情况相符的是( )
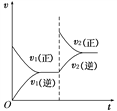
A. 增加了X的物质的量 B. 降低了温度
C. 增大了压强 D. 增大了Y的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的应用与性质相对应的说法正确的有( )
①光导纤维可用作通讯材料是因为其具有导电性
②明矾能用于净水是因为铝离子水解生成的氢氧化铝胶体具有强氧化性
③浓硫酸可用作干燥剂是因为其具有脱水性
④MgO、Al2O3的熔点很高,可制作耐高温材料
⑤氯化铁溶液可用于制作印刷电路板是因为其能氧化单质铜
⑥NaHCO3能与碱反应,因此食品工业上可用作焙制糕点的膨松剂
⑦A1具有良好的延展性和抗腐蚀性,可制成铝箔包装物品
A. 5个 B. 4个 C. 3个 D. 2个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.标准状况下,22.4L水中所含的分子数约为6.02×1023
B.标准状况下,aL的氧气和氮气的混合物含有的分子数约为 ![]() ×6.02×1023
×6.02×1023
C.常温常压下,48g O3气体含有的氧原子数为6.02×1023
D.1mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com