
ЁОЬтФПЁПвбжЊMЪЧЖЬжмЦкН№ЪєдЊЫиЃЌXКЭYЪЧЖЬжмЦкЗЧН№ЪєдЊЫиЃЌЧвXЁЂMЁЂYЕФдзгађЪ§вРДЮдіДѓЁЃШ§епзщГЩЕФЮяжЪ M3XY(ПЩЪгЮЊM2X MY)ЪЧвЛжжСМКУЕФРызгЕМЬхЁЃбаОПепдкГЃбЙЯТРћгУЯТСаЗДгІКЯГЩM3XYЃК2M +2MXA + 2MY==2M3XY + A2ЁЃЦфжаГЃЮТГЃбЙЯТA2ЪЧЮоЩЋЮоЮЖЦјЬхЃЌвбжЊЩЯЪіЗДгІжаЯћКФ0.92 g MЕФЕЅжЪПЩЕУЕНБъзМзДПіЯТ448 mLЕФA2ЁЃЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ( )
A.XЮЛгкЕкЖўжмЦкЕкIVAзх
B.МђЕЅРызгАыОЖ:Y > M > X
C.MXAЪЧЙВМлЛЏКЯЮя
D.M3XYШмгкЫЎКѓШмвКГЪМюад
ЁОД№АИЁПD
ЁОНтЮіЁП
ИљОн2M+2MXA+2MY=2M3XY +A2ЃЌПЩЕУЙиЯЕЪН2M ~ A2ЃЌ ИљОнЬтИјЪ§ОнЃЌПЩжЊn(A2) =![]() =0.02molЃЌИљОнMгыA2ЕФЮяжЪЕФСПЙиЯЕЃЌn(M)=0.04molЃЌ0.92 g MЕФФІЖћжЪСПЕШгкM=
=0.02molЃЌИљОнMгыA2ЕФЮяжЪЕФСПЙиЯЕЃЌn(M)=0.04molЃЌ0.92 g MЕФФІЖћжЪСПЕШгкM=![]() =
=![]() =23g/molЃЌдђMЕФЕЅжЪЕФФІЖћжЪСП=23gmol-1ЃЌгжMЪЧЖЬжмЦкН№ЪєдЊЫиЃЌЙЪMЪЧNaЃЛMКЭYПЩаЮГЩЛЏКЯЮяMYЃЌЧвдзгађЪ§MЃМYЃЌYгжЪЧЖЬжмЦкЗЧН№ЪєдЊЫиЃЌЙЪYЪЧClЃЛдкM3XY(M2X.MY)жаXдЊЫиЕФЛЏКЯМлЪЧ-2МлЃЌЧвдзгађЪ§XЃМMЃЌЫљвдXЪЧOЃЛГЃЮТГЃбЙЯТA2ЪЧЮоЩЋЮоЮЖЦјЬхЃЌИљОнЬтИјЗДгІжаMXAжаAЕФЛЏКЯМлЮЊ+1ЃЌПЩжЊAЮЊHЃЌОЭДЫЗжЮіНтД№ЁЃ
=23g/molЃЌдђMЕФЕЅжЪЕФФІЖћжЪСП=23gmol-1ЃЌгжMЪЧЖЬжмЦкН№ЪєдЊЫиЃЌЙЪMЪЧNaЃЛMКЭYПЩаЮГЩЛЏКЯЮяMYЃЌЧвдзгађЪ§MЃМYЃЌYгжЪЧЖЬжмЦкЗЧН№ЪєдЊЫиЃЌЙЪYЪЧClЃЛдкM3XY(M2X.MY)жаXдЊЫиЕФЛЏКЯМлЪЧ-2МлЃЌЧвдзгађЪ§XЃМMЃЌЫљвдXЪЧOЃЛГЃЮТГЃбЙЯТA2ЪЧЮоЩЋЮоЮЖЦјЬхЃЌИљОнЬтИјЗДгІжаMXAжаAЕФЛЏКЯМлЮЊ+1ЃЌПЩжЊAЮЊHЃЌОЭДЫЗжЮіНтД№ЁЃ
AЃЎXЪЧOЃЌЮЛгкЕкЖўжмЦкЕкЂіAзхЃЌбЁЯюAДэЮѓЃЛ
BЃЎЕчзгВуЪ§ВЛЭЌЪБЃЌЕчзгВуЪ§дНЖрЃЌАыОЖдНДѓЃЌЕБЕчзгВуЪ§ЯрЭЌЪБЃЌКЫЕчКЩЪ§дНДѓЃЌАыОЖдНаЁЃЌРызгАыОЖЕФДѓаЁЫГађЮЊr(C1-)ЃОr(O2-)ЃОr(Na+ )ЃЌбЁЯюBДэЮѓЃЛ
CЃЎMXAЪЧNaOHЃЌЪЧКЌгаЙВМлМќЕФРызгЛЏКЯЮяЃЌбЁЯюCДэЮѓЃЛ
DЃЎM3 XY(Na2O.NaCl)ШмгкЫЎКѓКЭЫЎЗЂЩњЗДгІЩњГЩNaOHКЭNaClЃЌШмвКЯдМюадЃЌбЁЯюDе§ШЗЃЛ
Д№АИбЁDЁЃ


 ЦпаЧЭМЪщПкЫуЫйЫуЬьЬьСЗЯЕСаД№АИ
ЦпаЧЭМЪщПкЫуЫйЫуЬьЬьСЗЯЕСаД№АИ ГѕжабЇвЕПМЪдЕМгыСЗЯЕСаД№АИ
ГѕжабЇвЕПМЪдЕМгыСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвжЦБИ1,2ЖўфхввЭщЕФЗДгІдРэШчЯТЃКCH3CH2OH![]() CH2=CH2ЁќЃЋH2OЃЌCH2=CH2ЃЋBr2ЁњBrCH2CH2BrЁЃгУЩйСПЕФфхКЭзуСПЕФввДМжЦБИ1,2ЖўфхввЭщЕФзАжУШчЯТЭМЫљЪОЃК
CH2=CH2ЁќЃЋH2OЃЌCH2=CH2ЃЋBr2ЁњBrCH2CH2BrЁЃгУЩйСПЕФфхКЭзуСПЕФввДМжЦБИ1,2ЖўфхввЭщЕФзАжУШчЯТЭМЫљЪОЃК
гаЙиЪ§ОнСаБэШчЯТЃК
ввДМ | 1,2ЖўфхввЭщ | ввУб | |
зДЬЌ | ЮоЩЋвКЬх | ЮоЩЋвКЬх | ЮоЩЋвКЬх |
УмЖШ/gЁЄcmЃ3 | 0.79 | 2.2 | 0.71 |
ЗаЕу/Ёц | 78.5 | 132 | 34.6 |
ШлЕу/Ёц | Ѓ130 | 9 | Ѓ116 |
ЛиД№ЯТСаЮЪЬтЃК
(1)дкзАжУcжагІМгШы________(бЁЬюађКХ)ЃЌЦфФПЕФЪЧЮќЪеЗДгІжаПЩФмЩњГЩЕФЫсадЦјЬхЁЃ
ЂйЫЎ ЂкХЈСђЫс ЂлЧтбѕЛЏФЦШмвК ЂмБЅКЭЬМЫсЧтФЦШмвК
(2)ХаЖЯdЙмжажЦБИЖўфхввЭщЗДгІвбНсЪјЕФзюМђЕЅЗНЗЈЪЧ______________________ЁЃ
(3)НЋЖўфхввЭщДжВњЦЗжУгкЗжвКТЉЖЗжаМгЫЎЃЌеёЕДКѓОВжУЃЌВњЮягІдкЫЎЕФ________(ЬюЁАЩЯЁБЛђЁАЯТЁБ)ВуЁЃ
(4)ШєВњЮяжагаЩйСПЮДЗДгІЕФBr2ЃЌзюКУгУ________(Ьюе§ШЗбЁЯюЧАЕФађКХ)ЯДЕгГ§ШЅЁЃ
ЂйЫЎЁЁЂкЧтбѕЛЏФЦШмвКЁЁЂлЕтЛЏФЦШмвКЁЁЂмввДМ
ЃЈ5ЃЉЗДгІЙ§ГЬжаашгУРфЫЎРфШД(зАжУe)ЃЌЦфжївЊФПЕФЪЧ______________________ЃЛ ЕЋВЛгУБљЫЎНјааЙ§ЖШРфШДЃЌдвђ_______________________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊАзСзКЭP4O6ЕФЗжзгНсЙЙШчЭМЫљЪОЃЌгжжЊЛЏбЇМќЕФМќФмЪЧаЮГЩ(ЛђЖЯПЊ)1 molЛЏбЇМќЪБЪЭЗХ(ЛђЮќЪе)ЕФФмСПЃЌЯжВщжЊPЁЊPМќФмЮЊ198 kJЁЄmolЃ1ЁЂPЁЊOМќФмЮЊ360 kJЁЄmolЃ1ЁЂO===OМќФмЮЊ498 kJЁЄmolЃ1ЁЃШєЩњГЩ1 mol P4O6ЃЌдђЗДгІP4(АзСз)ЃЋ3O2=P4O6жаЕФФмСПБфЛЏЮЊ( )
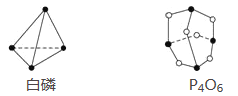
A. ЮќЪе1 638 kJФмСП B. ЗХГі1 638 kJФмСП
C. ЮќЪе126 kJФмСП D. ЗХГі126 kJФмСП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПN2O5ЪЧвЛжжаТаЭЯѕЛЏМСЃЌЦфаджЪКЭжЦБИЪмЕНШЫУЧЕФЙизЂЁЃвЛЖЈЮТЖШЯТЃЌдк2LКуШнУмБеШнЦїжаЗЂЩњЗДгІЃК2N2O5(g)![]() 4NO2(g)ЃЋO2(g) ЁїHЃО0ЁЃЗДгІЮяКЭВПЗжЩњГЩЮяЕФЮяжЪЕФСПЫцЗДгІЪБМфБфЛЏЕФЧњЯпШчЭМЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
4NO2(g)ЃЋO2(g) ЁїHЃО0ЁЃЗДгІЮяКЭВПЗжЩњГЩЮяЕФЮяжЪЕФСПЫцЗДгІЪБМфБфЛЏЕФЧњЯпШчЭМЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
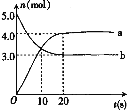
A.0ЁЋ20sФкЃЌЦНОљЗДгІЫйТЪv(N2O5)ЃН0.05 molЁЄLЃ1ЁЄsЃ1
B.Щ§ИпЮТЖШЃЌПЩЪЙе§ФцЗДгІЫйТЪОљдіДѓ
C.ДяЕНЦНКтЪБЃЌЛьКЯЦјЬхЕФбЙЧПБЃГжВЛБф
D.10 sЪБЃЌе§ЁЂФцЗДгІЫйТЪЯрЕШ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏбЇгУгяЪЧбЇЯАЛЏбЇЕФживЊЙЄОпЃЌЯТСагУРДБэЪОЮяжЪБфЛЏЕФЛЏбЇгУгяжаЃЌе§ШЗЕФЪЧЃЈ ЃЉ
A.ЭзїЕчМЋВФСЯЕчНтБЅКЭЪГбЮЫЎЪБзмЗДгІЮЊЃК2H2O+2ClЃ![]() Cl2Ёќ+H2Ёќ+2OHЃ
Cl2Ёќ+H2Ёќ+2OHЃ
B.ЧІаюЕчГиГфЕчЪБбєМЋЗДгІЪНЮЊЃКPbSO4Ѓ2eЃ+2H2O=PbO2+4H++SO42Ѓ
C.ДжЭОЋСЖЪБЃЌгыЕчдДе§МЋЯрСЌЕФЪЧДПЭЃЌЕчМЋЗДгІЪНЮЊЃКCuЃ2eЃ=Cu2+
D.ИжЬњЗЂЩњЕчЛЏбЇИЏЪДЕФе§МЋЗДгІЪНЃКFeЃ3eЃ=Fe3+
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЃЈ1ЃЉаДГіЕчзгЪНЃКKOH________________________ЃЛCO2_______________________
ЃЈ2ЃЉгУЕчзгЪНБэЪОЯТСаЛЏКЯЮяЕФаЮГЩЙ§ГЬЃКCaF2ЃК___________________________________
H2SЃК____________________________________________________________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊгавдЯТЮяжЪЯрЛЅзЊЛЏ
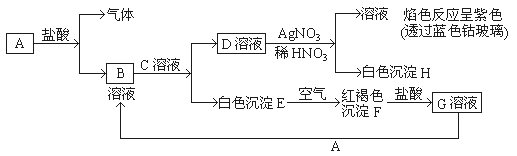
ЪдЛиД№ЃКЃЈ1ЃЉаДГіBЕФЛЏбЇЪН_________ЃЌDЕФЛЏбЇЪН ______ЁЃ
ЃЈ2ЃЉаДГігЩEзЊБфГЩFЕФЛЏбЇЗНГЬЪН ______________ЁЃ
ЃЈ3ЃЉаДГіGзЊЛЏГЩBЕФРызгЗНГЬЪН ___________ЃЛ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАб1 L 0.1 mol/LЕФДзЫсШмвКгУеєСѓЫЎЯЁЪЭЕН10 LЃЌЯТСаа№Ъіе§ШЗЕФЪЧЃЈЁЁЁЁЃЉ
A. cЃЈCH3COOHЃЉБфЮЊдРДЕФ1/10
B. cЃЈHЃЋЃЉБфЮЊдРДЕФ![]()
C. cЃЈCH3COOЃЃЉ/cЃЈCH3COOHЃЉЕФБШжЕдіДѓ
D. ШмвКЕФЕМЕчаддіЧП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПзюНќвтДѓРћПЦбЇМвЛёЕУСЫМЋОпРэТлбаОПвтвхЕФN4ЗжзгЁЃN4ЗжзгНсЙЙШчЭМЫљЪОЃЌвбжЊЂёЁЂЖЯСб1 mol NЁЊNЮќЪе167 kJШШСПЃЌаЮГЩ1 mol ![]() ЗХГі942 kJШШСПЃЛЂђЁЂN2(g)ЃЋ3H2(g)
ЗХГі942 kJШШСПЃЛЂђЁЂN2(g)ЃЋ3H2(g)![]() 2NH3(g) ІЄH1ЃНЃ92 kJ/molЃЌN4(g)ЃЋ6H2(g)
2NH3(g) ІЄH1ЃНЃ92 kJ/molЃЌN4(g)ЃЋ6H2(g)![]() 4NH3(g) ІЄH2(kJ/mol)ИљОнвдЩЯаХЯЂКЭЪ§ОнЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
4NH3(g) ІЄH2(kJ/mol)ИљОнвдЩЯаХЯЂКЭЪ§ОнЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)

A.ІЄH2ЃО0B.N2ЗжзгБШN4ЗжзгЮШЖЈ
C.ІЄH2ЃН2ІЄH1D.ІЄH2гыЗНГЬЪНЯЕЪ§ЮоЙи
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com