
【题目】
A. ①③⑤ B. ②③⑤ C. ①②④ D. ②④⑤
科目:高中化学 来源: 题型:
【题目】碱式碳酸镁可用于牙膏、医药和化妆品等工业,化学式为4MgCO3Mg (OH)25H2O,某碱式碳酸镁中含有SiO2杂质,为测定其纯度,某兴趣小组设计了如下方案: 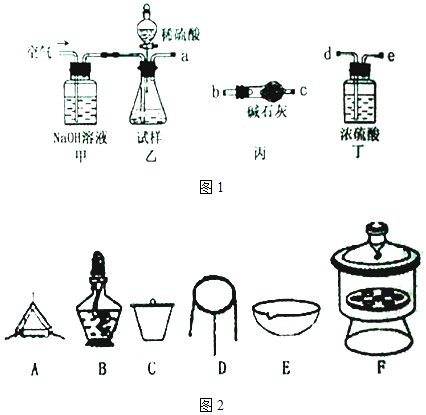
方案I 取一定质量的样品,与硫酸充分反应,通过测定生成CO2的质量计算纯度
(1)乙中发生反应的方程式为 .
(2)仪器接口的连接顺序为(装置如图1可以重复使用)a , 丁的作用是 .
(3)当样品充分反应完后,缓慢通入空气的目的是 .
(4)方案 II①称取碱式碳酸镁样品mg;②将样品充分高温煅烧,冷却后称量;③重复操作②,测得剩余固体质量为m1g 下列仪器如图2中,该方案不会用到的是 .
(5)判断样品完全分解的方法是;本实验至少需要称量次.
(6)有同学认为方案 II高温煅烧的过程中会发生4MgCO3+SiO2 ![]() MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点正确吗?(填“正确”或“错误”)请说明理由: .
MgSiO3+CO2↑会导致测定结果有误,你认为这位同学的观点正确吗?(填“正确”或“错误”)请说明理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学进行SO2的性质实验。在点滴板a、b、c处分别滴有不同的试剂,再向Na2SO3固体上滴加数滴浓H2SO4后,在整个点滴板上盖上培养皿,一段时间后观察到的实验现象如下表所示。( )
序号 | 试剂 | 实验现象 |
|
a | 品红溶液 | 红色褪去 | |
b | 酸性KMnO4溶液 | 紫色褪去 | |
c | NaOH溶液(含2滴酚酞) | 红色褪去 |
下列说法正确的是
A.浓硫酸与Na2SO3固体发生了氧化还原反应
B.a、b均表明SO2具有漂白性
C.c中只可能发生反应:SO2+ 2OH—= SO32-+ H2O
D.c中所得溶液的离子浓度一定存在关系:c(Na+)+c(H+) = 2c(SO32-) +c(HSO3) + c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用右图所示装置制备乙酸乙酯。实验如下:( )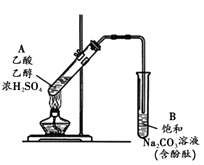
① 向浓H2SO4乙醇混合液中滴入乙酸后,加热试管A
② 一段时间后,试管B中红色溶液上方出现油状液体
③ 停止加热,振荡试管B,油状液体层变薄,下层红色溶液褪色
④ 取下层褪色后的溶液,滴入酚酞后又出现红色
结合上述实验,下列说法正确的是
A.①中加热利于加快酯化反应速率,故温度越高越好
B.③中油状液体层变薄主要是乙酸乙酯溶于Na2CO3溶液所致
C.③中红色褪去的原因可能是酚酞溶于乙酸乙酯中
D.取②中上层油状液体测其,共有3组峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极. 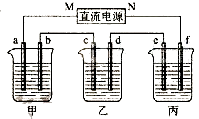
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
①电源的N端为极;
②电极b上发生的电极反应为;
③列式计算电极b上生成的气体在标准状况下的体积:
④电极c的质量变化是g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液;
乙溶液;
丙溶液;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某学生的化学实验中有如下记录,其中能达到测量要求的是( )
A. 用托盘天平称取35.20 g NaCl B. 用10 mL量筒量取8.5 mL盐酸
C. 用50 mL 烧杯量取15.80 mL溶液 D. 用250 mL 容量瓶量取25 mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时发生反应:CO(g)+2H2(g)![]() CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 5 |
n(CH3OH) (mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(1)下图中表示CH3OH的浓度变化的曲线是_________(填字母)。

(2)用H2表示从0~2s内该反应的平均速率v(H2) =__________。随着反应的进行,该反应的速率在逐渐减慢的原因是 _____________。
(3)能说明该反应已达到平衡状态的是________。
a.容器内CO与CH3OH的浓度相等 b.v逆(CO) = v正(H2)
c.容器内气体的密度保持不变 d.容器内气体的压强不变
(4)该反应是一个放热反应,说明该反应中破坏1mol CO和2mol H2的化学键吸收的能量_________形成1mol CH3OH释放的能量(填“﹤”、“=”或“﹥”)。
(5)已知在400 ℃时,反应CO(g)+2H2(g)![]() CH3OH(g) 生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q =_________kJ。
CH3OH(g) 生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q =_________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3和FeO)得到绿矾(主FeSO47H2O),再通过绿矾制备铁黄[FeO(OH)]的流程如下:烧渣 ![]() 溶液
溶液 ![]() 绿矾
绿矾 ![]() 铁黄 已知:FeS2和铁黄均难溶于水下列说法不正确的是( )
铁黄 已知:FeS2和铁黄均难溶于水下列说法不正确的是( )
A.步骤①,最好用硫酸来溶解烧渣
B.步骤②,涉及的离子反应为FeS2+14Fe3++8H2O═15Fe2++2SO42﹣+16H+
C.步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D.步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com