
| A、1,2-二氯丙烷 |
| B、1,1-二氯丙烷 |
| C、1,3-二氯丙烷 |
| D、2,2-二氯丙烷 |


科目:高中化学 来源: 题型:
| 物 质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |

查看答案和解析>>
科目:高中化学 来源: 题型:
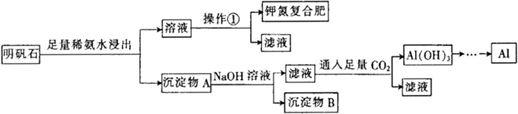
查看答案和解析>>
科目:高中化学 来源: 题型:
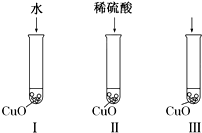 氧化铜是一种黑色固体,可溶于稀硫酸.某化学兴趣小组为探究稀硫酸中哪种粒子能使氧化铜溶解,该小组同学提出如下假设:
氧化铜是一种黑色固体,可溶于稀硫酸.某化学兴趣小组为探究稀硫酸中哪种粒子能使氧化铜溶解,该小组同学提出如下假设:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑤⑥⑦ | B、②⑤⑦⑥ |
| C、①③⑤⑥⑦ | D、③④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、b=2 |
| B、容器中一定没有残余的CO2和水蒸气 |
| C、a≥b |
| D、反应中转移的电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 空气 |
| △ |
| HNO3(稀) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com