
下列各项不正确的是
| A.等物质的量浓度的下列溶液中① NH4Al(SO4)2② NH4Cl,③CH3COONH4,④ NH3·H2O; c(NH4+),由大到小的顺序是①>②>③>④ |
B.室温下,向0.01mol/L NH4HSO4溶液中滴加NaOH溶液至中性 |
| C.25℃时,0.1mol/LCH3COOH溶液V1 mL和0.1mol/L NaOH溶液V2mL混合,若V1>V2,则混合溶液的pH一定小于7 |
D.对于反应 ,在任何温度下都能自发进行 ,在任何温度下都能自发进行 |
科目:高中化学 来源: 题型:单选题
相同温度下,体积均为1.5 L的两个恒容容器中发生可逆反应:
X2 (g+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
2XY3(g) ΔH=-92.6 kJ·mol-1,实验测得有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于化学反应方向的确定,下列说法正确的是( )
| A.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向 |
| B.温度、压强一定时,吸热的熵增反应一定能够自发进行 |
| C.反应焓变是决定反应能否自发进行的唯一因素 |
| D.固体的溶解过程与熵变无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于反应A (g)+ 3B(g) =" 2C(g)" + 2D(g),下列数据表示反应进行得最快的是( )
A.v(A)=0.7mol/(L·s) B.v (B) ="1.8mol/(L" · s)
C.v (C)=1mol/(L·s) D.v (D) =1.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某温度下,在一个2L的密闭容器中,加人4 mol A和2 molB进行如下反应:3A(g)+2B(g)  4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
| A.此时,B的平衡转化率是40% |
| B.增加B,平衡向右移动,B的平衡转化率增大 |
C.该反应的化学平衡常数表达式是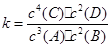 |
| D.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学平衡常数(K)、电离常数(Ka、Kb)、溶度积常数(Ksp)等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
| A.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 |
| B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸强 |
| C.向氯化钡溶液中加入同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3) |
| D.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组物质的变化不能用勒夏特列原理解释的是( )
| A.氯水在光照条件下颜色变浅最终变为无色 |
| B.将FeS固体投入到含有Cu2+的废水中以除去Cu2+ |
| C.500 ℃时比室温更利于合成氨 |
| D.乙酸乙酯的合成中用浓硫酸比稀硫酸更有利于乙酸乙酯的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在密闭的容积可变的容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)  2C(g) ΔH<0。达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )
2C(g) ΔH<0。达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )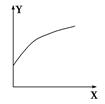
| | X | Y |
| A | 再加入A | B的转化率 |
| B | 降低温度 | 混合气体的密度 |
| C | 增大压强 | A的转化率 |
| D | 升高温度 | 混合气体的平均摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定条件下,发生如下反应:2A(g)+2B(g) 3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
3C(g)+ D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
| A.单位时间内生成n mol B,同时消耗3n mol C |
| B.容器内压强不随时间而变化 |
| C.混合气体的密度不随时间变化 |
| D.单位时间内生成2n mol A,同时生成n mol D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com