
【题目】在反应3Cl2+2FeBr2===2FeCl3+2Br2中被还原的元素是)
A. Fe B. Fe和Cl C. Cl D. Br
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】海水占地球总蓄水量的97.2%,若把海水的淡化和化工生产结合起来,就可充分利用海洋资源来解决淡水资源缺乏的问题。
(1)氯化钠中的金属元素在周期表中的位置是_________;
(2)目前常用的“海水淡化”主要技术之一是蒸馏法,蒸馏法属于________(填“物理变化”或“化学变化”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。
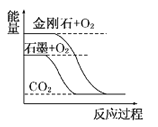

据此判断下列说法中正确的是( )
A. 石墨转变为金刚石是吸热反应 B. 白磷比红磷稳定
C. S(g)+O2(g)===SO2(g) ΔH1S(s)+O2(g)=SO2(g) ΔH2 则ΔH1>ΔH2 D. CO(g)+H2O(g)=CO2(g)+H2(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅在氧气中完全燃烧的化学方程式为:Si+O2 ![]() SiO2 , 1molSi完全燃烧生成SiO2放出992kJ的热量.已知断裂1molSi﹣Si键、1molO=O键和1molSi﹣O键吸收的能量分别为176kJ、496kJ、460kJ.晶体结构知识告诉我们,1molSiO2中含有4molSi﹣O键,则1molSi中含有Si﹣Si键的物质的量为( )
SiO2 , 1molSi完全燃烧生成SiO2放出992kJ的热量.已知断裂1molSi﹣Si键、1molO=O键和1molSi﹣O键吸收的能量分别为176kJ、496kJ、460kJ.晶体结构知识告诉我们,1molSiO2中含有4molSi﹣O键,则1molSi中含有Si﹣Si键的物质的量为( )
A.1mol
B.2mol
C.3mol
D.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.硅的原子结构示意图: 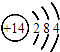
B.原子核内有8个中子的氧原子: ![]() O
O
C.二氧化碳分子的电子式: ![]()
D.甲烷分子的比例模型: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①C(s)+ ![]() O2(g)═CO(g);△H=﹣110.5kJmol﹣1
O2(g)═CO(g);△H=﹣110.5kJmol﹣1
②C(s)+O2(g)═CO2(g);△H=﹣393.51kJmol﹣1
则反应C(s)+CO2(g)═2CO(g)的△H为( )
A.﹣283.01 kJmol﹣1
B.+172.51 kJmol﹣1
C.+283.01 kJmol﹣1
D.﹣172.51 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁在下列情况下腐蚀最快的是
A. 铁放入海水中 B. 将铁和锌连接后放入到海水中
C. 将铁和锌连接后放入到淡水中 D. 将铁和锡连接后放入到海水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中可能含有如下几种阴阳离子:
阳离子 | Fe3+、Al3+、Fe2+、Ba2+、Na+ |
阴离子 | Cl-、CO32-、NO3-、SO42-、S2- |
现对该废水样品进行以下研究:
Ⅰ.向试管中滴加浓盐酸,有少量的无色气体生成,气体遇空气立即变为红棕色;
Ⅱ.若向Ⅰ所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅲ.若向Ⅰ所得的溶液中加入过量的NaOH溶液,有红褐色沉淀生成。过滤后向所得滤液中通入过量的CO2气体,有白色絮状沉淀生成。
根据上述实验,回答下列问题:
(1)该废水中一定含有的阴离子是 _____,一定不含有的阳离子是_____;
(2)写出Ⅰ中产生无色气体的反应的离子方程式:______;
(3)写出Ⅲ中通入过量CO2产生白色絮状沉淀所发生的反应离子方程式:______;
(4)在废水中加入新制氯水,测得溶液中c(Fe3+)=1.0×10-2mol·L-1,c(Al3+)=1.0×10-3mol·L-1。要想使Fe3+完全沉淀(离子浓度为1.0×10-5mol·L-1)而Al 3+不沉淀,则应调节溶液pH范围为______。(已知常温下Fe(OH)3的Ksp=1.0×10-38,Al(OH)3的Ksp=1.0×10-33)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应式为:Zn﹣2e﹣+2OH﹣=Zn(OH)2
B.放电时每转移3mol电子,正极有1 mol K2FeO4被还原
C.充电时阴极附近溶液的碱性增强
D.放电时正极反应式为:Fe(OH)3﹣3e﹣+5OH﹣=FeO42﹣+4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com