
【题目】选用一种试剂就能把浓度均为lmol/L的CuCl2、Na2SO4、NaNO3、AlCl3溶液加以区别,这种试剂是
A. CaCl2 B. AgNO3 C. Ba(OH)2 D. H2SO4
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:
【题目】我国对可呼吸的钠-二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO2![]() 2Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是
2Na2CO3+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中)。关于该电池,下列说法错误的是

A. 充电时,Na+从阳极向阴极移动
B. 可以用乙醇代替TEGDME做有机溶剂
C. 放电时,当转移1mol电子负极质量减轻23g
D. 放电时,正极反应为3CO2 + 4Na++4e- = 2Na2CO3 + C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 浓盐酸 | MnO2 | 产生黄绿色气体 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 酸化的FeCl2溶液 | H2O2溶液 | 溶液变成棕黄色,有气泡产生 |
D | Fe2(SO4)3溶液 | 铜粉 | 溶液变蓝色、有黑色固体产生 |

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氧化锌和金属锌。
Ⅰ.制取氧化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Zn2+ | 5.2 | 6.4 |
Fe2+ | 5.8 | 8.8 |
(1)为了加快反应,“酸溶”需要适当加热,但温度不宜太高,原因是_________。
(2)加入H2O2溶液发生反应的离子方程式_______。
(3)流程图中,为了降低溶液的酸度,调节pH范围为_______;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为________。
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为______。从ZnCl2溶液中提取无水ZnCl2的方法是__________.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O=Na2[Zn(OH)4](aq),然后电解浸取液。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是______。
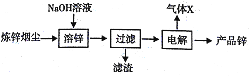
(6)以石墨作电极电解时,阳极产生的气体为______;阴极的电极反应为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2MOyx-+5S2-+16H+=2M2++5S↓+8H2O,则MOyx-中的M的化合价为
A. +3 B. +4 C. +6 D. +7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某化学研究性学习小组对某无色水样成分的检验过程,已知该水样中只可能含有 K+、Fe3+、Cu2+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子,该小组同学取 100 mL 水样进行实验:向样品中先滴加氯化钡溶液,再滴加 1 mol·L-1 盐酸,实验过程中沉淀质量的变化如图所示。下列说法正确的是

A. 水样中一定不存在Fe3+、Cu2+,可能存在Ag+
B. 水样中一定存在CO32-、SO42-、Cl-
C. BC段曲线所表示的离子方程式为CO32-+2H+=H2O+CO2↑
D. 水样中一定存在K+,且c(K+)≥0.6mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过以下操作流程:
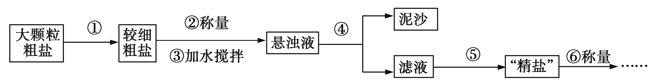
(1)操作①中必须用到的一种仪器是 (填序号)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到的仪器是 。
(3)实验结束后称量获得的“精盐”,并计算“精盐”的制得率,发现制得率较低,其可能原因是 (填序号)。
A.粗盐没有全部溶解即过滤 B.蒸发时液滴飞溅剧烈
C.蒸发后所得“精盐”很潮湿 D.蒸发皿上粘有的“精盐”没有全部转移到称量纸上
(4)小明查阅相关资料得知:粗盐中除含泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质。为了得到较纯净的氯化钠,小明将上述流程图中操作⑤得到的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种)。
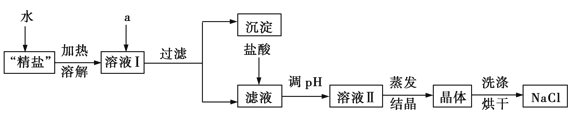
①提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、KOH溶液、饱和NaCl溶液。
从提供的试剂中选出a所代表的试剂是 、 。
②在滤液中加盐酸的作用是 、 (用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质制备的说法中正确的是( )
A. 将饱和FeCl3溶液滴入到NaOH溶液中加热煮沸可制得Fe(OH)3胶体
B. 可用Na从TiCl4的水溶液中生产Ti
C. 工业上利用氯气和石灰水反应生产漂白粉和漂粉精
D. 可用石英、石灰石、纯碱在高温下生产玻璃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液电导率越大导电能力越强.常温下用0.100mol·L-1盐酸分别滴定10.00mL浓度均为0.100mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氮相似,常温Kb[(CH3)2NH]=1.6×10-4。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
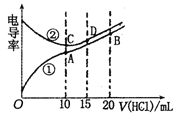
A. 曲线②代表滴定二甲胺溶液的曲线
B. A点溶液中:c(H+)=c(OH-)+c[(CH3)2NH·H2O]
C. D点溶液中:2c(Na+)=3c(Cl-)
D. 在相同温度下,A、B、C、D四点的溶液中,水的电离程度最大的是C点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com