
【题目】“封管实验”具有简易、方便、节约、绿色等优点。观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是
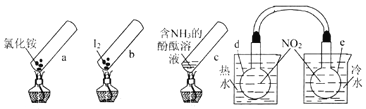
A.加热时,a上部聚集了固体NH4Cl,说明NH4C1的热稳性比较好
B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体
C.加热时,c中溶液红色变深,冷却后又变浅
D.水浴时,d内气体颜色变浅,e内气体颜色加深
【答案】B
【解析】
A、加热时氯化铵分解生成氨气和氯化氢,在试管的顶部氨气和氯化氢又反应生成氯化铵,NH4Cl的热稳定性较差,故A错误;
B、加热碘升华,变为紫色蒸气,在上部冷却聚集为紫黑色的碘固体,故B正确;
C、氨水显碱性,使酚酞变红,加热时,氨气逸出,溶液红色变浅,冷却后,氨气又溶于水和水反应,溶液红色又变深,故C错误;
D、容器中存在平衡2NO2(g)![]() N2O4(g) △H=-92.4kJ/mol,正反应为放热反应,d浸泡在热水中,升高温度平衡向逆反应方向移动,二氧化氮浓度增大,d容器内气体颜色变深;e浸泡在冷水中,温度降低平衡向正反应移动,二氧化氮浓度降低,e容器内气体颜色变浅,故D错误,
N2O4(g) △H=-92.4kJ/mol,正反应为放热反应,d浸泡在热水中,升高温度平衡向逆反应方向移动,二氧化氮浓度增大,d容器内气体颜色变深;e浸泡在冷水中,温度降低平衡向正反应移动,二氧化氮浓度降低,e容器内气体颜色变浅,故D错误,
答案选B。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】利用反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=+746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
2CO2(g)+N2(g) ΔH=+746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
A.降低温度B.缩小体积使压强增大
C.升高温度同时充入N2D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素W、X、Y、Z的原子序数依次增加,p、q、r是由这些元素组成的二元化合物;m、n分别是元素Y、Z的单质,n通常为深红棕色液体,p为最简单的芳香烃,s通常是难溶于水、密度比水大的油状液体。上述物质的转化关系如图所示:
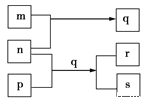
(1)q的溶液显______性(填“酸”“碱”或“中”),理由是:_________(用离子方程式说明)。
(2)s的化学式为______,Z在周期表中的位置为_____________。
(3)X、Y两种元素组成的化合物能溶于足量的浓硝酸,产生无色气体与红棕色气体的体积比为1:13,则该化合物的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 2SO2(g)+O2(g) ![]() 2SO3(g) 在恒温恒容密闭容器中进行,下列可作为判断其达到平衡状态的标志的是( )
2SO3(g) 在恒温恒容密闭容器中进行,下列可作为判断其达到平衡状态的标志的是( )
①SO2 和 SO3 的浓度相等 ②SO2 的质量分数保持不变 ③容器中气体的压强保持不变 ④SO3 的生成速率与 SO2 的消耗速率相等 ⑤容器中混合气体的密度保持不变⑥容器中气体的平均摩尔质量保 持不变 ⑦2v 正(SO2)=v 逆(O2) ⑧单位时间内生成 n mol O2 的同时消耗 2n mol SO3
A. ①②④⑤ B. ②③⑦⑧ C. ②③⑤⑥ D. ②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出)。
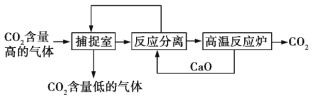
下列有关该方法的叙述中正确的是
①能耗小是该方法的一大优点
②整个过程中,有两种物质可以循环利用
③“反应分离”环节中,分离物质的基本操作是过滤、蒸发、结晶
④该方法可减少碳排放,“捕捉”到的CO2还可用来制备甲醇等产品
A.①③B.②④C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
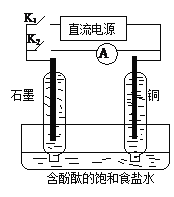
A. 断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲中可能含有NO、CO2、NO2、NH3、N2中的几种,将100mL气体甲经过如图所示实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
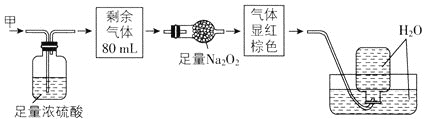
A.NO2、NH3、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)臭氧可用于烟气脱硝。O3氧化NO结合水洗,可产生HNO3和O2,该反应的化学方程式为_________________________。
(2)如图是用NH3脱除烟气中NO的原理。
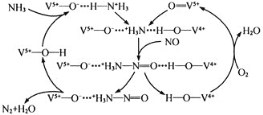
①该脱硝原理中,NO最终转化为__________(填化学式)和H2O。
②当消耗2mLNH3和0.5molO2时,除去的NO在标准状况下的体积为________L。
(3)用碱液脱硝是目前研究的课题之一。
①将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO3)2。该工艺需控制NO和NO2物质的量之比接近1:1。若n(NO2):n(NO)>1:1,则会导致_____________;若n(NO2):n(NO)<1:1,则会导致_____________。
②将氢氧化钠溶液脱硝得到的NaNO2、NaNO3的混合液和NaOH溶液分别加到如图所示的电解槽中进行电解。写出A室NO2-发生的电极反应式:______________。
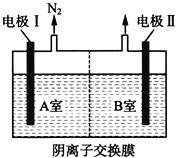
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将石油分馏得到的重油进行裂化可以获得较多的轻质燃油。某研究性学习小组模拟工业.上石油的催化裂化设计了如图所示实验装置。实验过程中可观察到烧瓶中固体石蜡先熔化,试管II中有少量液体生成,试管巩中酸性高锰酸钾溶液褪色,实验后闻试管II中液体的气味,发现其具有汽油的气味。

资料一 石蜡是含有20 ~ 30个碳原子的烷烃组成的混合物,常温下呈固态。
资料二 石油催化裂化过程中通常使用![]() 作催化剂。
作催化剂。
(1)为保证实验成功,实验前必须进行的操作是_________________;装置中长导管的作用是________________________。
(2)试管II中有少量液体生成说明________________。
(3)试管III中溶液褪色说明_______________________。
(4)_______(填“能”或“不能”)用试管II中的液体萃取溴水中的溴,理由是___________。
(5)写出二十烷裂化得到癸烷和癸烯的化学方程式:___________________________。
(6)石油裂化的主要目的是_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com