
【题目】将石油分馏得到的重油进行裂化可以获得较多的轻质燃油。某研究性学习小组模拟工业.上石油的催化裂化设计了如图所示实验装置。实验过程中可观察到烧瓶中固体石蜡先熔化,试管II中有少量液体生成,试管巩中酸性高锰酸钾溶液褪色,实验后闻试管II中液体的气味,发现其具有汽油的气味。

资料一 石蜡是含有20 ~ 30个碳原子的烷烃组成的混合物,常温下呈固态。
资料二 石油催化裂化过程中通常使用![]() 作催化剂。
作催化剂。
(1)为保证实验成功,实验前必须进行的操作是_________________;装置中长导管的作用是________________________。
(2)试管II中有少量液体生成说明________________。
(3)试管III中溶液褪色说明_______________________。
(4)_______(填“能”或“不能”)用试管II中的液体萃取溴水中的溴,理由是___________。
(5)写出二十烷裂化得到癸烷和癸烯的化学方程式:___________________________。
(6)石油裂化的主要目的是_______________________________。
【答案】检查装置的气密性 导气和冷凝气体 裂化生成了碳原子数大于4小于10的烃 裂化生成了碳原子数小于5的不饱和烃 不能 裂化产物中含有烯烃等不饱和烃,能与 ![]() 发生加成反应
发生加成反应 ![]() 提高石油产品中轻质燃油,特别是汽油的产量和质量
提高石油产品中轻质燃油,特别是汽油的产量和质量
【解析】
(1)装入药品之前要检查装置的气密性;根据石油分馏工业中的分馏塔原理,设置了长导管,其作用除导气外,还有冷凝气体。
故答案为: 检查装置的气密性;导气和冷凝气体;
(2)试管II中有液体生成,说明裂化生成了含4个碳原子以上的烃,因为常温常压下,碳原子数大于4小于10的烃一般呈液态。
故答案为:裂化生成了碳原子数大于4小于10的烃 ;
(3)试管III中酸性![]() 溶液褪色说明裂化生成了碳原子数小于5的不饱和烃(常温常压下呈气态)。
溶液褪色说明裂化生成了碳原子数小于5的不饱和烃(常温常压下呈气态)。
故答案为:裂化生成了碳原子数小于5的不饱和烃;
(4)由于裂化产物中有烯烃等不饱和烃,能与![]() 发生加成反应,所以不能用来萃取溴单质。
发生加成反应,所以不能用来萃取溴单质。
故答案为:不能 ;裂化产物中含有烯烃等不饱和烃,能与 ![]() 发生加成反应;
发生加成反应;
(5)二十烷裂化得到癸烷和癸烯的化学方程式:![]() ;
;
故答案为:![]() ;
;
(6)石油裂化的主要目的是获得更多的轻质燃油,特别是提高汽油的产量和质量。
故答案为:提高石油产品中轻质燃油,特别是汽油的产量和质量。


科目:高中化学 来源: 题型:
【题目】“封管实验”具有简易、方便、节约、绿色等优点。观察下列四个“封管实验”(夹持装置未画出),判断下列说法正确的是
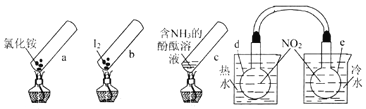
A.加热时,a上部聚集了固体NH4Cl,说明NH4C1的热稳性比较好
B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体
C.加热时,c中溶液红色变深,冷却后又变浅
D.水浴时,d内气体颜色变浅,e内气体颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总质量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量,上述能说明2NO2(g) ![]() N2O4(g)达到平衡状态的有( )个
N2O4(g)达到平衡状态的有( )个
A.4B.6C.3D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了在实验室利用工业原料制备少量氨气,有人设计了如图所示的装置(图中夹持装置均已去)。
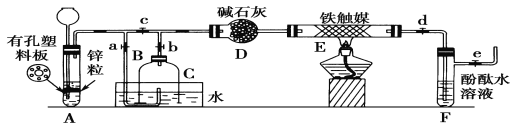
实验操作:
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗中注入一定量稀硫酸。打开弹簧夹c、d、e,A中有氢气产生。在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如上图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是______________________________________。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是_________,C瓶内气体的成分是____________。
(3)在步骤③中,先加热铁触媒的原因是________________________。反应管E中发生反应的化学方程式是_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是
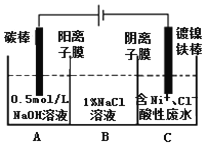
已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比是重要的学习方法,类比pH的定义可定义pOH和pKW。在某弱酸HX及其盐NaX的混合溶液中(HX和NaX的含量不确定),c(H+)和c(OH-)存在如图所示的关系,则下列说法不正确的是
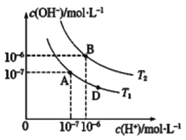
A. 图中温度T2>25℃
B. 若此混合溶液呈酸性且c(HX)=c(NaX),则HX电离能力大于NaX的水解能力
C. 位于AB线段上任意点的溶液均有pH=pOH=![]()
D. 图中D点处溶液中离子浓度:c(Na+)>c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH和体积均相同的HNO2和CH3COOH溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
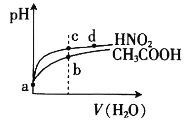
A.电离平衡常数:Ka(CH3COOH)>Ka(HNO2)
B.从c点到d点,溶液中 的值保持不变
的值保持不变
C.溶液中水的电离程度:b>c
D.a点时,相同体积的两溶液分别与NaOH恰好中和后,溶液中的n(Na+)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请写出下列物质的电子式:
(1)H2S________; (2)CO2________; (3)N2________;
(4)OH-________; (5)HClO________;(5)Na2O2________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以玉米为原料进行综合利用,可以提高经济效益,减少对环境的污染。如图所示为用玉米作原料制取各物质的转化过程。
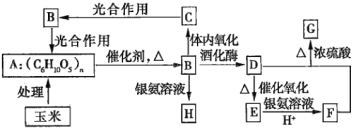
已知:
Ⅰ.G是具有果香气味的液体;D是重要的化工原料,并且可以代替汽油作汽车燃料。
Ⅱ.![]() 。
。
(1)A的名称为________,B的分子式为________,F的结构简式为________,G的结构简式为________。
(2)下列关于B的说法正确的是________(填序号)。
a.1molB能水解生成2molCH3CH2OH和2molCO2
b.欲检验A生成的B是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2悬浊液并加热
c.B不能发生酯化反应
d.蔗糖的水解产物之一为B
(3)由C→B的能量转化过程中,能量的转化形式为________能转化为________能。
(4)D→E的化学方程式为________________。
(5)写出足量的F与甘油、浓硫酸在加热条件下发生反应的化学方程式:________________,反应类型为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com