
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A.  <1.0×10-7mol/L
<1.0×10-7mol/L
B. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
【答案】C
【解析】A、因为溶液显酸性,因此有Kw/c(H+) <10-7,故A说法正确;B、因为两者是等体积等浓度加入,因此NH4HCO3和NaCl物质的量相等,即n(Na+)=n(HCO3-),根据物料守恒,因此有c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3),故B说法正确;C、发生的反应是NH4HCO3+NaCl=NaHCO3↓+NH4Cl,溶液有NH4Cl和一部分NaHCO3,因此依据电中性,有c(H+)+c(Na+)+c(NH4+)=c(OH-)+c(HCO3-)+c(Cl-)+2c(HCO3-),故C说法错误;D、根据选项C的分析,离子浓度大小顺序是 c(Cl-)> c(NH4+)> c(HCO3-)> c(CO32-),故D说法正确。


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:高中化学 来源: 题型:
【题目】如图为元素周期表短周期的一部分,Z原子的电子层数为n,最外层电子数为2n+1。下列叙述错误的是

A. X和Z氢化物的热稳定性和还原性均依次减弱
B. R、W和氢三种元素形成的阴离子有2种以上
C. RY2分子中每个原子的最外层均为8电子结构
D. R、Y、Z的最高价氧化物对应的水化物的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研宄在其他条件不变时,改变某一条件对A2(g) +3B2 (g) ![]() AB3 (g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如图可得出的判断结论正确的是( )
AB3 (g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如图可得出的判断结论正确的是( )
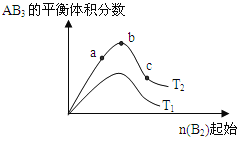
A.反应速率a>b>c
B.若T2>T1,则正反应一定是吸热反应
C.达到平衡时,AB3的物质的量大小为:b>c>a
D.达到平衡时A2的转化率大小为:b>a>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙酮是一种常用的有机溶剂,可与水以任意体积比互溶,密度小于1 g/mL,沸点约55 oC,分离水和丙酮时最合理的方法是
A. 蒸发 B. 分液 C.过滤 D. 蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反 应mX(g) ![]() nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确的是( )
气体体积/L c(Y)/molL-1 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
A.m>n+p
B.Q<0
C.温度不变,压强增大,Y的体积分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一支25mL的酸式滴定管中盛入0.1mol/L-1 HCl溶液,其液面恰好在5mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.1mol/L-1 NaOH溶液进行滴定,则所需NaOH溶液的体积
A.大于20mL B.小于20mL C.等于20mL D.等于5mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验或操作不能达到目的的是( )
A. 制取溴苯:将铁屑、溴水、苯混合加热
B. 用 NaOH 溶液除去溴苯中的溴
C. 鉴别己烯和苯:向己烯和苯中分别滴入酸性 KMnO4 溶液,振荡,观察是否褪色
D. 除去甲烷中含有的乙烯:将混合气体通入溴水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)达到平衡状态,其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)达到平衡状态,其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K[来 | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= ;再充入CO2气体,则平衡 移动(选“正向移动”、“逆向移动”或“不移动”),平衡常数K (选“增大”、“减小”或“不变”)。
(2)该反应的逆反应方向为 反应方向(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下的各物质平衡浓度符合:c(CO2)=c(CO),c(H2)=c(H2O),试判断此时的温度为 ℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
A.使用催化剂,可加快反应速率,目的是提高生产效率
B.使用冰箱保存食物,是利用了化学反应速率理论
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使用有限原料多出产品
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com