
【题目】下面有关Na2CO3与NaHCO3的性质比较中错误的是
A.相同浓度溶液的碱性:Na2CO3>NaHCO3
B.同条件下在水中的溶解度:Na2CO3>NaHCO3
C.与同浓度的硫酸反应放出气泡的速率:NaHCO3 <Na2CO3
D.热稳定性:NaHCO3 <Na2CO3
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列有关有机物结构、性质的说法正确的是( )
A. 石油的分馏、裂化和煤的气化、液化、干馏都是化学变化
B. 乙烯与苯都能与H2发生加成反应,说明二者分子中所含碳碳键相同
C. 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应
D. 蔗糖、油脂、蛋白质都能发生水解反应,都属于天然有机高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘,有甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O。请回答:
(1)步骤X使用分液漏斗前须检漏,检漏方法为_________。
(2)用右图所示装置进行蒸馏。指出右图所示实验装置中的任意两处错误:
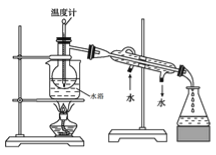
①___________;②__________。
(3)进行上述操作时,使用水浴加热更好的原因是___________;最后碘晶体在__________里聚集。
(4)下列有关步骤Y的说法,正确的是________。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
(5)方案乙在上层溶液中加入H2SO4溶液得到I2的水溶液发生的反应方程式是:_____________;
(6)操作Z的名称是____________。
(7)工业中采用方案乙从海带中提取碘,方案甲中采用蒸馏不合理,理由是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关盐酸、硝酸、硫酸的叙述正确的是( )
A.都是无色液体
B.都是易挥发有刺激性气味的液体
C.浓溶液在空气中都有白雾生成
D.都是易溶于水的强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中可以大量共存的是( )
A.H+、SO32﹣、S2﹣、K+
B.Fe3+、Cl﹣、S2﹣、Ba2+
C.Cu2+、Cl﹣、S2﹣、K+
D.Na+、K+、S2﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强碱性溶液中可能含有的离子是K+、NH![]() 、Al3+、AlO
、Al3+、AlO![]() 、SO
、SO![]() 、SiO
、SiO![]() 、CO
、CO![]() 、Cl-中的某几种离子,现进行如下实验:
、Cl-中的某几种离子,现进行如下实验:
①取少量的溶液用硝酸酸化后,加Ba(NO3)2溶液,无沉淀生成;
②另取少量溶液加入盐酸,其现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失。
(1)原溶液中肯定存在的离子是,肯定不存在的离子是。
(2)已知一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187g,则原溶液中是否含有Cl- ?。
(3)按照反应顺序逐步书写出②中发生反应的离子反应方程式
①H++OH-=H2O②
③
④HCO3-+H+=H2O+CO2↑
⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知FeCl3溶液中存在下列平街:Fe3+ + 3 H2O![]() Fe(OH)3 + 3 H+,下列操作能使FeCl3的水解程度增大且溶液的酸性增强的是( )
Fe(OH)3 + 3 H+,下列操作能使FeCl3的水解程度增大且溶液的酸性增强的是( )
A.加入FeCl3固体 B.加水 C.加入少量浓盐酸 D.升温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com