
下列实验操作不正确的是
A.实验室制乙烯时,为防止暴沸,应加入沸石
B.不慎将苯酚溶液沾到皮肤上,应立即用稀NaOH溶液清洗
C.饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
D.向AgNO3溶液中逐滴加入稀氨水,至沉淀恰好溶解,制得银氨溶液
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
利用反应2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH=-746.8kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
2CO2(g)+N2(g) ΔH=-746.8kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
A.降低温度 B.增大压强同时加催化剂
C.升高温度同时充入N2 D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 MgO、CaO等,生产工艺流程示意如下:
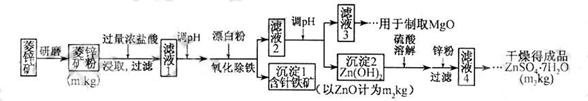
(1) 将菱锌矿研磨成粉的目的是_____。
(2) 完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3 +□CI-
(3)针铁矿(Goethite)是以德国诗人歌德(Go ethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
ethe)名字命名的,组成元素是Fe、O和H,化学式量为89,化学式是_______。
(4)根据下表数据,调节“滤液 2”的pH时,理论上可选用的最大区间为______。
2”的pH时,理论上可选用的最大区间为______。
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | — | — |
| 沉淀完全的pH | 12.4 | 8.0 | — | — |
| 开始溶解的pH | — | 10.5 | — | — |
| Ksp | 5.6× | — | 6.8× | 2.8× |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。K^S*5U.C#O%
a.大理石粉  b.石灰乳 c.纯碱溶液 d.烧碱溶液
b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3 的质量分数不低于________。
查看答案和解析>>
科目:高中化学 来源: 题型:
油酸的结构简式为CH3(CH2)7CH=CH(CH2)7COOH,下列说法正确的是
A.油酸的分子式为C18H33O2 B.油酸是乙酸的同系物
C.油酸可与氢气发生加成反应 D.1mol油酸最多可与1mol甘油酯化
查看答案和解析>>
科目:高中化学 来源: 题型:
甘蔗渣可综合利用,回答下列问题。
Ⅰ. 甘蔗渣可生成一种常见单糖A,A在乳酸菌的作用下生成有机物B,B经过缩聚反应生成可降解塑料,其结构简式为: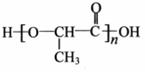
(1)A的分子式是____________;
(2)下列有关B的叙述正确的是____________(填序号);
A. B的分子式为C3H6O3 B. 1 mol B可与2 mol NaOH反应
C. 1 molB与足量的Na反应可生成1 molH2
(3)B在一定条件下可生成C,C能使溴的四氯化碳溶液褪色。B生成C的化学方程式是____________;
Ⅱ. 甘蔗渣还可生产一种重要的化工原料D,D的相对分子质量为90,1 mol D与足量NaHCO3反应放出标准状况下44.8 L CO2。
(4)D的官能团名称是____________;
(5)等物质的量的D与乙二醇在催化剂作用下可生成链状高分子化合物,其化学方程式是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
我国缺碘病区甚广,防治缺碘病的主要措施是食盐中加碘。1996年我国政府以国家标准的方式规定食盐的碘添加剂是KIO3。
(1)可用盐酸酸化的KI和淀粉的混合物检验食盐是否为加碘盐,反应的化学方程式为__________________________________
(2)可用电化学方法制备KIO3。原理是:以石墨为阳极,不锈钢为阴极,以KI溶液(加入少量K2Cr2O7)为电解质溶液,在一定电流强度和温度下进行电解,其电解总反应方程式为KI+3H2O KIO3+3H2↑。试写出两极反应式:阳极_____________;阴极_____________。
KIO3+3H2↑。试写出两极反应式:阳极_____________;阴极_____________。
(3)如果在容积为10 L的离子交换膜电解槽中,1 min时阴极可产生11.2 L(标准状况)Cl2,这时溶液的pH是(设体积维持不变)_____________。
(4)Cl2常用于自来水的消毒杀菌,现有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为_____________。
方法指引:在正确书写电解反应方程式的基础上,关键把握电解过程中的等量关系,然后进行综合处理,便可解决。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电子排布中,原子处于激发状态的是
A.1s22s2 B.1s22s22p5 C.1s22s22p63s23p63d34s2 D.1s22s12p3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com