
【题目】“84”消毒液在日常生活中使用广泛,该消毒液无色,有漂白作用。它的有效成分是下列物质中的一种,这种物质是( )
A. NaOHB. NaClOC. KMnO4D. Na2O2
 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】在一定条件下,反应N2+3H22NH3 , 在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为( )
A.v(H2)=0.03 mol/(Lmin)
B.v(N2)=0.02 mol/(Lmin)
C.v(NH3)=0.17 mol/(Lmin)
D.v(NH3)=0.01 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,反应H2(g)+I2(g)![]() 2HI(g)△H<0,在带有活塞的密闭容器中达到平衡,下列说法中不正确的是
2HI(g)△H<0,在带有活塞的密闭容器中达到平衡,下列说法中不正确的是
A. 容器体积不变,升温正、逆反应速率均增大
B. 温度、压强均不变,充入氦气,正、逆反应速率不变
C. 温度不变,压缩气体的体积,平衡不移动,颜色加深
D. 容积、温度不变,充入氦气后,正、逆反应速率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应及其应用在化学中占有重要地位。回答下列各题。
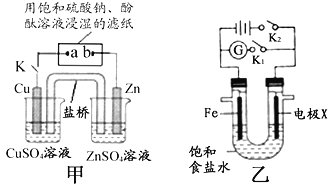
(1)写出铝与氢氧化钠溶液反应的离子方程式____________________;若将镁条、铝条和灵敏电流计用导线相连,使镁条、铝条浸入氢氧化钠溶液中,电流计指针发生偏转时,负极材料为________。
(2)当闭合K时,甲装置中Zn极的电极反应式为____;电子流动的方向为______;若盐桥中填充KCl琼脂,K+离子移动的方向为______;a极的电极反式为________;一段时间后,b极附近的现象为____________________。
(3)装置乙中。
①断开K2,接通K1。当X为石墨电极,Fe极的电极反应式为_________;当X为锌电极,Fe极的电极反应式为_____________。
②断开K1,接通K2。若X为石墨电极,X极的电极名称为_____;装置反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种三室微生物燃料电池污水净化系统原理如右图所示,图中有机废水中有机物可用C6Hl0O5表示。下列有关说法正确的是( )

A. 电解精炼铜应将粗铜连接在a电极上
B. b电极附近溶液的pH减小
C. 中间室:Na+移向左室,Cl-移向右室
D. a电极反应式C6H10O5-24e-+7H2O=6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1molL—1二元弱酸H2A溶液的pH,溶液中的H2A、HA—、A2—的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=c(x)/(c(H2A)+c(HA—)+c(A2—)])。下列叙述正确的是

A. Ka2(H2A)的数量级为10-4
B. NaHA溶液中,HA-的水解能力小于HA-的电离能力
C. 在含H2A、HA-和A2-的溶液中,加入少量NaOH固体,δ(HA-)一定增大
D. 将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中δ(HA-)=δ(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四个恒容密闭容器中按左下表相应量充入气体,发生2N2O(g) ![]() 2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如右下图所示,下列说法正确的是( )
2N2(g)+O2(g),容器I、II、III中N2O平衡转化率如右下图所示,下列说法正确的是( )
容器 | 容积/L | 起始物质的量/L |
| ||
N2O | N2 | O2 | |||
I | V1 | 0.1 | 0 | 0 | |
II | 1.0 | 0.1 | 0 | 0 | |
III | V2 | 0.1 | 0 | 0 | |
IV | 1.0 | 0.06 | 0.06 | 0.04 | |
A. 该反应的正反应放热
B. 相同温度下反应时,平均反应速率:v(I)>v(Ⅲ)
C. 图中A、B、C三点处容器内总压强:V(III)<V(II)<V(I)
D. 容器IV在470℃进行反应时,起始速率:v(N2O)正<v(N2O)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组设计实验,利用酸性KMnO4溶液与H2C2O4溶液反应,测定溶液紫色消失所需时间的方法,研究浓度对反应速率的影响。供选择的实验药品有:0.01mol·L-1酸性KMnO4溶液、0.1mol·L-1酸性KMnO4溶液、0.1mol·L-1H2C2O4溶液、0.2mol·L-1H2C2O4溶液。
(1)H2C2O4溶液与酸性KMnO4溶液反应的化学方程式为____________________________。
(2)请完成以下实验设计表。
实验 | 酸性KMnO4溶液 | H2C2O4溶液 | 褪色 时间/s | ||
c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
甲 | 0.01 | 4 | 0.1 | 2 | t1 |
乙 | a | 4 | b | 2 | t2 |
①表中a=________、b=________;
②甲组实验KMnO4的平均反应速率是:____________(用含t1的式子表示)。
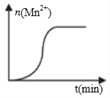
(3)测得某次实验(恒温)时,溶液中Mn2+物质的量与时间关系如图。请解释n(Mn2+)在反应起始时变化不大、一段时间后快速增大的原因:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于NaHCO3的性质,下列说法正确的是(双选)( )
A.和酸反应放出等量的CO2所消耗的酸比Na2CO3少
B.相同温度下溶解度比Na2CO3要大
C.热稳定性比Na2CO3大
D.NaHCO3只能和酸作用不能和碱作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com