
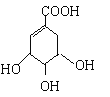
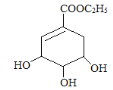
【题目】莽草酸合成治疗禽流感的药物—达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
 (提示:环丁烷
(提示:环丁烷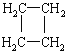 可简写成
可简写成![]() )
)
(1)A的分子式是_______________________________
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)_______________________
(3)A与乙醇反应的化学方程式(有机物用结构简式表示)是_______________________
(4)17.4g A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积(标准状况)________________
(5)A在浓硫酸作用下加热可得到B(B的结构简式为![]() ),其反应类型是_______________。
),其反应类型是_______________。
(6)苯与硝酸反应生成硝基苯的方程式_______________________
(7)蔗糖水解的方程式______________
【答案】C7H10O5 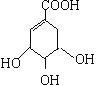 +Br2→
+Br2→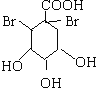
 +C2H5OH
+C2H5OH![]()
 +H2O; 2.24 L 消去反应
+H2O; 2.24 L 消去反应 ![]() ; C12H22O11 + H2O
; C12H22O11 + H2O![]() C6H12O6(葡萄糖)+C6H12O6(果糖)
C6H12O6(葡萄糖)+C6H12O6(果糖)
【解析】
(1)根据碳原子形成4个化学键及结构简式分析分子式;根据结构简式判断官能团;
(2)A中含碳碳双键,能与溴的四氯化碳溶液中溴单质发生加成反应;
(3)A中含有羧基,可与乙醇发生酯化反应;
(4)先计算出A的物质的量,再根据1 mol羧基可结合1 mol碳酸氢钠生成1 mol二氧化碳气体分析作答;
(5)根据A![]() B的结构(官能团)变化,再结合羟基可在浓硫酸加热条件下发生消去反应,分析作答;
B的结构(官能团)变化,再结合羟基可在浓硫酸加热条件下发生消去反应,分析作答;
(6)苯与浓硝酸在浓硫酸加热的条件下可发生硝化反应;
(7)蔗糖属于二糖,可在稀硫酸催化作用下发生水解反应生成葡萄糖和果糖。
(1)由碳原子形成4个化学键及结构简式可知,该有机物的分子式为C7H10O5,
故答案为:C7H10O5;
(2)A与溴的四氯化碳溶液发生加成反应,其化学方程式为: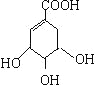 +Br2→
+Br2→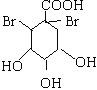 ,
,
故答案为: +Br2→
+Br2→ ;
;
(3)A中含COOH,与乙醇发生酯化反应,其化学方程式为:  +C2H5OH
+C2H5OH![]()
 +H2O,
+H2O,
故答案为: +C2H5OH
+C2H5OH![]()
 +H2O;
+H2O;
(4)A和NaHCO3发生的反应可以表示为: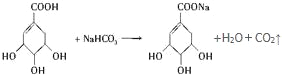 ,生成二氧化碳的体积为
,生成二氧化碳的体积为![]() ×22.4L/mol = 2.24 L,
×22.4L/mol = 2.24 L,
故答案为:2.24 L;
(5) 在浓硫酸加热条件下,可发生羟基的消去反应,生成
在浓硫酸加热条件下,可发生羟基的消去反应,生成![]() ,
,
故答案为:消去反应;
(6)苯和浓硝酸、浓硫酸在50℃~60℃发生取代反应生成硝基苯和水,该反应方程式为:![]() ,
,
故答案为:![]() ;
;
(7)C12H22O11 + H2O![]() C6H12O6(葡萄糖)+C6H12O6(果糖)
C6H12O6(葡萄糖)+C6H12O6(果糖)


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】已知实验室制氯气的化学方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,现用足量浓盐酸与8.7 g二氧化锰完全反应制取氯气(假设Cl2全部逸出)。求:
MnCl2+Cl2↑+2H2O,现用足量浓盐酸与8.7 g二氧化锰完全反应制取氯气(假设Cl2全部逸出)。求:
(1)产生多少升氯气(标准状况)?____________________
(2)把产生的氯气通入足量NaOH溶液中,假设氯气全部参加反应,可产生多少mol NaClO?____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证同主族元素性质的递变规律。某小组用如图所示的装置进行实验(夹持仪器已略去,装置气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当装置B和装置C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当装置B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
(1)浸有NaOH溶液的棉花的作用____________________________。
(2)装置A中发生的置换反应的化学方程式为___________________。
(3)装置B的溶液中NaBr完全被氧化,则消耗Cl2的物质的量为__________。
(4)为验证溴元素的非金属性强于碘元素,过程Ⅳ的操作和现象是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧生成CO2和H2O。将12.4 g该有机物的完全燃烧产物通过浓硫酸,浓硫酸增重10.8 g,再通过碱石灰,碱石灰增重了17.6 g。下列说法不正确的是
A. 该有机物的最简式为CH3O
B. 该有机物的分子式可能为CH3O
C. 该有机物的分子式一定为C2H6O2
D. 该有机物可能属于醇类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡酸钠可用于制造陶瓷电容器的基体、颜料和催化剂。以锡锑渣(主要含Sn、Sb、As、Pb的氧化物)为原料,制备锡酸钠的工艺流程图如下图所示:

请回答下列问題:
(1)Sn(IVA)、As(VA)、Sb(VA)三种元素中,Sn的原子序数为50,其原子结构示意图为_____,碱浸”时SnO2发生反应的化学方程式为___________________________。
(2)“碱浸”时,若Sn元素氧化物中SnO含量较高,工业上则加入NaNO3,其作用是_______。
(3)从溶液中得到锡酸钠晶体的实验操作是_________、趁热过滤、洗涤、干燥。下图是“碱浸”实验的参数,请选择“碱浸”的合适条件_______。
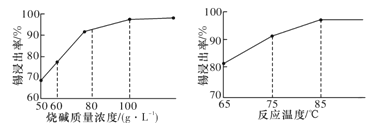
(4)“脱铅”是从含Na2PbO2的溶液中形成硫化铅渣,其离子方程式为_________________。
(5)“脱锑”时Na2SbO4发生的化学方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中溴含量约为 65 mg·L-1,从海水中提取溴的工艺流程如下:

(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是____________。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的____。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面方框内填入适当的化学计量数:_____![]()
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是____。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用。不仅可以提高经济效益,而且还能防止环境污染,生产流程如下:

已知石油裂解已成为生产C的主要方法,E的溶液能发生银镜反应,G是具有果香味的液体,试填空:
(1) B的名称:_________________;D中官能团的名称:___________________。
(2) 写出C发生加聚反应的方程式:___________________。
(3) D→E的化学方程式:_____________________;F→G的化学方程式:_____________________。
(4)已知HCOOCH3也具有果香味,则该物质与G的关系互称为_________________,与F的关系互称为:_________________。
下图为实验室制取G的装置图,图中a试剂名称为________________,实验结束后分离a和G的方法为_________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
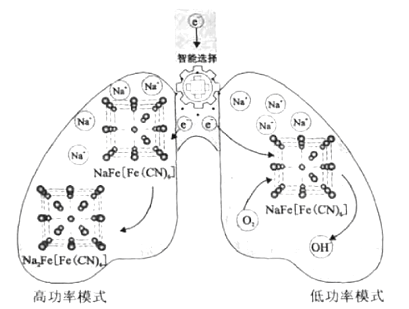
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,22.4LCO2中所含的分子数为NA
B.标准状况下,3.6gH2O所占的体积为4.48L
C.常温常压下,28gN2中所含氮原子数为2NA
D.2.4g金属镁变为镁离子时,失去的电子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com