
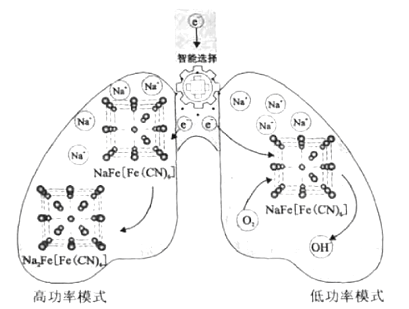
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
【答案】D
【解析】
A.根据图示可知:电池以低功率模式工作时,负极是Zn-2e-=Zn2+,正极上是NaFe[Fe(CN)6]获得电子,然后与吸附在它上面的氧气即溶液中发生反应为O2+4e-+2H2O=4OH-,从NaFe[Fe(CN)6]上析出,故NaFe[Fe(CN)6]的作用是作催化剂,A正确;
B.电池以低功率模式工作时,电子进入NaFe[Fe(CN)6]时Na+的嵌入;当形成OH-从NaFe[Fe(CN)6]析出时,Na+从NaFe[Fe(CN)6]脱嵌,因此Na+的嵌入与脱嵌同时进行,B正确;
C.根据电池以高功率模式工作时,正极上NaFe[Fe(CN)6]获得电子被还原变为Na2Fe[Fe(CN)6],所以正极的电极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6],C正确;
D.若在无溶解氧的海水中,由于在低功率模式工作时需要氧气参与反应,因此在该电池不能实现长续航的需求,D错误;
故合理选项是D。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】已知常温下Ksp(AgCl)=1.6×10-10、Ksp(AgI)=2.0×10-16,下列说法中正确的是
A.含有大量Cl-的溶液中肯定不存在Ag+
B.AgI悬浊液中加入少量KI粉末,平衡AgI(s)![]() Ag+(aq)+I-(aq)向左移动,溶液中离子的总浓度会减小
Ag+(aq)+I-(aq)向左移动,溶液中离子的总浓度会减小
C.AgCl悬浊液中逐渐加入KI固体至c(I-)=Ksp(AgI)/Ksp(AgCl)mol·L-1时,AgCl开始向AgI沉淀转化
D.向浓度均为0.01 mol·L-1的KCl和KI的混合溶液中滴加AgNO3溶液,当Cl-开始沉淀时,溶液中I-的浓度为1.25×10-8 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
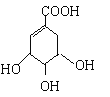
【题目】莽草酸合成治疗禽流感的药物—达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
 (提示:环丁烷
(提示:环丁烷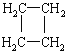 可简写成
可简写成![]() )
)
(1)A的分子式是_______________________________
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)_______________________
(3)A与乙醇反应的化学方程式(有机物用结构简式表示)是_______________________
(4)17.4g A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积(标准状况)________________
(5)A在浓硫酸作用下加热可得到B(B的结构简式为![]() ),其反应类型是_______________。
),其反应类型是_______________。
(6)苯与硝酸反应生成硝基苯的方程式_______________________
(7)蔗糖水解的方程式______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图两种化合物的结构或性质描述正确的是
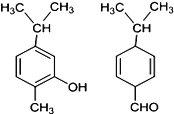
A. 两种化合物均是芳香烃
B. 两种化合物可用红外光谱区分,但不能用核磁共振氢谱区分
C. 两种化合物分子中共平面的碳原子数相同
D. 两种化合物互为同分异构体,均能与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电-Fenton法是用于水体中有机污染物降解的高级氧化技术,其反应原理如图所示。其中电解产生的H2O2与Fe2+发生Fenton反应:H2O2+Fe2+=Fe3++OH-+·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法中正确的是

A.电源的X极为正极,Y极为负极
B.阴极的电极反应式为Fe2+-e-=Fe3+
C.阳极的电极反应式为H2O-e-=H++·OH
D.每消耗1molO2,整个电解池中理论上可产生2mol·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知制备胶体的反应原理为: FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl,现有甲、乙、丙三名同学分别进行制备Fe(OH)3胶体的实验
Fe(OH)3(胶体)+3HCl,现有甲、乙、丙三名同学分别进行制备Fe(OH)3胶体的实验
Ⅰ、甲同学直接加热饱和FeCl3溶液;
Ⅱ、乙同学向25 mL沸水中逐滴加入FeCl3饱和溶液;煮沸至液体呈红褐色,停止加热
Ⅲ、丙同学和乙同学一样,但是溶液出现红褐色后忘记停止,继续加热较长时间。
试回答下列问题:
(1)判断胶体制备是否成功,可利用胶体的__________________________,其中操作方法及现象是_____________________________________。
(2)Fe(OH)3胶体是不是电解质:_______________(填“是”或“不是”)。
(3)丁同学检查实验结果发现___________(填甲、乙或丙)的烧杯底部有沉淀。
(4)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①取部分胶体将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶体的胶粒带___________电荷。
②取部分胶体向其中逐滴滴加硫酸溶液,开始产生红褐色沉淀,这是因为_________;继续滴加,沉淀减少最终消失,写出化学反应方程式__________________。
③欲除去Fe(OH)3胶体中混有的NaCl溶液的操作名称是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol/LAlCl3溶液中,含![]() 数目小于
数目小于![]()
B. 25℃,![]() pH=1的稀硫酸中含有的
pH=1的稀硫酸中含有的![]() 数为
数为![]()
C. 标准状况下,![]()
![]() 和
和![]() 混合气体中含
混合气体中含![]() 个原子
个原子
D. 由![]()
![]() 和少量
和少量![]() 形成的中性溶液中,CH3COO-数目为
形成的中性溶液中,CH3COO-数目为![]() 个
个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用两支惰性电极插入50mLAgNO3溶液中,通电电解。当电解液的PH值从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),电极上析出银的质量大约是:
A. 27mg B. 54mg C. 108mg D. 216mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是一种抗脑缺血药物,合成路线如下:
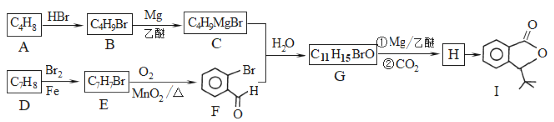
已知:
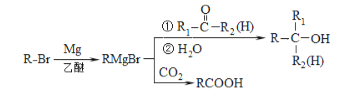
回答下列问题:
(1)按照系统命名法,A的名称是_____;写出A发生加聚反应的化学方程式:__________。
(2)反应H→I的化学方程式为________;反应E→F的反应类型是______。
(3)写出符合下列条件的G的所有同分异构体的结构简式:________
①遇FeCl3溶液发生显色反应 ②核磁共振氢谱有4组峰
(4)α,α-二甲基苄醇(![]() )是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:
)是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:

该合成路线中X的结构简式为____,Y的结构简式为________;试剂与条件2为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com