
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,22.4LCO2中所含的分子数为NA
B.标准状况下,3.6gH2O所占的体积为4.48L
C.常温常压下,28gN2中所含氮原子数为2NA
D.2.4g金属镁变为镁离子时,失去的电子数为0.1NA
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】莽草酸合成治疗禽流感的药物—达菲(Tamiflu)的原料之一。莽草酸是A的一种异构体。A的结构简式如下:
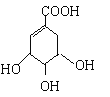 (提示:环丁烷
(提示:环丁烷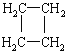 可简写成
可简写成![]() )
)
(1)A的分子式是_______________________________
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)_______________________
(3)A与乙醇反应的化学方程式(有机物用结构简式表示)是_______________________
(4)17.4g A与足量碳酸氢钠溶液反应,计算生成二氧化碳的体积(标准状况)________________
(5)A在浓硫酸作用下加热可得到B(B的结构简式为![]() ),其反应类型是_______________。
),其反应类型是_______________。
(6)苯与硝酸反应生成硝基苯的方程式_______________________
(7)蔗糖水解的方程式______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol/LAlCl3溶液中,含![]() 数目小于
数目小于![]()
B. 25℃,![]() pH=1的稀硫酸中含有的
pH=1的稀硫酸中含有的![]() 数为
数为![]()
C. 标准状况下,![]()
![]() 和
和![]() 混合气体中含
混合气体中含![]() 个原子
个原子
D. 由![]()
![]() 和少量
和少量![]() 形成的中性溶液中,CH3COO-数目为
形成的中性溶液中,CH3COO-数目为![]() 个
个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用两支惰性电极插入50mLAgNO3溶液中,通电电解。当电解液的PH值从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),电极上析出银的质量大约是:
A. 27mg B. 54mg C. 108mg D. 216mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按下图所示的装置进行实验。![]() 、
、![]() 为两种常见金属,它们的硫酸盐可溶于水,当
为两种常见金属,它们的硫酸盐可溶于水,当![]() 闭合时,
闭合时,![]() 从右向左通过交换膜移向
从右向左通过交换膜移向![]() 极。下列分析不正确的是
极。下列分析不正确的是

A. 溶液中![]() 增大
增大
B. ![]() 极的电极反应:
极的电极反应:![]()
C. ![]() 电极上有
电极上有![]() 产生,发生氧化反应
产生,发生氧化反应
D. 反应初期,![]() 电极周围出现白色胶状沉淀
电极周围出现白色胶状沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的三个烧杯中均盛有足量的氯化铜溶液。请按要求回答下列问题:
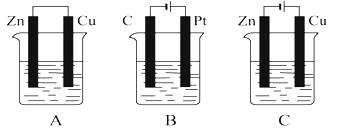
(1)![]() 、
、![]() 、
、![]() 三个装置中不属于电解池的是______。
三个装置中不属于电解池的是______。
(2)![]() 池中
池中![]() 是______极,
是______极,![]() 池中
池中![]() 移向______极(填“
移向______极(填“![]() ”或“
”或“![]() ”)。
”)。
(3)![]() 池中
池中![]() 电极上发生反应__________(填“氧化”或“还原”)
电极上发生反应__________(填“氧化”或“还原”)
(4)![]() 池中
池中![]() 电极上的电极反应为______,反应过程中
电极上的电极反应为______,反应过程中![]() ______(填“变大”“变小”或“不变”)
______(填“变大”“变小”或“不变”)
(5)![]() 池中总反应的化学方程式为______
池中总反应的化学方程式为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用湿法冶金工艺回收废旧光盘中的金属Ag(其他金属因微量忽略不计),其流程如下:
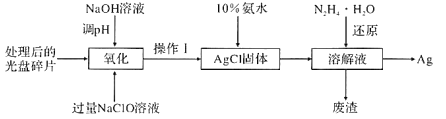
回答下列问题:
(1)①“操作I”为_____,在实验室进行此操作需要用到的玻璃仪器有_____。
②在实验室利用“操作I”的装置洗涤难溶物的操作方法是_______。
(2)若NaClO溶液与Ag反应的产物有AgCl和O2,则该反应的化学方程式为____若以稀HNO3代替NaClO溶液,其缺点是___(写出一条即可)。
(3)已知Ag2O在酸性条件下能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上 述过程设计为一种电化学装置,以回收电极材料中的金属Ag。则此电池的正极反应式为_____。
(4)已知室温时,Ksp(Ag2SO4)=1.4×10-5,Ksp(AgCl)=1.8×10-10。计算反应Ag2SO4(s)+2Cl-(aq) ![]() 2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是一种抗脑缺血药物,合成路线如下:
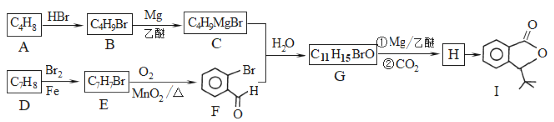
已知:
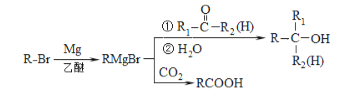
回答下列问题:
(1)按照系统命名法,A的名称是_____;写出A发生加聚反应的化学方程式:__________。
(2)反应H→I的化学方程式为________;反应E→F的反应类型是______。
(3)写出符合下列条件的G的所有同分异构体的结构简式:________
①遇FeCl3溶液发生显色反应 ②核磁共振氢谱有4组峰
(4)α,α-二甲基苄醇(![]() )是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:
)是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:

该合成路线中X的结构简式为____,Y的结构简式为________;试剂与条件2为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水凝胶材料要求具有较高的含水率,以提高其透氧性能,在生物医学上有广泛应用。由N-乙烯基吡咯烷酮(NVP)和甲基丙烯酸![]() -羟乙酯(HEMA)合成水凝胶材料高聚物A的路线如图:
-羟乙酯(HEMA)合成水凝胶材料高聚物A的路线如图:
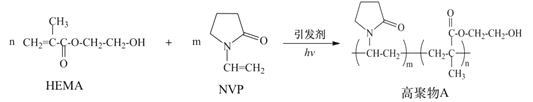
下列说法正确的是
A. NVP具有顺反异构
B. 高聚物A因含有-OH而具有良好的亲水性
C. HEMA和NVP通过缩聚反应生成高聚物A
D. 制备过程中引发剂浓度对含水率影响关系如图,聚合过程中引发剂的浓度越高越好

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com