
【题目】采用湿法冶金工艺回收废旧光盘中的金属Ag(其他金属因微量忽略不计),其流程如下:
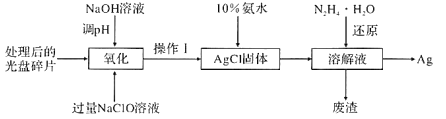
回答下列问题:
(1)①“操作I”为_____,在实验室进行此操作需要用到的玻璃仪器有_____。
②在实验室利用“操作I”的装置洗涤难溶物的操作方法是_______。
(2)若NaClO溶液与Ag反应的产物有AgCl和O2,则该反应的化学方程式为____若以稀HNO3代替NaClO溶液,其缺点是___(写出一条即可)。
(3)已知Ag2O在酸性条件下能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上 述过程设计为一种电化学装置,以回收电极材料中的金属Ag。则此电池的正极反应式为_____。
(4)已知室温时,Ksp(Ag2SO4)=1.4×10-5,Ksp(AgCl)=1.8×10-10。计算反应Ag2SO4(s)+2Cl-(aq) ![]() 2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
2AgCl(s)+SO42- (aq)的平衡常数K=_____。(保留两位有效数字)
【答案】过滤 烧杯、漏斗、玻璃棒 向过滤器内加蒸馏水浸没沉淀,使水自然流下,重复 2~3 次 4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2↑ 没有 Cl-不能生成 AgCl(或生成氮氧化物,污染空气) Ag2O + 2e- + 2H+ = 2Ag + H2O 4.3×1014
【解析】
(1)①“操作I”得到溶液和固体,故为过滤;在实验室进行此操作需要用到的玻璃仪器有烧杯、漏斗、玻璃棒;
②在实验室利用“操作I”的装置洗涤难溶物的操作方法是向过滤器内加蒸馏水浸没沉淀,使水自然流下,重复 2~3 次;
(2)若NaClO溶液与Ag反应的产物有AgCl和O2,银元素和氧元素化合价升高,则氯元素化合价降低,根据氧化还原反应进行配平得反应的化学方程式为4Ag+ 4NaClO + 2H2O = 4AgCl + 4NaOH + O2↑;
若以稀HNO3代替NaClO溶液,其缺点是没有 Cl-不能生成 AgCl、生成氮氧化物,污染空气;
(3)已知Ag2O在酸性条件下能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上 述过程设计为一种电化学装置,以回收电极材料中的金属Ag。则此电池的正极氧化银得电子产生银,电极反应式为Ag2O + 2e- + 2H+ = 2Ag + H2O;
(4)已知室温时,Ksp(Ag2SO4)=1.4×10-5,Ksp(AgCl)=1.8×10-10。计算反应Ag2SO4(s)+2Cl-(aq) ![]() 2AgCl(s)+ SO42- (aq)的平衡常数K=
2AgCl(s)+ SO42- (aq)的平衡常数K=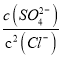 =
= =
= =
= =4.3×1014。
=4.3×1014。


科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用。不仅可以提高经济效益,而且还能防止环境污染,生产流程如下:

已知石油裂解已成为生产C的主要方法,E的溶液能发生银镜反应,G是具有果香味的液体,试填空:
(1) B的名称:_________________;D中官能团的名称:___________________。
(2) 写出C发生加聚反应的方程式:___________________。
(3) D→E的化学方程式:_____________________;F→G的化学方程式:_____________________。
(4)已知HCOOCH3也具有果香味,则该物质与G的关系互称为_________________,与F的关系互称为:_________________。
下图为实验室制取G的装置图,图中a试剂名称为________________,实验结束后分离a和G的方法为_________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列有关说法正确的是
A. 常温常压下,31 g P4中含P-P键的数目为NA
B. 常温常压下,46 g NO2与92 g N2O4所含的分子数相同
C. 一定条件下,6.4 g铜粉与过量的硫粉充分反应,转移电子数为0.2 NA
D. 标准状况下,将22.4 L Cl2 通入足量NaOH溶液中,转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,22.4LCO2中所含的分子数为NA
B.标准状况下,3.6gH2O所占的体积为4.48L
C.常温常压下,28gN2中所含氮原子数为2NA
D.2.4g金属镁变为镁离子时,失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述
中,正确的是

A.常压下五种元素的单质中,Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.气态氢化物的稳定性W的比X的强
D.Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将等浓度的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是( )

A. a点时,溶液中由水电离的c(OH-)约为1×10-10 mol·L-1
B. 电离平衡常数:Ka(HA)< Ka(HB)
C. b点时,c(B-)=c(HB)>c(Na+)>c(H+)>c(OH-)
D. 向HB溶液中滴加NaOH溶液至pH=7时:c(B-)> c(HB)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某温度下,在2L密闭容器中X、Y、Z三种物质(均为气态)间进行反应,其物质的量随时间的变化曲线如图。依图回答:

(1)该反应的化学方程式可表示为____________。
(2)反应起始至t min(设t=5),Y的平均反应速率是________。
(3)在t min时,该反应达到了平衡状态,下列可判断反应已达到该状态的是________(选填字母)。
a.X、Y、Z的反应速率相等
b.X、Y的反应速率比为2:3
c.混合气体的密度不变
d.生成1mol Z的同时生成2mol X
e.X、Y、Z物质的量之比等于化学计量数比
f.混合气体的总压强不再发生改变
II.燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液。完成下列关于甲烷(CH4)燃料电池的填空:
(1)已知燃料电池的总反应式为CH4+2O2+2KOH==K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH--8e-== CO32-+7H2O,这个电极是燃料电池的______(填“正极”或“负极”),另一个电极上的电极反应式为:____________________。
(2)随着电池不断放电,电解质溶液的碱性__________(填“增强”、“减弱”或“不变”)。
(3)通常情况下,甲烷燃料电池的能量利用率_________(填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图填空:

(1)反应物是______________,生成物是______________。
(2)在2 min内用A、B、C表示的化学反应速率分别为____________、____________、____________。
(3)该反应的化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
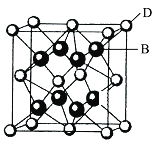
【题目】已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1~18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物,其晶胞结构如图。
请回答:
(1)A元素的名称是______。
(2)B的元素符号是__________,C的元素符号是______。
(3)E属元素周期表中第________周期第______族的元素,其元素名称是______,它的+2价离子的电子排布式为________。
(4)从图中可以看出,D跟B形成的离子化合物的化学式为______;该离子化合物晶体的密度为a g·cm-3,则晶胞的体积是______(只要求列出算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com