
【题目】氮、磷、砷、硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。回答下列问题:
(1)基态As原子的电子排布式为__________。N、P、As的第一电离能的大小顺序为 _______。
(2)氮化硼(BN)有多种晶体,其中立方氮化硼与金刚石的构型类似,则其晶胞中B-N-B之间的夹角是_________(填角度)。
(3)砷化硼(BAs)是Ⅲ-V族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与_____个B相连,As的杂化形式为______;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有_______(填字母)。
A.离子键 B. 金属键 C.极性键 D.氢键 E.配位键F.![]() 键G.
键G. ![]() 键
键
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,这种陶瓷材料可作为金属表面的保护薄膜,它是通过在高温(T>750℃)氢气氛围下BBr3和PBr3反应制得的,BBr3的空间构型为______,BP晶胞的结构如图所示,当晶胞晶格参数为478pm(即图中立方体的每条边长为478pm)时,BP中B和P之间的最近距离为_____。
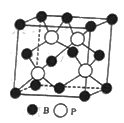
【答案】 1s22s22p63s23p63d104s24p3 N>P>As 109°28′ 4 sp3杂化 CEF 平面三角形 119.5![]() pm
pm
【解析】(1)As是33号元素,其核外电子排布为,1s22s22p63s23p63d104s24p3;非金属性越强,第一电离能越大,N>P>As;(2)立方氮化硼与金刚石的构型类似,金刚石为正四面体结构,键角为109°28′,则其晶胞中B﹣N﹣B之间的夹角是109°28′;(3)①砷化硼(BAs)晶体结构与金刚石相似,为正四面体结构,则每个As与4个B相连,BAs的电子对有![]() =4对,中心原子As的杂化形式为sp3杂化;②硼原子可以形成3个硼硼单键,所以每个As应与3个B相连,金刚石中含有的化学键是共价键,所以该物质中含有的化学键是极性键,单键为
=4对,中心原子As的杂化形式为sp3杂化;②硼原子可以形成3个硼硼单键,所以每个As应与3个B相连,金刚石中含有的化学键是共价键,所以该物质中含有的化学键是极性键,单键为![]() 键,又因为砷原子还有1对孤对电子,而硼原子有容纳孤对电子的空轨道,所以还可以构成配位键。答案选CEF;(4)B原子含有3个价电子,与3个Br原子形成σ键,空间构型为平面三角形;根据BP的晶胞示意图可知硼原子和磷原子之间的最近距离等于晶胞体对角线的
键,又因为砷原子还有1对孤对电子,而硼原子有容纳孤对电子的空轨道,所以还可以构成配位键。答案选CEF;(4)B原子含有3个价电子,与3个Br原子形成σ键,空间构型为平面三角形;根据BP的晶胞示意图可知硼原子和磷原子之间的最近距离等于晶胞体对角线的![]() ,设最近距离为x,则(4x)2=4782+4782+4782,解得x=
,设最近距离为x,则(4x)2=4782+4782+4782,解得x=![]() pm=119.5
pm=119.5![]() pm。
pm。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】烯烃的甲酰化反应实例之一是CH3CH=CH2与CO、H2在催化剂作用下可合成正丁醛(CH3 CH2 CH2 CHO),有关反应如下:
①CH3CH=CH2(g)+CO (g)+H2(g)![]() CH3CH2CH2CHO(g) ΔH1
CH3CH2CH2CHO(g) ΔH1
副反应有:
②CH3CH=CH2(g)+ CO (g)+ H2(g)![]() (CH3)2CHCHO(g) ΔH2
(CH3)2CHCHO(g) ΔH2
③CH3CH=CH2(g)+ H2(g) → CH3 CH2 CH3(g) ΔH3
回答下列问题:
(1)不考虑副反应,则从绿色化学角度考虑,烯烃甲酰化反应的主要优点是_______________________________。
(2)已知下列键能数据:
化学键 | C-H | C-C | C=C | H-H |
键能/KJ·mol-1 | 413.3 | 347.7 | 615.0 | 436.0 |
则反应CH3CH=CH2(g)+ H2(g) → CH3 CH2 CH3(g)的ΔH3=_______________。
(3)在恒容密闭容器中充入1 mol丙烯,加入某种催化剂在加热条件下进行反应,测得温度与丙烯的总平衡转化率及两种异构体的物质的量之比的关系如下图所示:
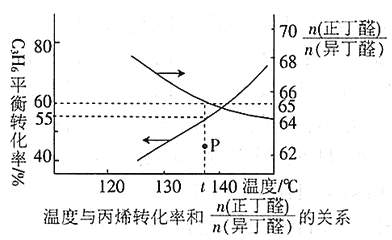
①丙烯合成正丁醛(CH3 CH2 CH2 CHO)及异丁醛((CH3)2CHCHO)的反应属于______________(填“吸热”或“放热”)反应。
②t℃时,反应(CH3)2CHCHO(g)![]() CH3 CH2 CH2 CHO(g)的平衡常数K =____________________,若发生上述反应①②,则反应达到平衡时,容器中正丁醛的物质的量为_______。
CH3 CH2 CH2 CHO(g)的平衡常数K =____________________,若发生上述反应①②,则反应达到平衡时,容器中正丁醛的物质的量为_______。
③t℃时,图中P点的反应速率v(正)_______v(逆)(填“<” “>”或“=”)。
④要提高正丁醛的产率除采用合适的温度外,还可_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组对物质的性质进行相关探究. 【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验: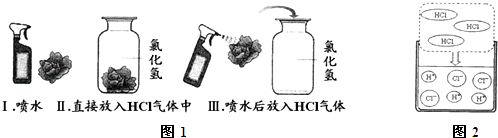
实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的微观示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是 .
(2)小明向实验Ⅲ中变红的小花上喷适当过量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式 .
(3)紫甘蓝的汁液在酸性溶液中显色,在碱性溶液中显色.
(4)下列实验可以用来说明氯化氢气体不显酸性的是 .
A.测试盐酸的导电性,盐酸能导电
B.干燥的碳酸钠粉末放人氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体
D.干燥的碳酸钠粉末放人盐酸中,能反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某条件下,合成氨反应的数据如下:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
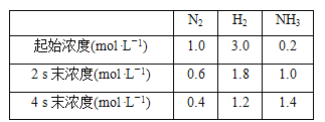
当用氨气浓度的增加来表示该反应的化学反应速率时,下列说法错误的是( )
A. 2~4 s内的平均反应速率为0.2 mol·L-1·s-1
B. 前4 s内的平均反应速率为0.3 mol·L-1·s-1
C. 前2 s内的平均反应速率为0.4 mol·L-1·s-1
D. 2 s末的反应速率为0.4 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的分子式为C10H803能与NaHCO3反应,在一定条件下存在如下转化关系:
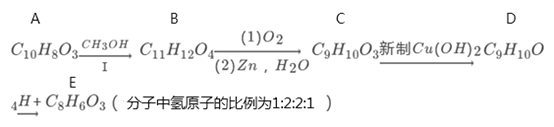
已知:
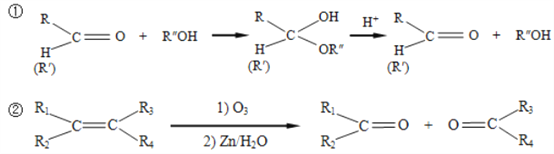
请回答下列问题:
(1)有机物A的结构简式为:___________。
(2)有机物B中含氧官能团的名称是:___________。
(3)反应I的作用为:___________。
(4)写出C→D的化学方程式:___________。
(5)F(C8H8O3)是由E与氢气在一定条件下反应得到的。F在一定条件下可以形成高分子,请写出该反应的化学方程式:_____________。
(6)E有多种同分异构体,其中满足下列条件的同分异构体共有______种(已知碳碳三键、碳碳双键与羟基相连不稳定)。
A.除苯环外无其他环且无一O—O—键
B.能与FeCl3溶液发生显色反应
C.苯环上一氯代物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
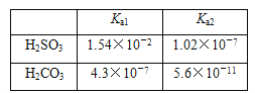
(1)在相同浓度的H2SO3和H2CO3的溶液中,用“>”“<”或“=”填空。
c(H+):H2SO3________H2CO3;c(SO![]() )________c(CO
)________c(CO![]() );c(H2SO3)________c(H2CO3);溶液导电能力:H2SO3________H2CO3。
);c(H2SO3)________c(H2CO3);溶液导电能力:H2SO3________H2CO3。
(2)HSO![]() 的电离平衡常数表达式为________________。
的电离平衡常数表达式为________________。
(3)H2SO3溶液与NaHCO3溶液反应的主要离子方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32、SO42、NO3中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是
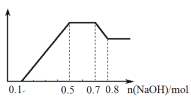
A.溶液中一定不含CO32,可能含有SO42和NO3
B.溶液中n(NH4+)=0.2mol
C.溶液中的阳离子只有H+、Mg2+、Al3+
D.n(H+)∶n(Al3+)∶n(Mg2+) = 1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X,Y,Z,E,F五种常见物质含有同一元素M,在一定条件下它们有如图转化关系,Z是NO,下列推断不合理的是( ) 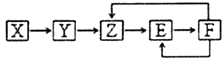
A.X可能是一种氢化物
B.X生成Z一定是化合反应
C.E可能是一种有色气体
D.F中M元素的化合价可能为+5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com