
��֪ͼ�١��ܵ������Ϣ��������Ӧ������ȷ���� �� ��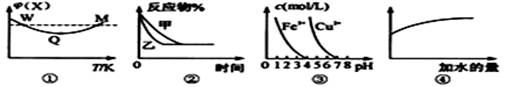
A��ͼ�ٱ�ʾ������ܱ������г���X��Y������Ӧ��2X(g)+Y(g)  3Z(g) ��H��0��W��X������Ӧ���ʵ���M��X������Ӧ���� 3Z(g) ��H��0��W��X������Ӧ���ʵ���M��X������Ӧ���� |
B��ͼ�ڱ�ʾѹǿ�Կ��淴ӦA(g)+2B(g) 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿС 3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿС |
| C����ͼ�ۣ���Ҫ��ȥCuSO4��Һ�е�Fe3+���ɼ���NaOH��Һ��PH��4���� |
| D�������£�ϡ��0.1mol/LNa2CO3��Һ��ͼ���е�������ɱ�ʾ��Һ��HCO3-����Ŀ |
D
�������������A��ͼ�ٱ�ʾW��X�ĺ�������M��X�ĺ�����ͬ�����Ƿ�Ӧ���ʲ�һ����ͬ������B.���ڸ÷�Ӧ�Ƿ�Ӧǰ�����������ȵķ�Ӧ������ƽ��ʱ��Ӧ��ĺ�����ͬ�������ȴﵽƽ�⣬���ͼ��Ҳ���Ա�ʾ�����Կ��淴ӦA(g)+2B(g) 3C(g)+D(s)��Ӱ�죬��ʹ���˴���������û��ʹ�ô���������C����ͼ�ۣ���Ҫ��ȥCuSO4��Һ�е�Fe3+���ɼ���CuO��CuCO3��PH��4���ҡ�����D����Na2CO3��ǿ�������Σ�ˮ�����HCO3-���ӡ���ҺԽϡ��ˮ��̶�Խ������HCO3-����ĿԽ�ࡣ��˸�ͼ��ɱ�ʾ�����£�ϡ��0.1mol/LNa2CO3��Һ��ͼ���е�������ɱ�ʾ��Һ��HCO3-����Ŀ����ȷ��
3C(g)+D(s)��Ӱ�죬��ʹ���˴���������û��ʹ�ô���������C����ͼ�ۣ���Ҫ��ȥCuSO4��Һ�е�Fe3+���ɼ���CuO��CuCO3��PH��4���ҡ�����D����Na2CO3��ǿ�������Σ�ˮ�����HCO3-���ӡ���ҺԽϡ��ˮ��̶�Խ������HCO3-����ĿԽ�ࡣ��˸�ͼ��ɱ�ʾ�����£�ϡ��0.1mol/LNa2CO3��Һ��ͼ���е�������ɱ�ʾ��Һ��HCO3-����Ŀ����ȷ��
���㣺����ͼ���ڱ�ʾ��ѧ��Ӧ���ʡ���ѧƽ�⡢��ȥ���ʡ��ε�ˮ���е�Ӧ�õ�֪ʶ��


 ��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ��ټ��ִ�ѧ������ϵ�д� �����������Ż�ѧϰϵ�д�
�����������Ż�ѧϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ڷ�ӦA (g)+ 3B(g) =" 2C(g)" + 2D(g)���������ݱ�ʾ��Ӧ���е�������( )
A��v(A)=0��7mol/(L��s) B��v (B) =1��8mol/(L �� s)
C��v (C)=1mol/(L��s) D��v (D) =1��6mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪298 Kʱ���ϳɰ���ӦN2(g)��3H2(g)  2NH3(g)����H����92��0 kJ��mol��1�������¶��µ�1 mol N2��3 mol H2����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ(�ٶ�����������û��������ʧ)
2NH3(g)����H����92��0 kJ��mol��1�������¶��µ�1 mol N2��3 mol H2����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ(�ٶ�����������û��������ʧ)
| A��һ��С��92��0 kJ | B��һ������92��0 kJ |
| C��һ������92��0 kJ | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ػ�ѧ֪ʶ�����жϣ����н��۴������
| A��ij���ȷ�Ӧ���Է����У���˸÷�Ӧ��������Ӧ |
| B��NH4Fˮ��Һ�к���HF�����NH4F��Һ���ܴ���ڲ����Լ�ƿ�� |
| C����ȼ����Ҫ������ˮ�ڵ��¸�ѹ���γɵ�ˮ���ᄃ�壬��˿ɴ����ں��� |
| D������Ӧ��Ũ�ȿɼӿ췴Ӧ���ʣ������Ũ����������Ӧ����������H2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��C(s)��CO2(g) 2CO(g)��Ӧ�п�ʹ��Ӧ��������Ĵ�ʩ��
2CO(g)��Ӧ�п�ʹ��Ӧ��������Ĵ�ʩ��
�ټ�С�������ʹ����ѹǿ�� ������̼������ �ۺ���ʱͨ��CO2��
�ܺ�ѹ�³���N2�� �ݺ����³���N2��
| A���٢ۢݡ��� | B���ڢ� | C���٢� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ijʵ��С�����ݷ�Ӧ �����ͼԭ��أ�̽��pH��AsO43-�����Ե�Ӱ�졣��õ�ѹ��pH�Ĺ�ϵ��ͼ�������й������������
�����ͼԭ��أ�̽��pH��AsO43-�����Ե�Ӱ�졣��õ�ѹ��pH�Ĺ�ϵ��ͼ�������й������������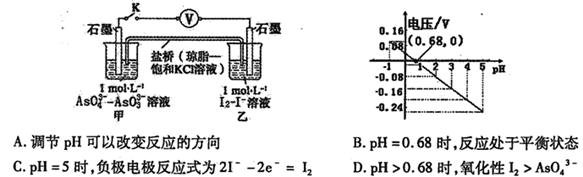
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
1000��ʱ��FeO(s) + H2 Fe(s) + H2O��K��0.52����ʹ��������1.0 mol FeO����ԭ����Ӧǰ������Ӧ����a mol H2����a��ӽ�
Fe(s) + H2O��K��0.52����ʹ��������1.0 mol FeO����ԭ����Ӧǰ������Ӧ����a mol H2����a��ӽ�
| A��1.0 | B��2.0 | C��3.0 | D��4.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����dz��ȵ�λ��1������1��10-9�ף����ʵĿ����ﵽ����ʱ��������������ʡ����罫����ͭ�Ƴɡ�����ͭ��ʱ�����зdz�ǿ�Ļ�ѧ���ԣ��ڿ����п���ȼ�ա����жԡ�����ͭ�� ���й�������ȷ���ǣ� ��
| A�������¡�����ͭ����ͭƬ�Ļ�ԭ��ǿ����Ӧʱ��Ӧ���ʿ� |
| B��������ͭ��������ϸС����ѧ��Ӧʱ�Ӵ�������Է�Ӧ���ʿ� |
| C��������ͭ����ͭ��ͬ�������� |
| D�������¡�����ͭ����ͭƬ���õ��ӣ���Ӧʱ��Ӧ���ʿ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���淴Ӧ��2NO2(g) 2NO(g)��O2(g)������̶����ܱ������н��У��ﵽƽ��״̬�ı�־����(����)
2NO(g)��O2(g)������̶����ܱ������н��У��ﵽƽ��״̬�ı�־����(����)
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2
�ڵ�λʱ��������n mol O2��ͬʱ����2n mol NO
����NO2��NO��O2��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�ܻ���������ɫ���ٸı��״̬
�ݻ��������ܶȲ��ٸı��״̬
��������ѹǿ���ٸı��״̬
��������ƽ����Է����������ٸı��״̬
| A���٢ܢޢ� | B���ڢۢݢ� | C���٢ۢܢ� | D��ȫ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com