
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得ClO2:![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.1mol![]() 参加反应,转移2mol电子
参加反应,转移2mol电子
B.![]() 在反应中被氧化
在反应中被氧化
C.![]() 的还原性强于ClO2
的还原性强于ClO2
D.CO2是![]() 被氧化后得到的产物
被氧化后得到的产物
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】室温下,用0.100mol·L1的NaOH溶液分别滴定均为20.00mL0.100mol·L1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是
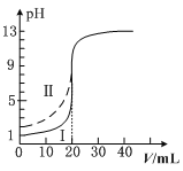
A.Ⅰ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL
C.V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D.V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示( )
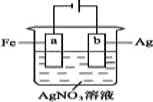

①c(Ag+) ②c(AgNO3) ③a棒的质量 ④b棒的质量 ⑤溶液的pH
A. ①③B. ③④C. ①②④D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,组成单质A的元素有可变化合价。它们之间存在如下图所示的转化关系。由此推断:

(1)甲的化学式为________________,丙的化学式为________________。
(2)写出甲和D反应的化学方程式:_________________________________________。
(3)为检验化合物甲中元素的化合价,需要用到的药品有________(填字母)。
A.稀硫酸 B.盐酸
C.硫氰化钾溶液 D.高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为了测定x值,进行下述实验:①称取ng草酸晶体配成100.00mL水溶液;②取25.00 mL所配制的草酸溶液置于锥形瓶中,加稀硫酸,用浓度为amol·L-1的KMnO4溶液滴定,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。反应生成MnSO4在水溶液中基本无色,试回答下列问题:
(1)实验台上有以下仪器,实验中不需要的是___(填序号)。
a.托盘天平(带砝码、镊子) b.滴定管 c.100 mL容量瓶 d.烧杯 e.漏斗 f.锥形瓶 g.玻璃棒 h.药匙 i.烧瓶
(2)实验中KMnO4溶液应装在___式滴定管中,原因是___。
(3)滴定过程中用去VmLamol·L-1的KMnO4溶液,则所配制的草酸的物质的量浓度为__mol·L-1,由此可计算x的值为___。
(4)若滴定终点读数时俯视,则计算出的x值可能__(填偏大、偏小、无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁碳混合物处理含Cu2+废水获得金属铜。当保持铁屑和活性炭总质量不变时,测得废水中Cu2+浓度在不同铁碳质量比(x)条件下随时间变化的曲线如下图所示。

下列推论不合理的是
A. 活性炭对Cu2+具有一定的吸附作用
B. 铁屑和活性炭会在溶液中形成微电池,铁为负极
C. 增大铁碳混合物中铁碳比(x),一定会提高废水中Cu2+的去除速率
D. 利用铁碳混合物回收含Cu2+废水中铜的反应原理:Fe+Cu2+=Fe2++Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用可逆反应N2(g)+3H2(g) ![]() 2NH3(g)合成氨,下列叙述正确的是( )
2NH3(g)合成氨,下列叙述正确的是( )
A.合成氨的适宜条件是高温高压催化剂,其中催化剂不改变该反应的逆反应速率
B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,NH3 (g)的浓度分别是c1、c2,则时间间隔t1~t2内,NH3 (g)生成的平均速率为v=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题。
(Ⅰ)下列一组有水参与的反应
①2Na+2H2O=2NaOH+H2↑
②2Na2O2+2H2O=4NaOH+O2↑
③Na2O+H2O=2NaOH
④3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
⑤2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
⑥2F2+2H2O=4HF+O2
(1)其中不属于氧化还原反应的是_____________(填编号)。
(2)在这些氧化还原反应中,水既作氧化剂,又作还原剂是___________(填编号),水既不作氧化剂,又不作还原剂是__________(填编号)。
(3)请你运用所学知识分析3NO2+H2O=2HNO3+NO是否属于氧化还原反应?___________(填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是________;
(Ⅱ)写出下列反应的离子方程式
①铜片与稀硝酸的反应_____________________________________;
②往氯化铝溶液中加入过量的NaOH溶液______________________;
(Ⅲ)写出下列反应的化学方程式
①二氧化硫发生催化氧化反应_________________________________;
②制漂白液的反应____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2(g)与H2(g)在一定条件下反应生成NH3(g),过程如下图,下列说法正确的是
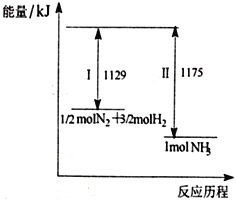
A. I为放热过程、Ⅱ为吸热过程
B. 1/2 molN2和3/2molH2的键能之和大于1 mol NH3的键能
C. 1/2molN2和3/2molH2所具有的能量之和低于1 mol NH3所具有的能量
D. 该过程的热化学反应方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ/mol
2NH3(g) ΔH=-92 kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com