
【题目】现有 A、B、C、D、E、F 六种短周期主族元素,原子序数依次增大。已知 A 的气态氢化物能与其最高价氧化物对应的水化物反应得到一种离子化合物,B 的一种单质具有杀菌消毒的作用,C+和 D3+的电子层结构相同,E 的主族序数是其周期序数的2倍。
(1)F 在元素周期表中的位置是__________________。
(2)上述元素形成的简单离子中,半径最大的是__________________ (填离子符号)
(3)由上述元素中的一种或几种组成的物质甲可以发生如图反应:
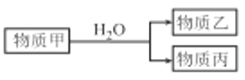
①若丙具有漂白性,则甲和水反应的离子方程式为_________________。
②若乙的水溶液是强碱性溶液,物质丙为B 的一种单质,则甲中含有的化学键类型为_______________,D 的单质与乙的水溶液反应的离子方程式为______________。
(4)A 的最高价氧化物对应的水化物的稀溶液与金属铜反应的离子方程式为_____________________________。
【答案】第三周期第VIIA 族 S2- C12 +H2O =H+ +C1- +HC1O 离子键、(非极性)共价键 2Al+2OH- +2H2O=2A1O2- +3H2 ↑ 3Cu+8H+ +2NO3- = 3Cu2+ +2NO ↑+4H2O
【解析】
A、B、C、D、E、F 六种短周期主族元素,原子序数依次增大。已知 A 的气态氢化物能与其最高价氧化物对应的水化物反应得到一种离子化合物,则A为氮(N);B 的一种单质具有杀菌消毒的作用,则B为氧(O);C+和 D3+的电子层结构相同,则C为钠(Na),D为铝(Al);E 为第三周期元素,其主族序数是其周期序数的2倍,则E为硫(S),F为氯(Cl)。
(1)F 为氯(Cl),在元素周期表中的位置是第三周期第VIIA 族。答案为:第三周期第VIIA 族;
(2)上述元素形成的简单离子中,半径最大的是电子层数多、核电荷数小的非金属离子,因为离子半径S2->Cl-,所以应为S2-。答案为:S2-;
(3)①若丙具有漂白性,则应为HClO,甲为Cl2,Cl2和水反应的离子方程式为C12 +H2O =H+ +C1- +HC1O。答案为:C12 +H2O =H+ +C1- +HC1O;
②若乙的水溶液是强碱性溶液,则其为NaOH,物质丙为B 的一种单质,则应为O2,甲为Na2O2,含有的化学键类型为离子键、(非极性)共价键;D 的单质为Al,与乙(NaOH)的水溶液反应,生成NaAlO2和H2,离子方程式为2Al+2OH- +2H2O=2A1O2- +3H2 ↑。答案为:离子键、(非极性)共价键;2Al+2OH- +2H2O=2A1O2- +3H2 ↑;
(4)A 的最高价氧化物对应的水化物为HNO3,它的稀溶液与金属铜反应,生成Cu(NO3)2、NO和H2O,离子方程式为3Cu+8H+ +2NO3- = 3Cu2+ +2NO ↑+4H2O。答案为:3Cu+8H+ +2NO3- = 3Cu2+ +2NO ↑+4H2O。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】写出下列热化学反应方程式:
(1)1mol硫酸和氢氧化钠稀溶液反应放出115kJ热量,写出表示中和热的热化学反应方程式__。
(2)0.5molC2H5OH(l)完全燃烧生成液态水放出683.4kJ热量,写出表示C2H5OH燃烧热热化学反应方程式___。
(3)24g碳与适量H2O(g)反应吸收262.6kJ热量__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.某课外活动小组同学用下图装置进行实验,试回答下列问题。
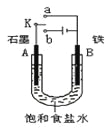
(1)若开始时开关K与a连接,则B极的电极反应式为________________________。
(2)若开始时开关K与b连接,则B极的电极反应式为_____,总反应的离子方程式为_________________,有关该实验的下列说法正确的是(填序号)___________。
①溶液中Na+向A极移动 ②从A极处逸出的气体能使湿润KI淀粉试纸变蓝 ③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 ④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模拟工业上用离子交换膜法制烧碱的方法,设想用下图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
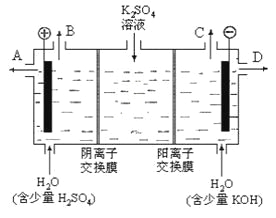
①该电解槽的阳极反应式为___________。此时通过阴离子交换膜的离子数_____(填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从_____________________________________________________________出口 (填写“A”、“B”、“C”、“D”)导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因_______________________。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯原子对O3分解有催化作用:
O3+Cl===ClO+O2 ΔH1
ClO+O===Cl+O2 ΔH2
大气臭氧层的分解反应是:O3+O===2O2 ΔH,该反应的能量变化如图:

下列叙述中,正确的是
A. 反应O3+O===2O2的ΔH=E1-E3
B. O3+O===2O2是吸热反应
C. ΔH=ΔH1+ΔH2
D. ΔH=E3-E2>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的1/10。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式。
正极:_____________________;负极:____________________。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,其中焊接在铁闸门的固体材料R可以采用_______________。
A.铜 B.钠 C.锌 D.石墨
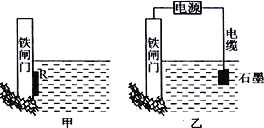
(3)上图中乙方案也可降低铁闸门腐蚀速率,其中铁闸门应该连接在直流电源的_____________极。
(4)除了以上金属防护的方法外,请再例举两种办法:___________;___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确但不是从实验安全角度考虑的是
A.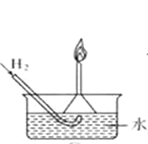 使用稍浸入液面下的倒扣漏斗检验氢气的纯度
使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B.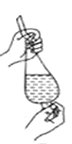 使用 CCl4 萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
使用 CCl4 萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
C.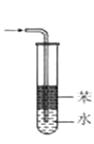 吸收氨或氯化氢气体并防止倒吸
吸收氨或氯化氢气体并防止倒吸
D.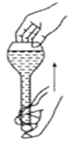 用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年3月科学家研发出一种新型的锌碘单液流电池,其原理如图所示。下列说法正确的是
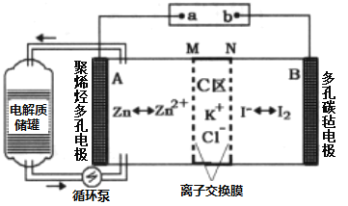
A.充电时B电极反应式为: I2 + 2e- = 2I-
B.放电时电解质储罐中离子总浓度减小
C.M为阴离子交换膜,N为阳离子交换膜
D.充电时,A极增重65g时,C区增加离子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程及实验装置(部分夹持装置省略)如图:下列叙述正确的是( )
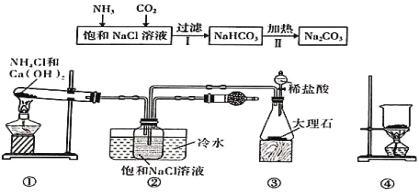
A.实验时先打开装置③中分液漏斗的旋塞,过一段时间后再点燃装置①的酒精灯
B.装置②的干燥管中可盛放碱石灰,作用是吸收多余的NH3
C.向步骤 I 所得滤液中通入氨气,加入细小的食盐颗粒并降温可析出NH4Cl
D.用装置④可实现步骤Ⅱ的转化,所得CO2可循环使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标号为①~⑩的元素,在元素周期表中的位置如下:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
试回答下列问题:
(1)(填写元素符号)① _____③______⑤_____ ⑦_____
(2)①和④号元素形成的化合物的化学式________,用电子式表示其形成过程为__________。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是: ______﹥_________ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是: ______ ﹥_________ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是________,在该化合物中既含有________键,又含有________键。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com