
【题目】利用下图装置进行实验,甲乙两池均为1 mol·L–1的AgNO3溶液,A、B均为Ag电极。实验开始先闭合K1,断开K2。一段时间后,断开K1,闭合K2,形成浓差电池,灵敏电流计指针发生偏转(提示:Ag+ 浓度越大,氧化性越强)。下列说法不正确的是( )

A. 闭合K1,断开K2后,A电极增重
B. 闭合K1,断开K2后,乙池溶液中Ag+浓度增大
C. 断开K1,闭合K2后,NO3–向A电极移动
D. 断开K1,闭合K2后,B电极发生氧化反应
科目:高中化学 来源: 题型:
【题目】元素①~⑧在元素周期表中的位置如下,回答有关问题:
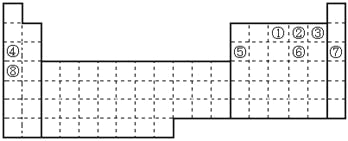
(1)画出⑥的离子结构示意图__________。
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为______(示例:用r(A2-)>r(B-)的形式表示)。
(3)元素②、③氢化物的稳定性由强到弱的顺序为________(填化学式)。
(4)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的电子式___________________________。
(5)表中能形成两性氢氧化物的元素是_______(填元素符号),写出该元素的单质与⑧的最高价氧化物的水化物反应的离子方程式____________________________。
(6)比较①与其同族短周期元素的氢化物的熔沸点高低,并说明理由_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关水的电离的说法正确的是
A. 将水加热,KW增大,pH不变
B. 向水中加入少量NaHSO4固体,恢复到原温度,水的电离程度增大
C. 向水中加入少量NaOH固体,恢复到原温度,水的电离被抑制,c(OH—)增大
D. 向水中加入少量NH4Cl固体,恢复到原温度,水的电离程度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量铝片与过量的稀盐酸反应,为了加快反应速率,同时几乎不影响生成的氢气总量,不可以采取的措施是
A. 加热,升高溶液温度 B. 将铝片改为等质量的铝粉
C. 加入少量CuSO4溶液 D. 加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 1mol金属钠与氧气完全反应,转移的电子数一定为NA
B. 25℃时,pH=1盐酸溶液中含有H+的数目约为0.1NA
C. 任意条件下,1mol苯中含C-C键的数目一定为3NA
D. 密闭容器中充入1molNO2,气体分子数一定是NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用系统命名法命名的有机物名称正确的是( )
A. 2 -甲基--4--乙基戊烷 B. 2, 3 --二甲基--1--戊烯
C. 3, 4, 4--三甲基己烷 D. 2, 2--二甲基-2-丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2molA与2molB混合于2L的密闭容器中,发生如下反应,2A(g)+3B(g) ![]() 2C(g)+2D(g),2s后A的转化率为50%,测得v(D)=0.25mol/(L·s)。下列推断不正确的是
2C(g)+2D(g),2s后A的转化率为50%,测得v(D)=0.25mol/(L·s)。下列推断不正确的是
A. z=2
B. 2s后,容器内的压强是初始的7/8倍
C. 2s时,C的体积分数为2/7
D. 2s后,B的浓度为0.5mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com