


科目:高中化学 来源: 题型:
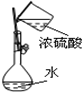 | 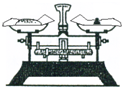 | 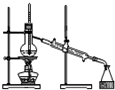 | 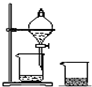 |
| A.配制硫酸溶液时,将浓硫酸慢慢注入盛有水的容量瓶中进行配制 | B.用托盘天平称量药品时,将药品置于天平左盘 | C.将混合液蒸馏分离时,应使温度计水银球浸没在混合液中 | D.分液时,将上下层液体依次从分液漏斗下口分别流入两个烧杯中 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2与O2的转化率可能相等 |
| B、容器中一定存在n(SO2)>1mol且n(SO3)<2mol |
| C、放出的热量为197 kJ |
| D、当O2的转化率为50%时SO2和SO3的物质的量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使水的温度升高 |
| B、增加水中O2的含量 |
| C、起到杀菌作用 |
| D、使水中HClO分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁中含有碳,抗腐蚀能力比纯铁弱 |
| B、用锡焊接的铁质器件,焊接处易生锈 |
| C、金属在海水中比在淡水中更易生锈 |
| D、电解熔融的氯化钠制取金属钠,用铁作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0,△S<0的反应肯定能自发进行 |
| B、原电池反应一定是自发进行的氧化还原反应,且△H<0 |
| C、体系能量增大和混乱度增大都有促使反应自发进行的倾向 |
| D、CaCO3(s)=CaO(s)+CO2(g)的△H>0,△S<0,该反应在较高温度下能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液与硫酸的反应:OH-+H+=H2O |
| B、碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、CH3COOH溶液与NH3?H2O溶液反应:H++OH-═H2O |
| D、澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由H+(aq)+OH-(aq)=H20(1)△H=-57.3 kJ?mol-1,可知含1 mo1 CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量为57.3 kJ |
| B、由C(石墨)=C(金刚石)△H=+1.9 kJ?mol-1,可知石墨比金刚石更稳定 |
| C、由N2(g)+3H2(g)=2NH3(g)△H=-92.4 kJ?mol-1,可知将1 mol N2(g)和3 mol H2(g)置于密闭容器中充分反应后放出热量为92.4 kJ |
| D、由△G=△H-T△S可知,所有的放热反应都能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18 g水所含分子数目为NA |
| B、17 g NH3所含氢原子数目为NA |
| C、标准状况下,2.24L O2所含的原子数为0.2NA |
| D、2.4 g金属镁所含电子数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com