
����Ŀ��ҽ���Ȼ��ƿ������������ơ�������������ҩ��Թ�ҵ̼��ƣ���������MgCl2���ʣ�����ҽҩ���Ȼ��Ƶ���Ҫ�������£�

��ش��������⣺
��1��������������Ҫ���ʵĻ�ѧʽΪ_____���Լ�A��_____��
��2�����������м������������������Һ��Ŀ����_____����������Ӧ�Ļ�ѧ����ʽΪ_____��
��3�����������У������ữ��Ŀ����_____���û�ѧ����ʽ��ʾ����
��4������I��������_____�������������_____��
���𰸡�Mg(OH)2�����ȥ��Һ�е�Mg2+Ca(OH)2+MgCl2��Mg(OH)2+CaCl2Ca(OH)2+2HCl��CaCl2+2H2O���������ᾧ
��������
��ҵ̼��Ƽ�������������ܽ������Ȼ��ƣ���Һ�к�������MgCl2���ʣ�����������������Ƴ���þ���ӣ����˵õ�����Ϊ������þ��������Һ�ữ���������ȥ�������������ƣ��õ���Һ�����õ��Ȼ��ƹ��壬�ݴ˽��
��1���������Ϸ�����֪��������������Ҫ���ʵĻ�ѧʽΪMg(OH)2���Լ�A�����
��2�����ڼ��������õ�����Һ�к����Ȼ�þ���ʣ������������м������������������Һ��Ŀ���dz�ȥ��Һ�е�Mg2+����������Ӧ�Ļ�ѧ����ʽΪCa(OH)2+MgCl2��Mg(OH)2+CaCl2��
��3�������������ƹ����������������У���A�����ữ��Ŀ���dz�ȥ������Ca(OH)2����Ӧ�Ļ�ѧ����ʽΪCa(OH)2+2HCl��CaCl2+2H2O��
��4���������Ϸ�����֪���������ǹ��˲������������Ǵ���Һ�еõ��Ȼ��ƹ��壬�������������ᾧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ���������ֵ�������й�������ȷ���ǣ��� ����
��1mol���к��е�̼̼˫����Ϊ3NA
��6.2g�����ƺ�7.8g�������ƵĻ�����к��е���������Ϊ0.6NA
��3.4gNH3�к�N��H����ĿΪ0.2NA
�ܳ�����1L 0.5mol/L NH4Cl��Һ��2L 0.25mol/L NH4Cl��Һ����NH4+����Ŀ��ͬ
�ݳ�����4.6gNO2��N2O4�������������ԭ������Ϊ0.3NA
�������Ũ�Ⱦ�Ϊ1mol/L����������ᣬ���������������֮��Ϊ3��1
��1mol������1mol�����г��ȼ�գ�ʧȥ�ĵ�����Ϊ3NA
������£�16.8g Fe������ˮ������ȫ��Ӧʧȥ0.8NA�����ӣ�
A. �٢ܢݢ� B. �ڢݢ� C. �ڢܢݢߢ� D. �ݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ���������ֵ������˵����ȷ����
A. 7.8gNa2O2������ˮ��Ӧ��ת�Ƶĵ�����Ϊ0.1NA
B. 36g��35Cl��37Cl��ɵ�����������������һ��Ϊ17NA
C. 25��ʱ��pH=12�İ�ˮ������OH-����ĿΪ0.01NA
D. 30 g�ɼ�ȩ(HCHO)�������ϵ���Һ������C-H������ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��һ����������ij������ϣ��Ի�ͭ��(��Ҫ�ɷ�ΪCu2S)Ϊԭ���Ʊ�����ͭ�۵Ĺ���������ͼ1��ʾ��
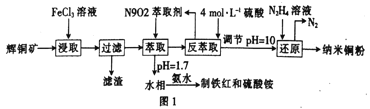
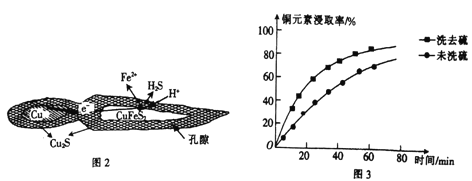
(1)�û�ͭ��(��Ҫ�ɷ�ΪCuFeS2)����ͭ����ϡ���Ṳͬ���ÿɻ�ýϴ�����Cu2S����ԭ����ͼ2��ʾ���÷�Ӧ�����ӷ���ʽΪ____________________________��
(2)�ӻ�ͭ���н�ȡͭԪ��ʱ������FeCl 3��Һ����ȡ����
�ٷ�Ӧ:Cu2S+4FeCl3=2CuCl2+4FeCl�±�2+S��ÿ����1molCuCl2����Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ_____����ȡʱ�������������¿�ά��Fe3+�ϸ�Ũ�ȣ��йط�Ӧ�����ӷ���ʽΪ_________��
�ڽ�ȡ�����м���ϴ�Ӽ��ܽ���ʱ��ͭԪ�ؽ�ȡ�ʵı仯��ͼ3��ʾ��δϴ��ʱͭԪ�ؽ�ȡ�ʽϵͣ���ԭ����________________��
(3)����ȡ��ʱ�����ֽ���������ȡ����pH�Ĺ�ϵ��ͼ4��ʾ����pH>1.7ʱ��pHԽ����������ȡ��Խ�ͣ�����Fe3+��ȡ�ʽ��͵�ԭ����_________________��

(4)�á�����ȡ���õ���CuSO4 ��Һ�Ʊ�����ͭ��ʱ���÷�Ӧ�л�ԭ�������������������֮��Ϊ_____��
(5)����ȡ��ġ�ˮ�ࡱ�м���������ˮ�����ã��پ����ˡ�_____�����____�Ȳ����ɵõ�Fe2O3 ��Ʒ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϵΪԪ�����ڱ��е���B�塢ԭ������Ϊ57~71��Ԫ�ء�
��1����(Dy)�Ļ�̬ԭ�ӵ����Ų�ʽΪ[Xe]4f106s2��������(Dy)ԭ����Χ�����Ų�ͼ��___________��
��2�����³��������籵ͭ�������к���Cu3+����̬ʱCu3+ �ĵ����Ų�ʽΪ________________��
��3���۲�����������ϵԪ�صĵ������������ж����п�����ʾ+3 �۵�Ԫ����___________(��Ԫ������)��������ϵԪ�صĵ�����(��λ��kJ mol-1)
Ԫ�� | I1 | I2 | I3 | I4 |
Yb(� | 604 | 1217 | 4494 | 5014 |
Lu(�壩 | 532 | 1390 | 4111 | 4987 |
La(�磩 | 538 | 1067 | 1850 | 5419 |
Ce(�棩 | 527 | 1047 | 1949 | 3547 |
��4��Ԫ����(Ce)�����γ������(NH4)2[Ce(NO3)6]��
���������������Ԫ�����縺���ɴ�С��˳��Ϊ________________(��Ԫ�ط��ű�ʾ)��
��д�����������̬�⻯��ˮ��Һ�д��ڵ������__________________(��дһ��)��
��Ԫ��Al Ҳ�����Ƴɼ��������̬�Ȼ������ӱ�ʾΪ(AlCl3)2��������Al ԭ���ӻ���ʽΪ_____________��������������ѧ��������______________(����ĸ)��
a.���Ӽ� b.���Լ� C.�Ǽ��Լ� d.��λ��
��5��PrO2(��������)�ľ���ṹ��CaF2��������������ԭ��λ�����ĺͶ�������PrO2(��������)�ľ�������________����ԭ������֪��������Ϊa pm���ܶ�Ϊ�� g�� cm-3��NA=_____________ (�ú�a�����Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. �ñ��Ӷ���ʢ��������ƿ�ڣ��Ϳ����ᵽ��������ζ
B. �������ſ����������ռ�������������
C. ���ȹ�����й©��Ӧ����緽����ɢȺ��
D. ��������Һ��й©ʱ��Ӧ������������й©����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�Ĺ��ɽ���Ԫ�أ�ͨ�������Ͻ���ֵ����Ӽ�������ǿ�Ͻ��ǿ�ȡ�Ӳ�ȡ��ɺ��Եȡ������ƾ���(Na2MoO4��2H2O)����Ϊ��������ȴˮϵͳ�Ľ�����ʴ���Ƽ�����ͼ15�ǻ����������Ի����(��Ҫ�ɷ�Ϊ����MoS2)Ϊԭ�����Ʊ������⡢�����ƾ������Ҫ����ͼ��

�ش���������:
��1����֪��Ӧ��Ϊ���ֽⷴӦ����������Կ�Ļ��ϼ�Ϊ___________��
��2����Ӧ�������ӷ���ʽΪ___________��
��3�����������ʱ�Ļ�ѧ����ʽΪ____________��
��4������XΪ_________����֪��������һ���¶ȷ�Χ�ڵ��������ʼ���Ӧ���ʵ��ܽ�����±���ʾ�����ڲ���X��Ӧ�����¶ȵ���ѷ�ΧΪ_______(�����)��
�¶�(��) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
�������� | Na2MoO4��10H2O | Na2MoO4��2H2O | Na2MoO4 | ||||||
�ܽ�� | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45.57 | |
A.0�桫10�� B.10�桫100�� C.15.5�桫50�� D.100������
��5���Ʊ������ƾ��廹����ͨ�����ƵĻ������ֱ�Ӽ������������Һ�����ķ����������������У��������������ɣ����������뻹ԭ�������ʵ���֮��Ϊ_________��
��6��Li��MoS2�ɳ���صĹ���ԭ��ΪxLi+nMoS2![]() Lix(MoS2)n[Lix(MoS2)n�����ڵ缫��]�����س��ʱ�����ĵ缫��ӦʽΪ___________________��
Lix(MoS2)n[Lix(MoS2)n�����ڵ缫��]�����س��ʱ�����ĵ缫��ӦʽΪ___________________��
��7�����û�ԭ������(CO��H2)��ԭMoO3���⣬��ҵ���Ʊ���ԭ������CO![]() 2CO+2H2���������������Ϊ90%��7L(��״��)��Ȼ��������������̼�ڸ����·�Ӧ������ת����Ϊ80%,�ò�����CO��H2��ԭMoO3���⣬�������������������Ϊ_________��
2CO+2H2���������������Ϊ90%��7L(��״��)��Ȼ��������������̼�ڸ����·�Ӧ������ת����Ϊ80%,�ò�����CO��H2��ԭMoO3���⣬�������������������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ���������ʵ������ȷ����(����)��
ѡ�� | ʵ���������ʵ | ���� |
A | �������Һ��S | �ȵ���������ų�Ag+��C |
B | �Ʊ���������ʱ,����Ӧ�����Թ�������Na2CO3��Һ��Һ���Ϸ� | ��������������̼������Һ,��ֹ�������� |
C | ��Fe(NO3)2��Һ�м���ϡ����,�Թܿ��к���ɫ������� | ��Һ��N |
D | ��Mg(HCO3)2��Ӳˮ��ʱ���ּ���,���յõ��ij��������Ҫ�ɷ�ΪMg(OH)2,������MgCO3 | Ksp(MgCO3)<Ksp[Mg(OH)2] |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ϢϢ��ء�����˵���������
A.���Ͻ�������ڸ�������B.����̿���г���ζ��ɱ������
C.��ʯ�ҿ�������װʳƷ�����D.����ͨ���ơ�������������ЧӦ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com