
【题目】某小组同学欲探究H2O2的性质,经历如下探究过程:
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是_________。
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。
实验① 实验②
实验②
(2)实验①利用了酸性高锰酸钾的_________ 性质,该实验中,证明KMnO4溶液与H2O2反应的现象除了溶液颜色变浅或褪色外,还有________。
(3)实验②是为了验证H2O2的_________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式____________。
解释和结论:
(4)以上实验可得出的结论是______________________ 。
【答案】H2O2中的O为-1价,可能降低为-2价,因此H2O2可能具有氧化性 氧化 有气体产生 氧化 2I-+H2O2+2H+= I2+2H2O H2O2既具有氧化性,也具有还原性
【解析】
(1)在化学反应中,化合价降低得电子的物质做氧化剂,具有氧化性,H2O2中的O为-1价,处于中间价态,即双氧水中的氧元素的化合价可降低显示氧化性;
(2)实验①利用酸性高锰酸钾具有强氧化性,与双氧水发生氧化还原反应,双氧水做还原剂,氧元素的化合价升高变为氧气,该反应现象为紫色高锰酸钾溶液褪色,同时有气体放出;
(3)实验②利用了碘化钾中碘为-1价,为碘元素的最低价态,具有还原性,验证双氧水具有氧化性,反应后的溶液中加入淀粉变蓝,说明碘化钾与双氧水发生氧化还原反应生成碘单质;
(4)实验①证明双氧水具有还原性,实验②证明双氧水具有氧化性,则结合上述实验得到最终结论。
(1)在化学反应中,化合价降低得电子的物质做氧化剂,具有氧化性,H2O2中的O为-1价,处于中间价态,氧元素的化合价可以升高,也可以降低,即双氧水中的氧元素的化合价可降低显示氧化性,故答案为:2O2中的O为-1价,可能降低为-2价,因此H2O2可能具有氧化性;
(2)实验①利用酸性高锰酸钾具有强氧化性,与双氧水发生氧化还原反应,双氧水做还原剂,氧元素的化合价升高变为氧气,该反应现象为紫色高锰酸钾溶液褪色,同时有气体放出,故答案为:氧化;有气体产生;
(3)实验②利用了碘化钾中碘为-1价,为碘元素的最低价态,具有还原性,验证双氧水具有氧化性,反应后的溶液中加入淀粉变蓝,说明碘化钾与双氧水发生氧化还原反应生成碘单质,发生的离子反应为:2I-+H2O2+2H+= I2+2H2O,故答案为:氧化;2I-+H2O2+2H+= I2+2H2O;
(4)实验①证明双氧水具有还原性,实验②证明双氧水具有氧化性,则结合上述实验得到最终结论:H2O2既具有氧化性,也具有还原性,故答案为:H2O2既具有氧化性,也具有还原性。


 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求,依靠理论知识做基础。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:K=![]() ,它所对应的化学反应为:________________。
,它所对应的化学反应为:________________。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)![]() CH3OH(g) △H=-90.8 kJ/mol
CH3OH(g) △H=-90.8 kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5 kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5 kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.3 kJ/mol
CO2(g)+H2(g) △H=-41.3 kJ/mol
总反应:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g) 的△H =____________;二甲醚(CH3OCH3)直接作燃料电池具有启动快,效率高等优点,若电解质为酸性,该电池的负极反应为________________。
CH3OCH3(g)+CO2(g) 的△H =____________;二甲醚(CH3OCH3)直接作燃料电池具有启动快,效率高等优点,若电解质为酸性,该电池的负极反应为________________。
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
该反应的正反应方向是_______反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为 0.020 mol/L,在该条件下,CO的平衡转化率为:________________。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如 NO、NO2、N2O4等,对反应N2O4(g)![]() 2NO2(g) △H >0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示.下列说法正确的是________________。
2NO2(g) △H >0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示.下列说法正确的是________________。
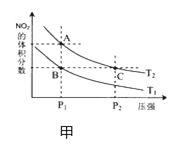
A. A、C 两点的反应速率:A>C
B. A、C 两点气体的颜色:A 深,C浅
C. B、C两点的气体的平均相对分子质量:B<C
D. 由状态 B 到状态 A,可以用加热的方法
E. A、C 两点的化学平衡常数:A>C
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加 n L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将________(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为________mol/L(NH3·H2O的电离平衡常数取Kb=2×10﹣5 mol/L)。
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图乙所示,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触。
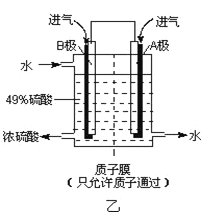
①溶液中H+的移动方向由________极到________极;(用 A、B 表示)
②B电极的电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家们研究开发了一种柔性手机电池,示意图如图所示[其中多硫化锂(Li2Sx)中x=2、4、6、8]。下列说法错误的是
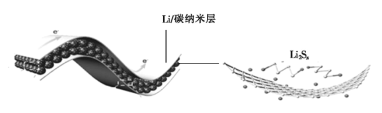
A.碳纳米层具有导电性,可用作电极材料
B.放电时,Li+移向Li2Sx膜
C.电池工作时,正极可能发生反应:2Li2S6+2Li++2e-=3Li2S4
D.电池充电时间越长,电池中Li2S2的量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池的工作原理:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料MnxZn(1-x)Fe2O4,其工艺流程如图所示:
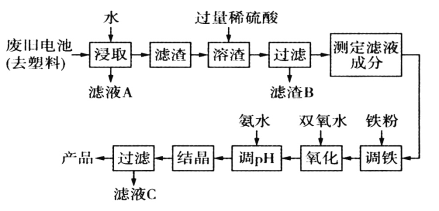
(1)滤液A中溶质的电子式为____________。
(2)已知MnxZn(1-x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为_________。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:_____________________________。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1-X)Fe2O4相符合。
①写出“调铁"工序中发生反应的离子方程式:_________________,___________________。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=amol.L-1,c(Fe2+)+c(Fe3+)=bmol.L-1,滤液体积为1m3,“调铁”工序中,需加入的铁粉质量为________kg(忽略溶液体积变化,用含a、b的代数式表示)。
(5)在“氧化"工序中,加入双氧水的目的是把Fe2+氧化为Fe3+;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是_______________。
(6)用氨水“调pH"后,经“结晶”“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一铁的氧化物样品,用140 mL 5 mol·L-1的盐酸恰好完全溶解,所得溶液还能与通入的0.56 L氯气(标准状况)反应,使Fe2+全部转化为Fe3+,则此氧化物为
A.Fe2O3B.Fe3O4C.Fe4O5D.Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入Y溶液中,生成沉淀的物质的量n2与所加X的物质的量n1的关系如图所示,符合如图所示的情况是( )
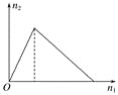
A.X为氢氧化钠,Y为氯化铝
B.X为氯化铝,Y为氢氧化钠
C.X为盐酸,Y为偏铝酸钠
D.X为偏铝酸钠,Y为盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
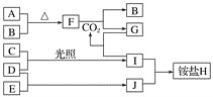
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCl2、BaCO3、BaSO4的化工厂,利用钡泥制取Ba(NO3)2,其部分工艺流程如图:
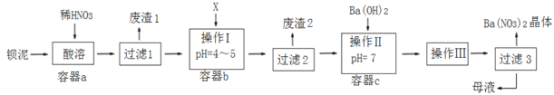
已知:①Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7
②Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小
下列有关说法不正确的是( )
A. 过滤2后滤液中含有硝酸,操作Ⅱ加入氢氧化钡中和得到硝酸钡溶液
B. X试剂应选过量的H2O2,目的是为了使溶液中的Fe2+转化为Fe3+,最终转化为Fe(OH)3沉淀
C. 操作Ⅲ蒸发结晶、冷却结晶
D. 此工艺流程生产流程会有氮的氧化物造成造成大气污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com