
【题目】实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求,依靠理论知识做基础。试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为:K=![]() ,它所对应的化学反应为:________________。
,它所对应的化学反应为:________________。
(2)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)![]() CH3OH(g) △H=-90.8 kJ/mol
CH3OH(g) △H=-90.8 kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5 kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5 kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.3 kJ/mol
CO2(g)+H2(g) △H=-41.3 kJ/mol
总反应:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g) 的△H =____________;二甲醚(CH3OCH3)直接作燃料电池具有启动快,效率高等优点,若电解质为酸性,该电池的负极反应为________________。
CH3OCH3(g)+CO2(g) 的△H =____________;二甲醚(CH3OCH3)直接作燃料电池具有启动快,效率高等优点,若电解质为酸性,该电池的负极反应为________________。
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,会发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
CO2(g)+H2(g),该反应平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
该反应的正反应方向是_______反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为 0.020 mol/L,在该条件下,CO的平衡转化率为:________________。
(4)从氨催化氧化可以制硝酸,此过程中涉及氮氧化物,如 NO、NO2、N2O4等,对反应N2O4(g)![]() 2NO2(g) △H >0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示.下列说法正确的是________________。
2NO2(g) △H >0,在温度为 T1、T2 时,平衡体系中 NO2的体积分数随压强变化曲线如图甲所示.下列说法正确的是________________。
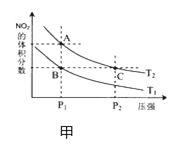
A. A、C 两点的反应速率:A>C
B. A、C 两点气体的颜色:A 深,C浅
C. B、C两点的气体的平均相对分子质量:B<C
D. 由状态 B 到状态 A,可以用加热的方法
E. A、C 两点的化学平衡常数:A>C
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,向该溶液滴加 n L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将________(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为________mol/L(NH3·H2O的电离平衡常数取Kb=2×10﹣5 mol/L)。
(6)某科研单位利用原电池原理,用SO2和O2来制备硫酸,装置如图乙所示,电极为多孔的材料能吸附气体,同时也能使气体与电解质溶液充分接触。
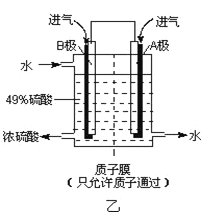
①溶液中H+的移动方向由________极到________极;(用 A、B 表示)
②B电极的电极反应式为____________。
【答案】C(s)+H2O(g)![]() CO(g)+H2(g) ﹣246.4 kJ/mol CH3OCH3-12e﹣+3H2O=2CO2+12H+ 放热 75% D 逆向
CO(g)+H2(g) ﹣246.4 kJ/mol CH3OCH3-12e﹣+3H2O=2CO2+12H+ 放热 75% D 逆向 ![]() B A SO2-2e-+2H2O═SO42-+4H+
B A SO2-2e-+2H2O═SO42-+4H+
【解析】
(1)根据质量守恒定律,结合可逆反应平衡常数的含义及表达式书写反应方程式;
(2)根据盖斯定律,将已知的热化学方程式叠加,就得到相应的反应的热化学方程式;CH3OCH3在负极失去电子,被氧化变为CO2、H2O,据此书写电极反应式;
(3)根据温度对化学平衡常数的影响判断反应的热效应;利用500℃时K=9,利用物质的起始浓度及反应转化关系计算CO的平衡转化率;
(4)根据外界条件对化学反应速率、化学平衡常数、化学平衡移动的影响分析判断;
(5)依据铵根离子水解分析回答;依据同粒子效应,一水合氨对铵根离子水解起到抑制作用;依据一水合氨的电离平衡常数计算得到氨水浓度;
(6)SO2与O2反应生成SO3,SO3再与水化合生成硫酸,根据硫酸的出口判断原电池的正负极,负极发生氧化反应,正极发生还原反应,原电池放电时,电解质溶液中阳离子向正极移动。
(1)平衡常数为生成物的浓度幂之积除以反应物的浓度幂之积,在平衡常数表达式中,分子为生成物,分母为反应物,固体或纯液体物质不能写入表达式中,再结合质量守恒定律,所以该反应的方程式为C(s)+H2O(g)![]() CO(g)+H2(g);
CO(g)+H2(g);
(2)①2H2(g)+CO(g)![]() CH3OH(g)△H=-90.8 kJ/mol
CH3OH(g)△H=-90.8 kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H=-23.5 kJ/mol
CH3OCH3(g)+H2O(g)△H=-23.5 kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-41.3 kJ/mol
CO2(g)+H2(g)△H=-41.3 kJ/mol
根据盖斯定律,将①×2+②+③,整理可得总反应的热化学方程式:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的△H =﹣246.4 kJ/mol;
CH3OCH3(g)+CO2(g)的△H =﹣246.4 kJ/mol;
二甲醚(CH3OCH3)直接作燃料电池具有启动快,效率高等优点,若电解质为酸性,该电池的负极反应为二甲醚失电子生成二氧化碳,负极的电极反应为:CH3OCH3-12e-+3H2O=2CO2+12H+;
(3)由于升高温度,化学平衡向吸热反应方向移动,对该反应来说,温度升高化学平衡常数K值减小,说明升高温度化学平衡逆向移动,逆反应为吸热反应,所以该反应的正反应为放热反应,假设反应消耗的CO浓度为x,则根据方程式CO(g)+H2O(g)![]() CO2(g)+H2(g)可知物质改变的物质的量相等,因此平衡时各种气体的物质的量浓度分别是:c(CO)=c(H2O)=(0.02-x) mol/L,c(CO2)=c(H2)=x mol/L,所以
CO2(g)+H2(g)可知物质改变的物质的量相等,因此平衡时各种气体的物质的量浓度分别是:c(CO)=c(H2O)=(0.02-x) mol/L,c(CO2)=c(H2)=x mol/L,所以![]() =9,解得x=0.015 mol/L,所以CO的平衡转化率为
=9,解得x=0.015 mol/L,所以CO的平衡转化率为![]() ×100%=75%;
×100%=75%;
(4)对反应N2O4(g)![]() 2NO2(g)△H >0,由于该反应的正反应为吸热反应,升高温度,平衡正向移动,NO2平衡时体积分数增大,根据图象可知NO2平衡时体积分数:A>B,说明温度:T2>T1。
2NO2(g)△H >0,由于该反应的正反应为吸热反应,升高温度,平衡正向移动,NO2平衡时体积分数增大,根据图象可知NO2平衡时体积分数:A>B,说明温度:T2>T1。
A.A点、C点温度相同,A点压强小于C点的压强,增大压强,化学反应速率越大,则反应速率:A<C,A错误;
B.在其他条件不变时,增大压强,化学平衡向正反应移动,使红棕色气体NO2的浓度增大,所以气体颜色C点比点深,即A点颜色浅,C点颜色深,B错误;
C.B、C两点NO2的体积分数相同,说明气体的总物质的量相同,由于气体总质量不变,所以混合气体的平均相对分子质量相同,C错误;
D.A、B两点的压强相同,气体温度A>B,在相同压强下,升高温度,化学平衡向吸热的正反应方向移动,则NO2的体积分数增大,所以由状态B到状态A,可以用加热的方法,D正确;
E.化学平衡常数只与温度有关,A、C两点的温度相同,所以它们的平衡常数也相等,E错误;
故合理选项是D;
(5)NO2可用氨水吸收生成NH4NO3,25℃时,将m mol NH4NO3溶于水,溶液显酸性,是由于NH4+水解,消耗水电离产生的OH-,最终达到平衡时,溶液中c(H+)>c(OH-),反应的离子方程式为:NH4++H2O![]() NH3H2O+H+;向其中加入氨水,使c(NH3H2O)增大,抑制了铵根离子水解,水解平衡逆向进行,水的电离平衡逆向移动;将m mol NH4NO3溶于水,向该溶液滴加n L氨水后溶液呈中性,则根据电荷守恒计算可知,溶液中氢氧根离子浓度c(OH-)=10-7mol/L,NH3H2O的电离平衡常数取Kb=2×10-5 mol/L,设混合后溶液体积为1 L,c(NH4+)=c(NO3-)=m mol/L;根据一水合氨电离平衡得到:NH3H2O
NH3H2O+H+;向其中加入氨水,使c(NH3H2O)增大,抑制了铵根离子水解,水解平衡逆向进行,水的电离平衡逆向移动;将m mol NH4NO3溶于水,向该溶液滴加n L氨水后溶液呈中性,则根据电荷守恒计算可知,溶液中氢氧根离子浓度c(OH-)=10-7mol/L,NH3H2O的电离平衡常数取Kb=2×10-5 mol/L,设混合后溶液体积为1 L,c(NH4+)=c(NO3-)=m mol/L;根据一水合氨电离平衡得到:NH3H2O![]() NH4++OH-,平衡常数K=
NH4++OH-,平衡常数K=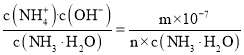 =2×10-5 mol/L,解得c(NH3H2O)=
=2×10-5 mol/L,解得c(NH3H2O)=![]() mol/L;
mol/L;
(6)该原电池中,负极上失电子被氧化,发生氧化反应,所以负极上投放的气体是SO2,SO2失电子和水反应生成SO42-和H+,正极上投放的气体是O2,正极上O2得电子和H+反应生成水,根据硫酸和水的出口方向知,B极是负极,A极是正极,所以B极上的电极反应式为:SO2-2e-+2H2O═SO42-+4H+,原电池放电时,溶液中的H+由负极B移向正极A,所以其电池反应式为:2SO2+O2+2H2O=2H2SO4。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B.Na2O2晶体中阳离子和阴离子个数比为2:1
C.Na2O2与CO2反应生成0.1 mol O2时转移电子0.4 mol
D.向饱和烧碱溶液中加入2 g Na2O2,充分反应完后,溶液中c(Na+)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①过量Na2O2投入到CuCl2溶液中
②过量Ba(OH)2溶液和硫酸铝溶液混合
③少量Ca(OH)2投入过量NaHCO3中
④澄清石灰水中通入少量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
A.全部B.①⑤C.②③④D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】福酚美克是一种影响机体免疫力功能的药物,可通过以下方法合成:
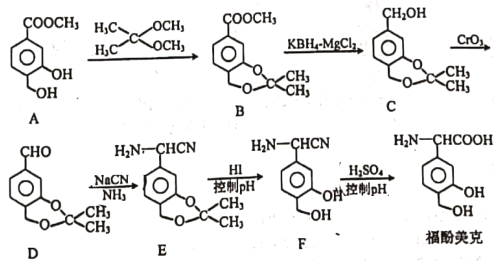
(1)B中的含氧官能团有________和_________(填名称);
(2)C→D的转化属于_________反应(填反应类型).
(3)已知E→F的转化属于取代反应,则反应中另—产物的结构简式为______。
(4) A (C9H10O4)的一种同分异构体X满足下列条件:
I.X分子有中4种不同化学环境的氢。
II. X能与FeCl3溶液发生显色反应。
III. lmol X最多能与4 mol NaOH发生反应
写出该同分异构体的结构简式:_____________。
(5)已知:![]()
![]()
![]() +R3CHO,根据已有知识并结合相关信息.
+R3CHO,根据已有知识并结合相关信息.
写出以  为原料制备
为原料制备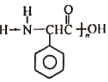 的合成路线流程图(无机试剂任用)。____________
的合成路线流程图(无机试剂任用)。____________
合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.Na ![]() Na2O
Na2O![]() NaOH
NaOH
B.MgCO3![]() MgCl2
MgCl2![]() Mg
Mg
C.Al2O3![]() Al
Al![]() Fe
Fe
D.Fe2O3![]() FeCl3
FeCl3![]() FeCl2(aq)
FeCl2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组拟利用如图装置制取干燥的氮气。下列说法错误的是( )

A.装置I中发生的反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B.加热片刻后需要将酒精灯移开,说明该反应是放热反应
C.装置II的作用是冷凝水蒸气
D.在装置III末端收集纯净干燥的N2只能用向下排空气法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:
CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1
COS(g)+H2(g) K=0.1
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应
B. 通入CO后,正反应速率逐渐增大
C. 反应前H2S物质的量为7mol
D. CO的平衡转化率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学欲探究H2O2的性质,经历如下探究过程:
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是_________。
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。
实验① 实验②
实验②
(2)实验①利用了酸性高锰酸钾的_________ 性质,该实验中,证明KMnO4溶液与H2O2反应的现象除了溶液颜色变浅或褪色外,还有________。
(3)实验②是为了验证H2O2的_________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式____________。
解释和结论:
(4)以上实验可得出的结论是______________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com