
【题目】硫酸厂烧渣(主要成分是Fe2O3,其次含少量的SiO2和FeS)经回收处理可制得绿矾(FeSO4·7H2O)和一种重要的水处理剂聚铁胶体[Fe(OH)SO4]n,上述生产工艺流程如下:

请通过分析回答下列相关问题:
(1)操作Ⅰ的名称是 _____。
(2)灼烧产生的尾气对大气有污染,因此工业生产中必须进行回收处理,下列方法可行的是____________。
A.直接用水吸收 B. 用氨水吸收
C. 用浓硫酸吸收 D. 与空气混合用石灰石粉末悬浊液吸收
(3)操作Ⅲ经蒸发浓缩、___________、过滤、____、干燥等。
(4)在由溶液X制聚铁胶体过程中①调节pH及②控制温度目的是_________。
(5)检验溶液X中金属阳离子所加试剂是______,其现象是___________ 。
(6)溶液X转化为溶液Y需加入一种常见物质是 ____________ 。
(7)在反应釜中FeS、O2及稀H2SO4反应生成硫酸铁等物质,则反应的离子方程式是________________________________________________________。
【答案】 过滤 B D 冷却结晶 洗涤 促使Fe3+充分水解并形成聚铁胶体 KSCN溶液 溶液变为血红色 Fe(或铁粉) 4FeS+ 3O2 + 12H+=4Fe3++ 4S + 6H2O
【解析】(1)操作Ⅰ之后得到固体混合物和溶液,故名称是过滤;(2)烧渣中含有FeS,燃烧产生二氧化硫,以尾气排放对大气有污染,二氧化硫是酸性气体,可以用碱或碱性物质吸收回收处理,则A、直接用水吸收,效果很差,不可行;B、用氨水吸收,效果显好,且可循环吸收,可行;C、浓硫酸不与二氧化硫反应,不可行;D、与空气混合用石灰石粉末悬浊液吸收,可转化为石膏,可行。答案选BD;(3)操作Ⅲ从溶液中得到绿矾晶体,可经蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作。(4)铁离子易水解形成胶体,在由溶液X制聚铁胶体过程中①调节pH及②控制温度目的是:促使Fe3+充分水解并形成聚铁胶体;(5)溶液X中金属阳离子是铁离子,检验所加试剂是KSCN溶液,其现象是溶液变为血红色;(6)溶液X转化为溶液Y是将铁离子还原为亚铁离子,在不引入杂质的情况下,最好加入铁粉;(7)在反应釜中FeS、O2及稀H2SO4反应生成硫酸铁、硫单质和水,其反应的离子方程式是:4FeS+ 3O2 + 12H+=4Fe3++ 4S + 6H2O。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】石墨晶体由层状石墨“分子”按 ABAB方式堆积而成,如右图(a)所示,并给出了一个石墨的六方晶胞如图(b)所示。

(1)每个晶胞中的碳原子个数为_________;
(2)在图中画出晶胞沿c轴的投影(用“●” 标出碳原子位置即可)________;
标出碳原子位置即可)________;
(3)假设石墨的层间距为300 pm,C-C键长为150 pm,计算石墨晶体的密度为_____ g·cm-3(碳元素的相对质量为12,NA=6.0×1023mol-1,计算结果保留一位小数);
(4)石墨可用作锂离子电池的负极材料,充电时发生下述反应: Li1-xC6+x Li++xe-→ LiC6 。其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。 在 LiC6中,Li+与相邻石墨六元环的作用力属_______键;
(5)某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等。回答:
![]()
(1)写出元素符号:A ;B ;C 。
(2)C的原子结构示意图: ;B的最高价氧化物对应水化物的化学式为 。
(3)A的氢化物的水溶液显 (填“酸”或“碱”)性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某燃料电池的工作原理如图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用。

下列说法正确的是
A. 该电池放电时K+向石墨Ⅰ电极迁移
B. 石墨Ⅰ附近发生的反应:NO2-e- +NO![]() =N2O5
=N2O5
C. O2在石墨Ⅱ附近发生氧化反应,Y为NO
D. 相同条件下,放电过程中消耗的NO2和O2的体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷、钛的单质及其化合物在生产生活中有重要的应用。回答下列问题:
(1)基态磷原子有________种不同能量的电子。
(2)N、P、As电负性由大到小的顺序为 ______ ,它们的氢化物沸点最高的为_______________,原因为___________________________。
(3)NO3- 离子的空间构型为_____,中心原子的杂化方式为_____ ,NO3-离子有多种等电子体,请写出一种_________ 。
(4)钛元素原子核外价电子排布图为____________,含Ti3+的配合物的化学式为[TiCl(H2O)5]Cl2·H2O,其配离子中含有的化学键类型为____________,该配离子的配位数为____________。
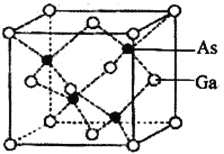
(5)砷化镓晶胞结构如下图。晶胞中距离Ga原子等距且最近的Ga原子有_________个,Ga与周围等距且最近的As形成的空间构型为____________。已知砷化镓晶胞边长为a pm,其密度为ρgcm-3,则阿伏加德罗常数的数值为_____________(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:
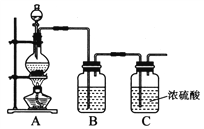
实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_______。装置B中盛放的试剂为_______,其作用为___________________。
(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______。
②装置D中发生的反应方程式为__________________。
③如果不用装置E会引起什么后果______________________。
④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与_______同时通入氢氧化钠溶液中。
(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42+H2O→N2+HSO3

①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________________。
②阴极的电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关。下列说法错误的是
A. 晶体硅是良好的半导体材料,用于制作光导纤维
B. 新型净水剂的制备和应用,进一步提高了饮用水的质量
C. 过氧化钠可用作为制氧剂
D. 深海底层“可燃冰”的试采成功,为其使用开拓了广阔前景
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)研究有机物一般经过以下几个基本步骤:分离、提纯 → 确定实验式 → 确定分子式 → 确定结构式。
已知:① 2R-COOH + 2Na → 2R-COONa + H2↑
② R-COOH + NaHCO3→ R-COONa + CO2↑ + H2O
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实 验 步 骤 | 解 释 或 实 验 结 论 |
(1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空: |
(2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g。 |
|
(3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 | (3)用结构简式表示A中含有的官能团 |
(4)A的核磁共振氢谱如下图: |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com