
| A. | 调味剂和着色剂是食品添加剂,添加量越多越好 | |
| B. | 蔬菜、水果富含膳食纤维,适量摄入有利人体健康 | |
| C. | 维生素c在人体内有重要功能,维生素c不溶于水 | |
| D. | 钾是人体必需的微量元素,食盐的主要成分是KCl |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某反应的△H>0、△S<0,则该反应一定不能正向自发进行 | |
| B. | 用简易量热计测定反应热时,需用环形玻璃搅拌棒搅拌使酸和碱充分反应 | |
| C. | 化合反应一定是放热反应,分解反应不一定是吸热反应 | |
| D. | 为加快漂粉精的漂白速率,使用时可滴加几滴醋酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
| A | K+、AlO2-、HCO3- | 少量CO2 | 2AlO2-+CO2+3H2O═2Al(OH) 3↓+CO32- |
| B | Ca2+、HCO3-、Cl- | 少量NaOH溶液 | Ca2++2HCO3-+2OH-═2H2O+CO32-+CaCO3↓ |
| C | Fe2+、NO3-、NH4+ | NaHSO4溶液 | 3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| D | NH4+、Al3+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
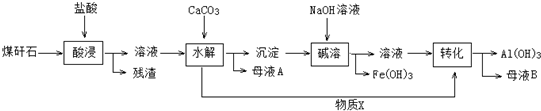
| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 2.1 | 3.2 |
| Al3+ | 4.1 | 5.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
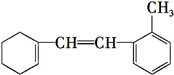
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
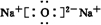 、
、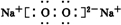 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
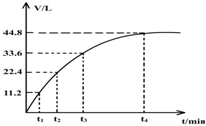 向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L.若将该混合物加入500ml15mol•L-的浓HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体.( )
向一洁净干燥的烧杯中加入44.4gAl粉与Fe粉混合物,然后加入过量的盐酸,产生标况下气体26.88L.若将该混合物加入500ml15mol•L-的浓HNO3中(不考虑发生钝化),产生的气体(标准状况下测定)如图所示,假设HNO3的还原产物为NO与NO2,那么理论上从哪一时刻开始产生NO气体.( )| A. | t1 | B. | t2 | C. | t3 | D. | t4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com