
【题目】下列反应中属于吸热反应的是
A. 镁与盐酸反应放出氢气 B. 氢氧化钠与盐酸反应
C. 硫粉在空气中燃烧 D. 八水氢氧化钡晶体与氯化铵反应
科目:高中化学 来源: 题型:
【题目】为了探究影响化学反应速率的因素,现设计如图所示两组对比试验:

(1)第1组:实验目的是探究________对化学反应速率的影响。
(2)第2组:甲中电流表指针偏转程度更大,说明反应物浓度越大,化学反应速率_____(“越大”“越小”)
(3)第2组甲中,当放出2.24L(标准状况)气体时,理论上消耗的锌的质量是____ g;
(4)甲烷-氧气燃料电池的工作原理如图所示:

①该电池工作时,a处(左侧)通入的物质为_______,b处(右侧)通入的物质为_____。
②该电池负极的电极反应式为________________。
③工作一段时间后,当12.8 g甲烷完全反应时,发生电子转移数目为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离或除杂方法不正确的是( )
A. 用分液法分离水和酒精 B. 用蒸馏法分离苯和溴苯
C. 用结晶法除去硝酸钾中的氯化钠杂质 D. 用饱和NaHCO3溶液除去CO2中混有的少量HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:
Fe2O3(s)+3CO(s,石墨)═2Fe(s)+3CO2(g)△H1=+489.0kJmol﹣1
C(s,石墨)+CO2(g)═2CO(g)△H2=+172.5kJmol﹣1
则CO还原Fe2O3(s)的热化学方程式为_____。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H
①取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H____0(填“>”、“<”或“=”,下同)。
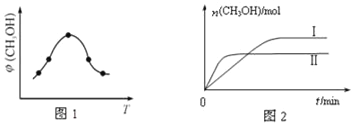
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数关系为KⅠ_____KⅡ。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成.开始以氨碳比![]() =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为_____。
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为_____。
②将足量CO2通入饱和氨水中可得氮肥NH4HCO3,已知常温下一水合氨Kb=1.8×10﹣5,碳酸一级电离常数Ka=4.3×10﹣7,则NH4HCO3溶液呈_____(填“酸性”、“中性”或“碱性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国南朝(梁)陶弘景著《本草经集注》中记叙药物730种,其中“消石”条目下写道:“…如握雪不冰.强烧之,紫青烟起,仍成灰…”.这里的“消石”是指( )
A.氯化钠
B.硝酸按
C.高锰酸钾
D.硝酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见氨基酸中唯一不属于α-氨基酸的是脯氨酸。它的合成路线如下:
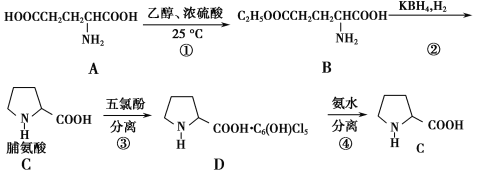
(1)化合物A的名称(用系统命名法命名)是________;反应①的类型为_______________________。
(2)写出一种不含手性碳原子的常见氨基酸的结构简式:__________。
(3)反应B→C可看作两步进行,其中间产物的分子式为C5H7O3N,且结构中含有五元环状结构。写出由B反应生成中间产物的化学方程式:___________________________________________。
(4)合成路线中设计反应③、④的目的是_____________________________。
(5)已知R-NO2![]() R-NH2,写出以甲苯和乙醇为原料制备
R-NH2,写出以甲苯和乙醇为原料制备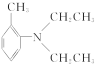 的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:CH2===CH2
的合成路线流程图(无机试剂任选)。合成路线流程图示例如下:CH2===CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.胶体和溶液、浊液的本质区别是能否产生“丁达尔效应”
B.氢氧化铁胶体能吸附水中的悬浮颗粒并沉降,起到净水作用
C.当光束通过硫酸铜溶液时可看见一条光亮的通路
D.胶体的分散质粒子的直径大于10﹣7m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是一种重要的含氧酸.实验室用浓硫酸与乙二酸(H2C2O4)晶体加热,可获得CO与CO2的混合气体,再将混合气体进一步通过(填一种试剂的名称)即可得纯净干燥的CO.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com