
【题目】一定条件下,可逆反应X(g)+3Y(g)=2Z(g)若X.Y.Z起始浓度分别为c1、c2、c3(均不为0),当达到平衡是X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
A.c1:c2=1:3
B.平衡时,Y 和Z的反应速率之比为3:2
C.X、Y的转化率不相等
D.c1的取值范围为0<c1<0.14mol/L
【答案】C
【解析】
试题分析:若反应向正反应进行到达平衡,X、Y的浓度最大,Z的浓度最小,假定完全反应,则:
根据方程式 X(气)+3Y(气)![]() 2Z(气)
2Z(气)
开始(mol/L):c1 c2 c3
变化(mol/L):0.04 0.12 0.08
平衡(mol/L):0.1 0.3 0.08
c1=0.14 c2=0.42 c3=0
若反应逆正反应进行到达平衡,X、Y的浓度最小,Z的浓度最大,假定完全反应,则:
根据方程式 X(气)+3Y(气)![]() 2Z(气)
2Z(气)
开始(mol/L):c1 c2 c3
变化(mol/L):0.1 0.3 0.2
平衡(mol/L):0.1 0.3 0.08
c1=0 c2=0 c3=0.28
由于为可逆反应,物质不能完全转化所以起始时浓度范围为0<c(X)<0.14,0<c(Y)<0.42,0<c(Z)<0.28,A、X 和Y平衡浓度为1:3,变化的量为1;3,所以起始量为1:3,c1:c2=1:3,A正确;B、平衡时,Y和Z的生成速率之比为化学方程式系数之比为3:2,B正确;C、X、Y的变化量之比和起始量之比相同,所以转化率相同,C错误;D、依据上述计算,c1的取值范围为0<c1<0.14molL-1,D正确;答案选C。


科目:高中化学 来源: 题型:
【题目】已知:SO![]() +Br2+H2O―→SO
+Br2+H2O―→SO![]() +2Br-+2H+。某溶液中可能含有Na+、NH
+2Br-+2H+。某溶液中可能含有Na+、NH![]() 、Fe2+、K+、Br-、SO
、Fe2+、K+、Br-、SO![]() 、SO
、SO![]() ,且所有离子物质的量浓度相等。向该无色溶液中滴加少量氯水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
,且所有离子物质的量浓度相等。向该无色溶液中滴加少量氯水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
A. 肯定不含Br- B. 无法确定SO![]() 是否存在
是否存在
C. 肯定含有SO![]() D. 肯定含有Na+
D. 肯定含有Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国里昂的科学家发现一种只由四个中子组成的微粒,这种微粒称为“四中子”,也有人称之为“零号”元素。它与天体中的中子星构成类似。有关该微粒说法正确的是
A. 该微粒不显电性 B. 该微粒的质量数为2
C. 在元素周期表中与氢元素占同一位置 D. 它与普通中子互称同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等.
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为 .
(2)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中(约1550℃)下通过下面两个反应共熔得到.
①2Ca3(PO4)2(s)+5C(s)═6CaO(s)+P4(s)+5CO2(g)△H1=+Q1kJmol﹣1
②CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣Q2kJmol﹣1
写出电炉中发生总反应的热化学方程式 .
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10;10C+P4O10=P4↑+10CO↑,上述反应中的各种物质,属于酸性氧化物的有 .
(Ⅱ)离子交换膜是一类具有离子交换功能的高分子材料.一容器被离子交换膜分成左右两部分,如右图所示.若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),一段时间后右边可观察到的现象: ,若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42﹣通过交换膜时(若反应迅速完全),则左右两室沉淀的物质的量之比为 .
![]()
(Ⅲ)某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质,利用相关工艺可进行提纯与综合利用.通入一定量的N2后,在1500℃下与Cl2充分反应得到纯化石墨与气体混合物,然后降温至80℃,分别得到不同状态的两类物质a和b.(注:石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃.)
(1)若a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性,化学反应方程式为 .
(2)若b与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某恒温恒容的密闭容器内发生反应:2A(g)+B(g)![]() C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是
C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是
A. 再充入2mol A,平衡正移,A的转化率增大
B. 如果升高温度,C的体积分数增大
C. 如果增大压强,化学平衡一定向正反应方向移动,B的体积分数减小
D. 再充入1mol C,C的物质的量浓度将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知阿伏伽德罗常数可表示为NA,则下列说法正确的是( )
A.17gNH3所含中子数目为10 NA
B.常温常压下,22 g氧气和26 g臭氧所含的氧原子总数为3NA
C.常温常压下,18g H2O含有的电子总数为8NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[aFe2(SO4)3·b(NH4)2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
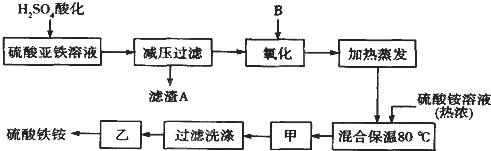
请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是 。
(2)下列物质中最适合的氧化剂B是 。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲的名称是:甲 。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量 (填试剂的化学式)检验Fe2+是否已全部被氧化;
(5)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3)2溶液,恰好完全反应。则该硫酸铁铵的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.8g Fe全部溶于一定浓度、200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,下列有关判断正确的是
A.反应后溶液中c(NO3-)=0.85mol/L
B.反应后的溶液最多还能溶解1.4gFe
C.反应后溶液中铁元素可能以Fe2+形式存在
D.1.12L气体可能是NO、NO2的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )
pC(g)△H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是( )

①m+n>p
②x点表示的正反应速率大于逆反应速率
③n>p
④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大.
A.①②⑤ B.只有②④ C.只有①③ D.只有①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com