
【题目】某兴趣小组探究SO2气体的还原性,装置如图所示,下列说法不合理的是
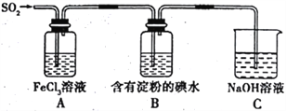
A. A装置中FeCl3溶液逐渐变为浅绿色,可以说明SO2有还原性
B. B装置中蓝色退去,说明还原性:SO2>I-
C. C装置中吸收尾气有可能倒吸
D. A、B装置中发生的反应转移电子数一定相等。
【答案】D
【解析】
A项,A装置中FeCl3溶液逐渐变为浅绿色,Fe3+被还原为Fe2+,说明SO2具有还原性;
B项,B装置中蓝色褪去,说明SO2与碘水发生了氧化还原反应,依据氧化还原反应中还原性:还原剂>还原产物分析;
C项,SO2能被NaOH溶液迅速吸收,导致C装置中导管内压强明显减小,C装置中可能产生倒吸;
D项,A、B装置中消耗反应物物质的量不确定。
A项,A装置中FeCl3溶液逐渐变为浅绿色,说明Fe3+被还原为Fe2+,则SO2被氧化,A装置中发生的反应为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,说明SO2具有还原性,A项正确;
B项,B装置中蓝色褪去,说明SO2与碘水发生了氧化还原反应,反应的离子方程式为SO2+I2+2H2O=4H++SO42-+2I-,在该反应中SO2为还原剂,I-为还原产物,氧化还原反应中还原性:还原剂>还原产物,则还原性:SO2>I-,B项正确;
C项,SO2污染大气,用NaOH溶液吸收尾气,SO2能被NaOH溶液迅速吸收,导致C装置中导管内压强明显减小,C装置中可能产生倒吸,C项正确;
D项,A、B装置中发生的离子反应依次为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+、SO2+I2+2H2O=4H++SO42-+2I-,由于A、B装置中消耗反应物物质的量不确定,A、B装置中反应转移电子物质的量不一定相等,D项错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】普鲁卡因毒性较小,是临床常用的局部麻药之一。某兴趣小组以苯和乙烯为主要原料,采用以下路线
合成:
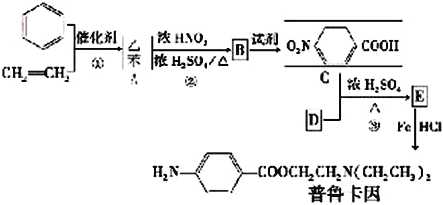
请回答下列问题:
(1)写出下列反应类型,反应①属于_________反应,反应②属于__________反应。反应②中混酸的配制方法为________________________________________。化合物B的结构简式___________________。
(2)写出C中所含的1个官能团的名称是:__________________________。已知: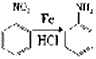 (NH3分子去掉一个H原子叫氨基-NH2)。并写出C+D-→E 反应的化学方程式:_______________________________。
(NH3分子去掉一个H原子叫氨基-NH2)。并写出C+D-→E 反应的化学方程式:_______________________________。
(3)已知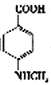 与化合物B 是同分异构体,且同时符合下列条件①②。写出同时符合下列条件的B的2个同分异构体的结构简式_________________、_____________________。
与化合物B 是同分异构体,且同时符合下列条件①②。写出同时符合下列条件的B的2个同分异构体的结构简式_________________、_____________________。
①分子中含有羧基 ②分子中含有苯环,且含有两个处于对位的取代基
(4)a-甲基苯乙烯(AMS) ![]() 与乙苯都属于烃类中的同一类别,该类别的名称是________。
与乙苯都属于烃类中的同一类别,该类别的名称是________。
a.芳香烃 b.烯烃 c.苯的同系物
(5)设计一条由AMS合成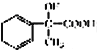 的合成路线:___________________________________。
的合成路线:___________________________________。
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2S和Na2SO3的混合溶液中加入足量的稀硫酸溶液,发生以下反应:
________Na2S+_________Na2SO3+________H2SO4→_______Na2SO4+_______S↓+______H2O
(1)配平上述化学方程式,标出电子转移的方向和数目。________________
(2)反应中被氧化的元素是___________。
(3)反应中氧化产物和还原产物物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 200 mL 2 mol·L-1的FeBr2溶液中通入11.2 L标准状况下的氯气:4Fe2++6Br-+5Cl2===4Fe3++3Br2+10Cl-
B. 以石墨作电极电解氯化铝溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C. 氢氧化钠溶液吸收足量SO2气体:SO2+2OH-===SO![]() +H2O
+H2O
D. 向明矾溶液中加入氢氧化钡溶液至沉淀的物质的量最大:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用阴离子交换膜控制电解液中OH-的浓度制备纳米Cu2O,反应为2Cu+H2O![]() Cu2O+H2↑,装置如图,下列说法中正确的是
Cu2O+H2↑,装置如图,下列说法中正确的是
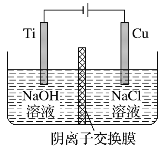
A. 电解时Cl-通过交换膜向Ti极移动
B. 阳极发生的反应为:2Cu -2e- +2OH- = Cu2O+H2O
C. 阴极OH-放电,有O2生成
D. Ti电极和Cu电极生成物物质的量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为硬脂酸甘油酯在碱性条件下水解的装置图,进行皂化反应时的步骤如下:
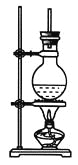
(1)在圆底烧瓶中加入7~8 g硬脂酸甘油酯,然后加入2~3 g的氢氧化钠、5 mL水和10 mL酒精,加入酒精的作用是__________________________________。
(2)隔着石棉网给反应混合物加热约10 min,皂化反应基本完成,所得的混合物为________(选填“悬浊液”、“乳浊液”、“溶液”或“胶体”)。
(3)向所得混合物中加入________,静置一段时间后,溶液分为上下两层,肥皂在________层,这个操作称为____________。
(4)图中长玻璃导管的作用为
________________________________________________________________________。
(5)写出该反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于某些离子的检验及结论一定正确的是
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO![]()
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO![]()
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH![]()
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com