
【题目】运用有关概念,判断下列叙述正确的是![]()
A.![]() 溶于水后能导电,故C
溶于水后能导电,故C![]() 为电解质
为电解质
B.![]() 、
、![]() 、
、![]() 、
、![]() 互为同素异形体
互为同素异形体
C.NaCl溶液和![]() 溶液均显中性,故两溶液中水的电离程度相同
溶液均显中性,故两溶液中水的电离程度相同
D.溶液与胶体本质区别为分散质微粒直径的大小不同
【答案】D
【解析】
A.电解质必须是自身电离产生的离子导电;
B.同种元素的不同单质,互为同素异形体;
C.![]() 促进水的电离;
促进水的电离;
D.当分散剂是水或其它物质时,根据分散质粒子直径大小来分类,把分散系划分为:溶液(小于1nm)、胶体(1nm~100nm)、浊液(大于100nm)。
A.二氧化碳溶于水后能导电,是由与水反应生成的碳酸电离出离子而导电,二氧化碳不能自身电离,所以二氧化碳为非电解质,故A错误;
B.![]() 、
、![]() 、
、![]() 、
、![]() 是化合物,不是单质,故B错误;
是化合物,不是单质,故B错误;
C.![]() 促进水的电离,NaCl对水的电离无影响,所以两溶液中水的电离程度不同,故C错误;
促进水的电离,NaCl对水的电离无影响,所以两溶液中水的电离程度不同,故C错误;
D.当分散剂是水或其它溶液时,根据分散质粒子直径大小来分类,把分散系划分为:溶液![]() 小于
小于![]() 、胶体
、胶体![]() 、浊液
、浊液![]() 大于
大于![]() ,所以,溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小,故D正确;
,所以,溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小,故D正确;
故选:D。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】在一个2L的恒容密闭容器中,加入3molA和1molB发生如下反应:3A(g)+B(g)![]() 2C(g)+3D(?)。5min后达到平衡,C的浓度为0.6mol·L-1。达到平衡后,当升高温度时,A的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
2C(g)+3D(?)。5min后达到平衡,C的浓度为0.6mol·L-1。达到平衡后,当升高温度时,A的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的正反应是___反应(填“吸热”或“放热”),D的状态是__(填“气态”或“非气态”)。
(2)达到平衡时,A的转化率为___,此温度下的平衡常数K=___(保留两位小数)。
(3)若加入适量B,则A的转化率将___(填“增大”“减小”或“不变”,下同),化学平衡常数将__。
(4)若B是有色物质,A、C均为无色物质,则上述反应达到平衡后:
①再加入适量A时,混合物的颜色___(填“变浅”“变深”或“不变”,下同);
②再加入适量C时,混合物的颜色__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列说法错误的是
A.l00g质量分数为46%的乙醇水溶液中氧原子数为4NA
B.向FeI2溶液中通人适量Cl2,当有1mol Fe2+被氧化时,反应转移电子数目为3NA
C.某温度下,1L pH=2的H2SO4溶液中,硫酸和水电离出的H+总数为0.01NA
D.常温下,1L 0.1mol·L1醋酸钠溶液中加入醋酸至中性,则溶液中CH3COO-数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某1L待测溶液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种:
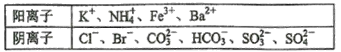
现进行如下实验操作(每次实验所加试剂均过量)
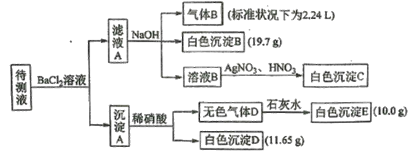
下列说法不正确的是
A.向溶液B中加AgNO3与HNO3的操作是多余的,待测液中一定含有的离子是K+、NH4+、CO32-、HCO3-、且c(K+)≥0.1mol·L-1
B.生成白色沉淀B的离子方程式为Ba2++HCO3-+OH-=BaCO3↓+H2O
C.已知白色沉淀C能溶于浓氨水,离子方程式为AgCl+2NH3·H2O=Ag(NH3)2++Cl-+2H2O
D.若无色气体D是混合气体,则沉淀A的成分可能是BaCO3、BaSO3、BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.镀锌铁板是利用了牺牲阳极的阴极保护法来达到防止腐蚀的目的
B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,说明BaCl2溶液显酸性
C.合成氨反应需使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动
D.汽车尾气的净化反应2NO+2CO![]() 2CO2+N2△H<0,则该反应一定能自发进行
2CO2+N2△H<0,则该反应一定能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知 4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol1
①该反应在________________(填“高温、低温或任何温度”)下能自发进行。
②对于该反应,改变某一反应条件(温度T1>T2),下列图象正确的是_______(填序号)。
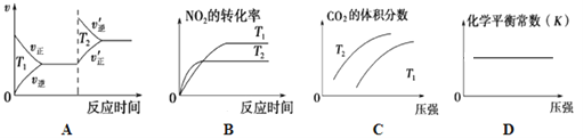
③某实验小组模拟上述净化过程,一定温度下,在2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________;两种方式达平衡时,N2的体积分数:甲______乙( 填“>、=、<或不确定”,下同),NO2的浓度:甲______乙。

(2)柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
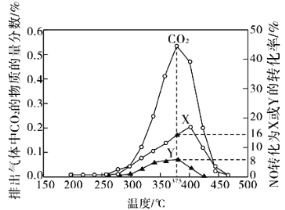
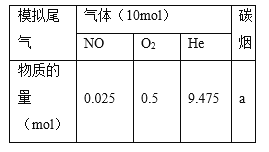
①375℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为________。
②实验过程中采用NO模拟NOx,而不采用NO2的原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答实验室配制0.1 mol/L的NaOH溶液500 mL实验中的下列问题。
(1)需NaOH_________g。
(2)有以下仪器:
①烧杯 ②100 mL量筒 ③药匙 ④500 mL容量瓶 ⑤胶头滴管 ⑥托盘天平,配制时,还缺少的玻璃仪器是__________________。
(3)下列称量NaOH的操作中,正确的是_______________。(填序号,下同)
①把NaOH直接放在托盘上称量
②把NaOH放在称量纸上称量
③把NaOH放入烧杯中称量
(4)使用容量瓶前必须进行的一步操作是_____________________________。
(5)配制过程中,下列操作会引起误差偏高的是_______________________。
①未洗涤烧杯、玻璃棒
②NaOH溶液未冷却至室温就转移到容量瓶中
③容量瓶不干燥,含有少量蒸馏水
④称量NaOH的时间太长
⑤定容时俯视刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型可充电钠离子电池因具有原料储量丰富,价格低廉,安全性高等优点而备受青睐,而![]() 因理论比容量较高,充放电过程中材料结构稳定,有利于
因理论比容量较高,充放电过程中材料结构稳定,有利于![]() 的可逆脱嵌,可以作为一种非常有潜力的正极材料,下列说法不正确的是
的可逆脱嵌,可以作为一种非常有潜力的正极材料,下列说法不正确的是
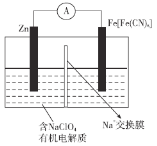
A.放电时,![]() 上的电势比Zn片上的高
上的电势比Zn片上的高
B.放电时,正极反应为![]()
C.充电时,外电路中通过0.2 mol电子时,阴极质量增加6.5 g
D.对于正极材料,充电可实现![]() 的嵌入,放电可实现
的嵌入,放电可实现![]() 的脱嵌
的脱嵌
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com