
(8分)从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
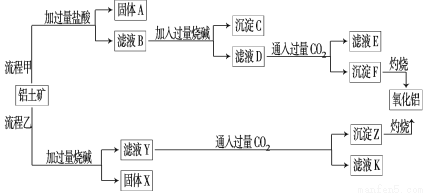
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_______________________________。
(2)流程乙加入烧碱后生成SiO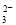 的离子方程式为___________________________。
的离子方程式为___________________________。
(3)验证滤液B含Fe3+,可取少量滤液并加入__________________(填试剂名称)。
(4)滤液E、K中溶质的主要成分是_____(填化学式),写出该溶质的一种用途________。
(5)已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12。取适量的滤液B,加入一定量的烧碱至达到沉淀溶解平衡,测得pH=13.00,则此温度下残留在溶液中的c(Mg2+)=__________。
21. (共8分) (除化学方程式2分外,其余每空1分)
(1)Al2O3+6H+===2Al3++3H2O
(2)SiO2+2OH-===SiO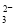 +H2O
+H2O
(3)硫氰化钾(或硫氰酸钾、等合理答案)
(4)NaHCO3 制纯碱(或作发酵粉等)
(5)5.6×10-10 mol/L
【解析】
试题分析:工艺流程图上的线路流程甲铝土矿加过量盐酸后二氧化硅不反应过滤得固体A;Al2O3、Fe2O3、MgO分别和盐酸反应生成氯化铝、氯化铁、氯化镁混合滤液B,加入过量氢氧化钠反应后生成氢氧化铁、氢氧化镁沉淀C、偏铝酸钠滤液D,通入过量二氧化碳后反应生成Al(OH)3沉淀F,滤液E(NaHCO3);路线流程乙铝土矿加过量氢氧化钠后,Fe2O3、MgO不反应过滤得固体X,SiO2、Al2O3分别于氢氧化钠反应生成硅酸钠、偏铝酸钠液过滤得滤液Y,向滤液Y中通入过量的CO2得到沉淀Z和滤液K(主要为NaHCO3);则(1)流程甲加入盐酸后生成Al3+的离子方程式为Al2O3+6H+===2Al3++3H2O(2) 流程乙加入烧碱后生成SiO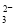 的离子方程式为SiO2+2OH-===SiO
的离子方程式为SiO2+2OH-===SiO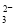 +H2O(3)检验Fe3+常用的化学试剂为硫氰化钾溶液,所以验证滤液B含Fe3+,可取少量滤液并加入硫氰化钾(4)滤液E、K中溶质的主要成分是NaHCO3,(5)pH=13.00的溶液OH-的浓度为0.1mol/L, 已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,所以(0.1)2x[Mg2+]=5.6×10-12得到[Mg2+]=5.6×10-10mol/L.
+H2O(3)检验Fe3+常用的化学试剂为硫氰化钾溶液,所以验证滤液B含Fe3+,可取少量滤液并加入硫氰化钾(4)滤液E、K中溶质的主要成分是NaHCO3,(5)pH=13.00的溶液OH-的浓度为0.1mol/L, 已知298 K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,所以(0.1)2x[Mg2+]=5.6×10-12得到[Mg2+]=5.6×10-10mol/L.
考点:考查二氧化硅和铝及其化合物的性质,把握流程中发生的化学反应,沉淀溶解平衡的计算等知识。


科目:高中化学 来源:2015届江西省高三暑期化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.少量金属钠加到冷水中:Na+2H2O===Na++2OH-+H2↑
B.NaHCO3溶液中滴加少量Ca(OH)2溶液:Ca2++OH-+HCO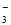 ===CaCO3↓+H2O
===CaCO3↓+H2O
C.硫酸铝溶液中加入过量氨水:Al3++4NH3·H2O===AlO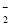 +4NH
+4NH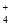 +2H2O
+2H2O
D.将2 mol/L AlCl3溶液和7 mol/L NaOH溶液等体积混合:2Al3++7OH-===Al(OH)3↓+ AlO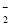 +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届江西省第一学期高三第一次月考化学(A卷)试卷(解析版) 题型:选择题
常温,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中: I-、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
用等体积的0.1mol/L的BaCl2 溶液,可使相同体积的Fe2 (SO4 )3 、 Na2 SO4 、 KAl(SO4)2 三种溶液中的SO42-完全沉淀,则三种硫酸盐的物质的量浓度之比为
A. 3:2:3 B. 3:1:2 C. 2:6:3 D. 1:1:1
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.小苏打溶液中加入少量石灰水:HCO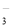 + Ca2+ + OH- = CaCO3↓ + H2O
+ Ca2+ + OH- = CaCO3↓ + H2O
B.稀硝酸中加入过量铁粉: Fe + 4H++ NO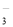 = Fe3++ NO↑ + 2H2O
= Fe3++ NO↑ + 2H2O
C.溴化亚铁溶液中通入足量氯气:2Fe2++ 2Br-+ 2Cl2 = 2Fe3++ Br2 + 4Cl-
D.苯酚钠溶液中通入少量二氧化碳: 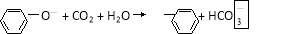
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市高三8月月考化学试卷(解析版) 题型:选择题
向100 mL 0.1 mol·L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1 mol·L-1 Ba(OH)2溶液。随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如下图所示。则下列说法中正确的是

A.a点的溶液呈中性
B.b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH— == Al(OH)3↓+2BaSO4↓
C.c点加入Ba(OH)2溶液的体积为200 mL
D.c点溶液呈碱性
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市高三8月月考化学试卷(解析版) 题型:选择题
下列各组离子在相应的条件下一定能大量共存的是
A.在碱性溶液中:HCO3-、K+、C1-、Na+
B.与铝粉反应放出氢气的无色溶液中:NO3-、K+、Na+、SO42-
C.在c(H+)/c(OH-)==1×1013的溶液中:NH4+、Br-、C1-、K+
D.通有SO2的溶液中: Ca2+、C1-、NO3-、A13+
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市三校高三上第一次联考化学试卷(解析版) 题型:选择题
关于某无色溶液中所含离子的鉴别,下列判断正确的是
A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在
B.通入Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在
C.加入Ba(NO3)2,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在
D.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
如图把气体缓慢通过盛有足量试剂的试剂瓶A和试管B,在试管B中不能观察到明显现象的是

选项 | 气体 | A中试剂 | B中试剂 |
A | SO2、CO2 | 酸性KMnO4溶液 | 澄清石灰水 |
B | Cl2、HCl | 饱和NaCl溶液 | KI淀粉溶液 |
C | CO2、HCl | 饱和NaHCO3溶液 | NaAlO2溶液 |
D | NH3、CO2 | 浓硫酸 | 酚酞试液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com