
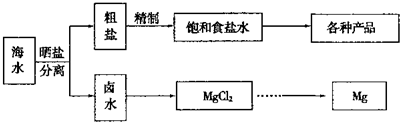
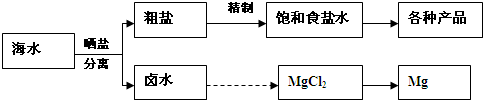
海水中蕴藏着丰富的资源。海水综合利用的流程图如下。

(1)用NaCl做原料可以得到多种产品。
① 工业上由NaCl制备金属钠的化学方程式是_______________________________。
②电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式:____________________________。
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经过下列途径可获得金属镁:
卤水 Mg(OH)2
Mg(OH)2 MgCl2溶液→MgCl2·6H2O→MgCl2
MgCl2溶液→MgCl2·6H2O→MgCl2 Mg
Mg
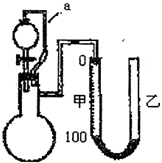
其中,由MgCl2·6H2O制取无水MgCl2的部分装置(铁架台、酒精灯已略)如下:

①上图中,装置a由 、 、双孔塞和导管组成。
②循环物质甲的名称是 。
③制取无水氯化镁必须在氯化氢存在的条件下进行,原因是 。
④装置b中填充的物质可能是 。
(8分)(1) ① 2NaCl(熔融) 2Na+Cl2↑
(1分)
2Na+Cl2↑
(1分)
②NaCl+H2O NaClO+H2↑ (2分) (2)
① 分液漏斗、烧瓶 (2分)
NaClO+H2↑ (2分) (2)
① 分液漏斗、烧瓶 (2分)
② 盐酸 (1分) ③抑制晶体失水过程中的水解 (1分) ④氯化钙(1分)
【解析】
试题分析:(1)①由于钠比较活泼,制取时只能采用电解熔融氯化钠的方法,反应的化学方程式为2NaCl(熔融) 2Na+Cl2↑。
2Na+Cl2↑。
②电解氯化钠溶液在阴极得到氢气,阳极得到氯气,同时还有氢氧化钠。生成的氯气被氢氧化钠溶液尾气吸收生成次氯酸钠即得到“84”消毒液,因此电解氯化钠溶液制取次氯酸钠的化学方程式为NaCl+H2O NaClO+H2↑。
NaClO+H2↑。
(2)①根据装置的结构特点可知,装置a是由分液漏斗、烧瓶、双孔塞和导管组成。
②MgCl2•6H2O在一定条件下加热得到无水MgCl2,若直接加热MgCl2•6H2O,会促进Mg2+水解,得不到无水MgCl2,因Mg2+水解呈酸性,加盐酸或在氯化氢气流中可抑制Mg2+水解,故一定条件为在HCl气流中,目的是抑制Mg2+水解,所以循环物质甲的名称是盐酸。
③根据以上分析可知,制取无水氯化镁必须在氯化氢存在的条件下进行,原因是抑制晶体失水过程中的水解。
④干燥管b中的物质是干燥氯化氢,由于氯化氢是酸性气体,所以b中填充的物质是氯化钙。
考点:考查海水综合应用的有关判断、仪器识别以及金属冶炼等


科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com