
【题目】盐酸阿比朵尔,适合治疗由 A、B 型流感病毒引起的上呼吸道感染,2020 年入选新冠肺炎试用药物,其合成路线:
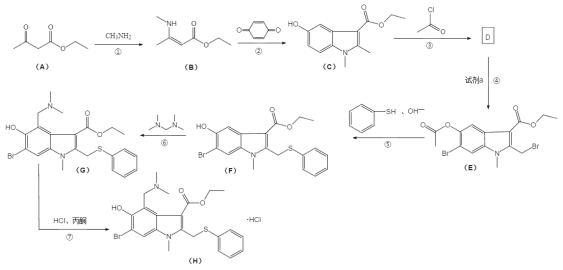
回答下列问题:
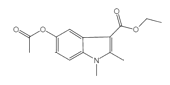
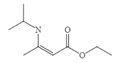
(1)有机物 A 中的官能团名称是______________和______________。
(2)反应③的化学方程式______________。
(3)反应④所需的试剂是______________。
(4)反应⑤和⑥的反应类型分别是______________、______________。
(5)I 是 B 的同分异构体,具有两性并能与碳酸氢钠溶液反应放出气体,写出具有六元 环结构的有机物 H 的结构简式______________。 (不考虑立体异构,只需写出 3 个)
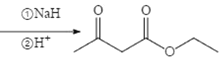
(6)已知:两分子酯在碱的作用下失去一分子醇生成β—羟基酯的反应称为酯缩合反应,也称为 Claisen (克莱森)缩合反应,如: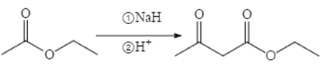 ,设计由乙醇和
,设计由乙醇和![]() 制备
制备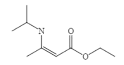 的合成线路______________。(无机试剂任选)
的合成线路______________。(无机试剂任选)
【答案】羰基 酯基 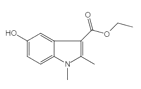 +
+![]() →
→ +HCl Br2 取代反应 取代反应
+HCl Br2 取代反应 取代反应 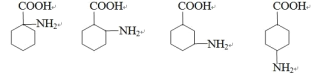 (任写 3 个) CH3CH2OH
(任写 3 个) CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH![]()
![]()
【解析】
根据合成路线图中反应物和生成物的结构变化分析反应类型;根据题给信息及路线图中反应类型比较目标产物及原料的结构设计合成路线图。
(1)根据A的结构简式分析,A中的官能团有羰基和酯基,故答案为:羰基;酯基;
(2)根据比较C和E的结构及反应物![]() 的结构,分析中间产物D的结构简式为:
的结构,分析中间产物D的结构简式为: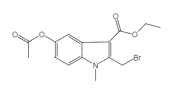 ,则反应③的化学方程式为:
,则反应③的化学方程式为: +
+![]() →
→ +HCl;故答案为:
+HCl;故答案为: +
+![]() →
→ +HCl;
+HCl;
(3)比较D和E的结构,反应④为取代反应,所需的试剂是Br2,故答案为:Br2;
(4)比较E和F的结构变化及F和G的结构变化,反应⑤为取代反应;反应⑥也为取代反应,故答案为:取代反应;取代反应;
(5)I 是 B(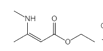 ) 的同分异构体,具有两性并能与碳酸氢钠溶液反应放出气体,则结构中含有氨基和羧基,其中具有六元环结构的有机物H的结构简式有:
) 的同分异构体,具有两性并能与碳酸氢钠溶液反应放出气体,则结构中含有氨基和羧基,其中具有六元环结构的有机物H的结构简式有: ;
;
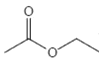
(6)乙醇氧化可以得到乙酸,乙酸与乙醇酯化反应反应得到乙酸乙酯( ),乙酸乙酯发生酯缩合反应生成
),乙酸乙酯发生酯缩合反应生成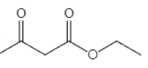 ,
, 与
与![]() 发生合成路线中反应①的反应即可得到
发生合成路线中反应①的反应即可得到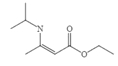 ,故答案为:CH3CH2OH
,故答案为:CH3CH2OH![]() CH3CHO
CH3CHO![]() CH3COOH
CH3COOH![]()


![]()
 。
。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙两U形管各盛有100mL溶液,请回答下列问题:
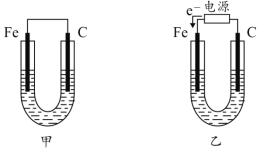
(1)若两池中均为饱和NaCl溶液:
①甲池中铁电极发生_____________腐蚀(填“析氢”或“吸氧”),碳棒上电极反应式__________________________;
②甲池铁棒腐蚀的速率比乙池铁棒_____(填“快”、“慢”或“相等”)。
(2)若乙池中盛CuSO4溶液:
①电解硫酸铜溶液的化学方程式___________________________________;
②乙池反应一段时间后,两极都产生3.36L(标况)气体,该硫酸铜溶液的浓度为___________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是黑棕色晶体,沸点为315℃,有强烈的吸水性,易潮解。某小组同学对无水FeCl3能否分解产生Cl2,进行了如下实验探究。
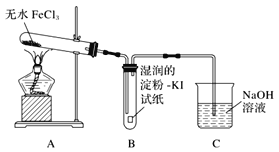
(1)甲同学认为装置B中湿润的淀粉KI试纸变蓝即可证明无水FeCl3能分解产生Cl2,乙同学认为不能得出此结论,理由是_______。
(2)乙同学提出了改进意见,用如图所示装置进行实验:
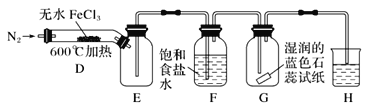
装置H中的试剂为________。装置F中饱和食盐水的作用是________。实验结束后,取装置D中残留固体溶于稀盐酸中,向所得溶液中加入_________(填化学式)溶液,若观察到_____,说明FeCl3已经分解完全。
(3)实验后把镁条投入装置F的溶液中,发生的现象是___,其原因是(结合离子方程式)解释_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中![]() 假设容器体积不变,固体试样体积忽略不计
假设容器体积不变,固体试样体积忽略不计![]() ,使其达到分解平衡:
,使其达到分解平衡:![]() 。实验测得不同温度下的平衡数据列于下表:
。实验测得不同温度下的平衡数据列于下表:
温度 |
|
|
|
|
|
平衡气体总浓度 |
|
|
|
|
|
下列有关叙述正确的是
A.该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变
B.因该反应![]() 、
、![]() ,所以在低温下自发进行
,所以在低温下自发进行
C.达到平衡后,若在恒温下压缩容器体积,体系中气体的浓度增大
D.根据表中数据,计算![]() 时的分解平衡常数约为
时的分解平衡常数约为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx的排放主要来自于汽车尾气,包含 NO2 和 NO I.
(1)用 CH4 催化还原 NOx 可以消除氮氧化物的污染。例如:
a.CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g) H1= -574kJ/mol
b.CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g) H2= -1160kJ/mol
①这两个反应在热力学上趋势均很大,其原因是:______________。
②有利于提高 NOx 的平衡转化率的反应条件是:______________(至少答一条)。
③在相同条件下,CH4(g)+2NO2(g)=N2(g)+2H2O(g)+CO2(g) H2=______________kJ/mol
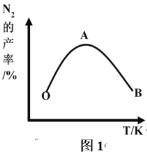
(2)为了提高 CH4 和 NO 转化为 N2 的产率,种学家寻找了一种新型的催化剂。将 CH4 和 NO 按一定比例、一定流速通过装有上述新型催化剂的反应器中,测得 N2 的产率与温度的关系如图1所示,OA 段 N2 产率增大的原因是______________。 AB 段 N2 产率降低的可能原因是______________(填标号)
A. 催化剂活性降低 B. 平衡常数变大 C. 副反应增多
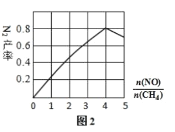
(3)N2 的产率与![]() ,由图可知
,由图可知![]() 最佳约为____________
最佳约为____________
II.有人利用反应 2C(s)+2NO2(g) ![]() N2(g)+2CO2(g) ΔH=-64.2kJ/mol 对 NO2 进行吸附。在 T℃下,向密闭容器中加入足量的 C 和一定量的 NO2 气体,图为不同压强下上述反应经过 相同时间,NO2的转化率随着压强变化的示意图。
N2(g)+2CO2(g) ΔH=-64.2kJ/mol 对 NO2 进行吸附。在 T℃下,向密闭容器中加入足量的 C 和一定量的 NO2 气体,图为不同压强下上述反应经过 相同时间,NO2的转化率随着压强变化的示意图。
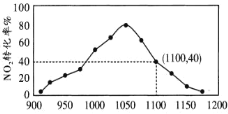
用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 Kp);在 T℃、 1100KPa 时,该反应的化学平衡常数 Kp=______________ (计算表达式表示); 已知:气体分压(P 分)=气体总压(P 总)×体积分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列实验装置说法中正确的是( )
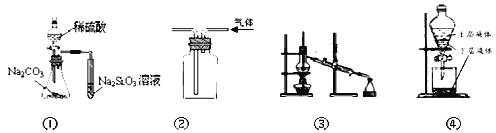
A.用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B.用图②所示实验装置排空气法收集CO2气体
C.用图③将混合液蒸馏分离时,应使温度计水银球浸没在混合液中
D.用图④提取海带中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
⑴4FeO·Cr2O3+8Na2CO3+7O2 ![]() 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
⑵2Na2CrO4+H2SO4![]() Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法中正确的是
A.反应⑴和⑵均为氧化还原反应
B.反应⑴的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成1mol的Na2Cr2O7时共转移7mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界水产养殖协会网介绍了一种利用电化学原理净化鱼池中水质的方法,其装置如图所示。下列说法正确的是
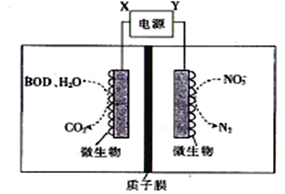
A. X为电源负极
B. 若该装置在高温下进行,则净化效率将降低
C. 若有1molNO3-被还原,则有6molH+通过质子膜迁移至阴极区
D. 若BOD为葡萄糖(C6H12O6),则1mol葡萄糖被完全氧化时,理论上电极流出20 mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业含铬(Ⅵ)污水能污染水源,被人体吸收后易积累而导致器官癌变,必须经无害化处理后才能排放。青岛某污水处理厂的工艺流程如图:
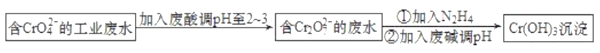
回答下列问题:
(1)CrO42-氧化性较弱,酸性条件下转化为具有较强氧化性的Cr2O72-的离子方程式为__。
(2)已知N2H4与Cr2O72-反应生成无毒气体。若要处理Cr2O72-浓度为0.01mol·L-1的废水1m3,至少需要加入N2H4__kg。
(3)含有SO32-的废水可以代替N2H4处理酸性含铬(Ⅵ)废水,用离子方程式表示其反应原理__。
(4)Cr(OH)3的化学性质与Al(OH)3相似。上述流程中“②加入废碱调pH”时要控制溶液的pH不能过高,原因是__。
(5)含铬(Ⅵ)污水也可用电解法处理。用铁和石墨作电极电解污水,Cr2O72-在阳极区转化为Cr3+,随着电解的进行,溶液pH逐渐增大,Cr3+转化为Cr(OH)3沉淀除去。
①该电解装置中用___作阳极,阳极区除生成Cr(OH)3外还有_沉淀(写化学式)。
②阴极电极反应式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com