
����Ŀ��X��Y��Z��WΪ���ֶ�����Ԫ�ء�Xԭ�������������Ǻ�����Ӳ�����3����Y�������������۵Ĵ�����Ϊ6��Z�ڵؿ��еĺ�������������Y��Z��Wͬ���ڣ�W��������ϼ�Ϊ-2���ش��������⣺
��1��Y-�Ľṹʾ��ͼΪ____________��
��2��д������10�����ӵ�Xԭ�ӵ�ԭ�ӷ���_____________��
��3��Z�������������Zͬ����ĵ���A�ܷ����û���Ӧ�������Ӧ�ڹ�ҵ���ǻ��Z��һ����Ҫ��Ӧ��д���ò���Ӧ�Ļ�ѧ����ʽ�����õ����ŷ��������ת�Ƶķ�������Ŀ________________��
��4����WX2��Һ�м���������NaOH��Һ����Ӧ�����ӷ���ʽΪ___________��
��5��Y����̬�⻯���백���ڿ����������а������ɣ��÷�Ӧ�Ļ�ѧ����ʽΪ_____________��
��6��ZX2��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ_____________________��
���𰸡� 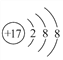 188O
188O 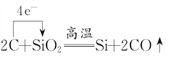 SO2+2OH-====SO32-+H2O HCl+NH3====NH4Cl SiO2+2NaOH====Na2SiO3+H2O
SO2+2OH-====SO32-+H2O HCl+NH3====NH4Cl SiO2+2NaOH====Na2SiO3+H2O
��������X��Y��Z��WΪ���ֶ�����Ԫ����Xԭ�������������Ǻ�����Ӳ�����3����XΪOԪ�أ�Y�������������۵Ĵ�����Ϊ6����Y������������Ϊa���������Ϊ+a�������Ϊa8��a+a8=6��a=7����F�����ۣ���YΪClԪ�أ�Z�ڵؿ��еĺ�������������ZΪSiԪ�أ�Y��Z��Wͬ���ڣ�W��������ϼ�Ϊ-2��˵��W���������6�����ӣ�WΪ�������ڵ�SԪ����
(1). Cl���ĺ˵����Ϊ17�����������Ϊ18����Cl���Ľṹʾ��ͼΪ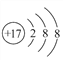 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
(2). ����10�����ӵ�Oԭ�ӵ�������Ϊ8+10=18��ԭ�ӷ���Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ�� ![]() ��
��
(3). ZΪSiԪ�أ�SiO2�뵥��C�ڸ����·�Ӧ���ɵ���Si��CO��SiԪ�صĻ��ϼ۴�+4�۽��͵�0�ۣ�CԪ�صĻ��ϼ۴�0�����ߵ�+2�����õ����ŷ���ʾ����ת�Ʒ������Ŀ��ʽ��Ϊ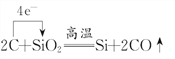 ���ʴ�Ϊ��
���ʴ�Ϊ��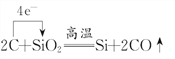 ��
��
(4). SO2��������NaOH ��Һ��Ӧ����Na2SO3��H2O���÷�Ӧ�����ӷ���ʽΪSO2+2OH-=SO32-+H2O���ʴ�Ϊ��SO2+2OH-=SO32-+H2O��
(5). HCl�����백����Ӧ�����Ȼ�粒����������а������ɣ���ѧ����ʽΪHCl+NH3=NH4Cl���ʴ�Ϊ��HCl+NH3=NH4Cl��
(6). SiO2��NaOH��Һ��Ӧ���ɹ����ƺ�ˮ����ѧ����ʽΪSiO2+2NaOH=Na2SiO3+H2O���ʴ�Ϊ��SiO2+2NaOH=Na2SiO3+H2O��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100mL �����Һ�У�HNO3�� H2SO4�����ʵ���Ũ�ȷֱ���0.1mol/L��0.4mol/L��û��Һ�м��� 2.56gͭ�ۣ����ȴ���ַ�Ӧ��������Һ�� Cu2+�����ʵ���Ũ����mol/L ��������Һ������䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ָ������������½���ѧ��ת��Ϊ���ܵ�װ�ã��乤��ԭ����ͼ��ʾ�������й������ص�˵��������ǣ� �� 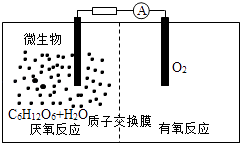
A.������Ӧ����CO2����
B.����ٽ��˷�Ӧ�е��ӵ�ת��
C.����ͨ������Ĥ�Ӹ���������������
D.����ܷ�ӦΪC6H12O6+6O2�T6CO2+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ��Һ�к���Fe(NO3)3��Cu(NO3)2��HNO3�����������������ۣ���Һ��Fe2+��Ũ����������۵����ʵ���֮��Ĺ�ϵ��ͼ��ʾ����ϡ��Һ��Fe(NO3)3��Cu(NO3)2��HNO3�����ʵ���Ũ��֮��Ϊ(����)

A. 1��1��4
B. 1��3��1
C. 3��3��8
D. 1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���������������ͼ������Aԭ��Ϊ�����Ķ��㣬Aλ������Ca��Sr��Ba��Pb����Bλ��V��Cr��Mn��Feʱ�����ֻ�����ĵ�����������ų�����ʱ��֮����ų�����ʱ���ھ�仯���ŵ���ЧӦ����
��1����A��B��O��ʾ�������⾧��Ļ�ѧʽ �� ��ͼ�У���Aԭ����λ����ԭ����ĿΪ ��
��2����̬Crԭ�ӵĺ�������Ų�ʽΪ �� ���е��ӵ��˶�״̬���֣�
��3��ijЩ���������������ܹ���NOֱ�ӷֽ�ΪN2��O2 �� N��O�Ļ�̬ԭ���У�δ�ɶԵĵ�����Ŀ��Ϊ ��
��4���±��Ǽ���̼���ε��ȷֽ��¶Ⱥ������Ӱ뾶
̼���� | CaCO3 | SrCO3 | BaCO3 |
�ȷֽ��¶�/�� | 900 | 1172 | 1360 |
�����Ӱ뾶/pm | 99 | 112 | 135 |
�����̼����ȷֽ��¶���͵�ԭ�� ��
��5���þ����X�������䷨���Բ�ð���٤���������Խ����ƵIJⶨ�õ����½��������Ϊ�����������ܶѻ����߳�Ϊ558pm����֪�Ƶ��ܶ�Ϊ1.54gcm��3 �� ��1cm3�ƾ����к���������������٤������Ϊ����ʽ���㣩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CaCO3������Һ�����ܽ�������ǣ� ��
A.CaCl2��Һ
B.Na2CO3��Һ
C.ϡ����
D.H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬ��ͬѹ���õ������ƿ���ռ���NH3��HCl���壬�ֱ������Ȫʵ�飬װ����ͼ��ʾ����������ƿ�ڳ�����Һ�Ҳ��������ʵ���ɢ��
����˵���������
A. NH3��HCl�ֱ��γ���ɫ����ɫ��Ȫ
B. �Ʊ������NH3��HCl,����ĸ�����ֱ��Ǽ�ʯ�ҡ�Ũ����
C. ����NO2������Ȫʵ������壬������Һ���ʵ����ʵ���Ũ����ǰ���߲�ͬ
D. ��ȥ��װ���еĽ�ͷ�ιܣ���Ϊ��������������ë������Բ����ƿ�����ƿ����Ӷ�������Ȫʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ӱ�컯ѧ��Ӧ���ʵ���Ҫ�����ǣ����¶� ��ѹǿ �۴��� ��Ũ�� �ݷ�Ӧ�ﱾ�������ʣ� ��
A.�٢ڢۢܢ�
B.��
C.�٢�
D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�绯ѧװ�ù���ԭ����ͼ�������й�˵����ȷ���ǣ� �� 
A.����XΪO2
B.c�缫Ϊ�����������ĵ缫��ӦʽΪH2��2e��=2H+
C.һ��ʱ���A��pH����
D.����0.4mol����ת��ʱ����B�������ɱ�״��������2.24L
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com