
【题目】某钙钛型复合氧化物(如图),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物的电阻率在有外磁场作用时较之无外磁场作用时存在巨大变化(巨磁电阻效应).
(1)用A、B、O表示这类特殊晶体的化学式 . 在图中,与A原子配位的氧原子数目为 .
(2)基态Cr原子的核外电子排布式为 , 其中电子的运动状态有种.
(3)某些钙钛型复合氧化物能够催化NO直接分解为N2和O2 , N和O的基态原子中,未成对的电子数目比为 .
(4)下表是几种碳酸盐的热分解温度和阳离子半径
碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 900 | 1172 | 1360 |
阳离子半径/pm | 99 | 112 | 135 |
请解释碳酸钙热分解温度最低的原因: .
(5)用晶体的X射线衍射法可以测得阿伏伽德罗常数.对金属钙的测定得到以下结果:晶胞为面心立方最密堆积,边长为558pm.又知钙的密度为1.54gcm﹣3 , 则1cm3钙晶体中含有个晶胞,阿伏伽德罗常数为(列式计算).
【答案】
(1)ABO3;12
(2)1s22s22p63s23p63d54s1;24
(3)3:2
(4)碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,使碳酸根分解为二氧化碳分子的结果.钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低
(5)5.76×1021;![]()
=6.0×1023
【解析】解:(1)A位于顶点、B位于体心,O位于面心,则晶胞中A的个数为8× ![]() =1,B的个数为1,O的个数为6×
=1,B的个数为1,O的个数为6× ![]() =3,则化学式为ABO3 , 晶胞中与A最近的氧原子位于同一平面内的面心和定点,每个晶胞中有
=3,则化学式为ABO3 , 晶胞中与A最近的氧原子位于同一平面内的面心和定点,每个晶胞中有 ![]() 个O与A距离最近,而A为8个晶胞共有,则与A原子配位的氧原子数目为8×
个O与A距离最近,而A为8个晶胞共有,则与A原子配位的氧原子数目为8× ![]() =12,所以答案是:ABO3;12;(2)Cr元素为24号元素,原子核外有24个电子,所以核外电子排布式为:1s22s22p63s23p63d54s1 , 每个电子的运动状态都不同,则有24种不同的电子,所以答案是:1s22s22p63s23p63d54s1;24;(3)N和O的价电子排布式分别为2s22p3、2s22p4 , 则未成对的电子数目比为3:2,所以答案是:3:2;(4)从表格中得出:这些物质的阴离子是相同的,均为碳酸根,阳离子的半径越大,分解温度越高,由于钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低,所以答案是:碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,使碳酸根分解为二氧化碳分子的结果.钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低;(5)钙的晶胞为面心立方最密堆积,则晶胞中含有Ca的数目为8×
=12,所以答案是:ABO3;12;(2)Cr元素为24号元素,原子核外有24个电子,所以核外电子排布式为:1s22s22p63s23p63d54s1 , 每个电子的运动状态都不同,则有24种不同的电子,所以答案是:1s22s22p63s23p63d54s1;24;(3)N和O的价电子排布式分别为2s22p3、2s22p4 , 则未成对的电子数目比为3:2,所以答案是:3:2;(4)从表格中得出:这些物质的阴离子是相同的,均为碳酸根,阳离子的半径越大,分解温度越高,由于钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低,所以答案是:碳酸盐的热分解是由于晶体中的阳离子结合碳酸根中的氧离子,使碳酸根分解为二氧化碳分子的结果.钙离子由于半径小和氧离子结合更为容易,氧化钙晶格能大,所以碳酸钙分解温度低;(5)钙的晶胞为面心立方最密堆积,则晶胞中含有Ca的数目为8× ![]() +6×
+6× ![]() =4,边长为558pm,则晶胞的体积为(558×10﹣10cm)3=1.74×10﹣22cm3 , 则1cm3钙晶体中含有晶胞的数目为
=4,边长为558pm,则晶胞的体积为(558×10﹣10cm)3=1.74×10﹣22cm3 , 则1cm3钙晶体中含有晶胞的数目为 ![]() ≈5.76×1021 , ρ=
≈5.76×1021 , ρ= ![]() =
= 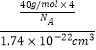 =1.54gcm﹣3 ,
=1.54gcm﹣3 ,
NA= ![]() =6.0×1023 , 所以答案是:5.76×1021;
=6.0×1023 , 所以答案是:5.76×1021; ![]() =6.0×1023 .
=6.0×1023 .


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】将32g铜与100mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2的混合气体标准状况下的体积为11.2L,气体全部逸出后,向溶液中加入VmL n mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的物质的量浓度为 mol/L.(结果须化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于热化学方程式的是( )
A.CaCO3→CaO + CO2-1185kJB.CaCO3(s)→CaO(s)+CO2(g)
C.CaCO3(s) →CaO(s)+CO2(g)-1185kJD.CaCO3→CaO+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的最低负化合价为-2。回答下列问题:
(1)Y-的结构示意图为____________。
(2)写出含有10个中子的X原子的原子符号_____________。
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目________________。
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为___________。
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为_____________。
(6)ZX2与NaOH溶液反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( ) 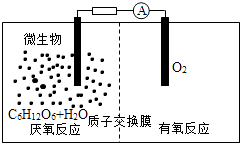
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2═6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某校实验小组设计的一套原电池装置,下列有关描述不正确的是( ) 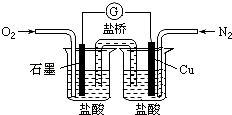
A.此装置能将化学能转变为电能
B.石墨电极的反应式:O2+2H2O+4e﹣=4OH﹣
C.电子由Cu电极经导线流向石墨电极
D.电池总的反应是:2Cu+O2+4HCl=2CuCl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分离的说法合理的是( )
A.分离I2和KMnO4两种固体时,可选择加热使I2升华的方法
B.除去AgI胶体中的NaI时,可将其装在用半透膜做的袋子里,放在流动的蒸馏水中,该分离方法称为渗析
C.粗盐水中含有Ca2+、Mg2+、Fe3+、SO ![]() 等离子,可以通过化学沉淀法除去.如:可以通过加入Ba(NO3)2的方法除去其中的SO
等离子,可以通过化学沉淀法除去.如:可以通过加入Ba(NO3)2的方法除去其中的SO ![]()
D.从海带中提取碘单质时,可以将其灼烧后加水溶解过滤,在滤液中加适量氯水将碘元素氧化为I2 , 最后用乙醇萃取出单质碘
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com