
����Ŀ�������£������йش�����Һ������������ȷ����
A.pH��5.6��CH3COOH��CH3COONa�����Һ�У�c(Na+)��c(CH3COO��)
B.Ũ�Ⱦ�Ϊ0.1 mol��L��1��CH3COOH��CH3COONa��Һ�������Ϻ�c(CH3COO��)��c(CH3COOH)��2[c(H+)��c(OH��)]
C.��pH��a�Ĵ���ϡ��ΪpH��a+1�Ĺ����У�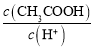 ����
����
D.�����pH��a�Ĵ�����pH��b��NaOH��Һǡ���к�ʱ��a+b��14
���𰸡�CD
��������
A����Һ�д��ڵ���غ�c(CH3COO��)+ c(OH��)= c(Na+)+ c(H+)����Һ�����ԣ�����c(OH��)��c(H+)������c(Na+)��c(CH3COO��)����A��ȷ��
B����Һ�д��ڵ���غ�c(CH3COO��)+c(OH��)= c(Na+)+ c(H+)�����������غ�c(CH3COO��)+c(CH3COOH)=2c(Na+)�����������ɵ�c(CH3COO��)��c(CH3COOH)��2[c(H+)��c(OH��)]����B��ȷ��
C������ĵ���ƽ�ⳣ������ʽKa=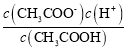 ������
������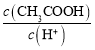 =
=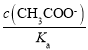 ��ϡ������c(CH3COO��)��С��Ka���䣬����
��ϡ������c(CH3COO��)��С��Ka���䣬����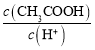 ��С����C����
������C����
D�������£������pH=a�Ĵ�����pH=b��NaOH��Һǡ���к�ʱ������ͼ�����ʵ���Ũ����ȣ������ĵ���̶�Ϊ������c(CH3COOH)=![]() =
=![]() mol/L=10 b-14mol/L(0������1)��������=1014-a-b(0������1)����a+b��14����D����
mol/L=10 b-14mol/L(0������1)��������=1014-a-b(0������1)����a+b��14����D����
�ʴ�ΪCD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǵ����Ϻ����ḻ��һ��Ԫ�أ���Ԫ�صĵ��ʼ��仯�����ڹ�ũҵ������������������Ҫ���á�
��1���������������仯ʾ��ͼ����д��![]() ��CO��Ӧ���Ȼ�ѧ����ʽ______��
��CO��Ӧ���Ȼ�ѧ����ʽ______��

��2���ڹ̶�������ܱ������У��������»�ѧ��Ӧ�� ![]()
![]() H<0����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
H<0����ƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
T/K | 298 | 398 | 498 |
ƽ�ⳣ��K |
|
|
|
�����ж�![]() ______
______![]() ����д>��=��<��
����д>��=��<��
�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬����_______������ĸ��
a. ������![]() ��
��![]() ��
��![]() ��Ũ��֮��Ϊ1��3��2
��Ũ��֮��Ϊ1��3��2
b. ![]()
c. ������ѹǿ���ֲ���
d. ���������ܶȱ��ֲ���
��3���Է�Ӧ![]()
![]() H>0�����¶ȷֱ�Ϊ
H>0�����¶ȷֱ�Ϊ![]() ��
��![]() ʱ��ƽ����ϵ��
ʱ��ƽ����ϵ��![]() �����������ѹǿ�仯��������ͼ��ʾ��
�����������ѹǿ�仯��������ͼ��ʾ��

��A��C����ķ�Ӧ���ʣ�A_________C����>��=��<��
��A��C����![]() ��ת���ʣ�A_________C����>��=��<��
��ת���ʣ�A_________C����>��=��<��
����״̬B��״̬A�����Բ��õķ�����__________��
��4��һ���¶���
������1L���ܱ������У�����1 mol![]() ��3 mol
��3 mol![]() ������Ӧ����ά���ݻ��㶨��10min�ﵽƽ��ʱ������������ʵ���Ϊԭ����7/8����
������Ӧ����ά���ݻ��㶨��10min�ﵽƽ��ʱ������������ʵ���Ϊԭ����7/8����![]() ��ת����a��
��ת����a��![]() ��=______����
��=______����![]() ��ʾ�ù��̵ķ�Ӧ����v��
��ʾ�ù��̵ķ�Ӧ����v��![]() ��=_________.
��=_________.
������1L���ܱ������У�����2mol![]() ��6mol
��6mol![]() ������Ӧ����ά��ѹǿ�㶨���ﵽƽ��ʱ��
������Ӧ����ά��ѹǿ�㶨���ﵽƽ��ʱ�� ![]() ƽ��Ũ�ȱȢ���
ƽ��Ũ�ȱȢ���![]() ƽ��Ũ�ȵ�2��________������>��=��<��
ƽ��Ũ�ȵ�2��________������>��=��<��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����( )
A.1mol/L��![]() ��Һ�к�
��Һ�к�![]() ����ĿΪ2NA
����ĿΪ2NA
B.��״���£�4.48L ![]() ������ԭ����ĿΪ0.2NA
������ԭ����ĿΪ0.2NA
C.���³�ѹ�£�28g ![]() ������������ĿΪNA
������������ĿΪNA
D.1mol Al������������ȫ��Ӧ��ת�Ƶ�����ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��� ���������⣺
��1������ʽ![]() ��ϵͳ����Ϊ____________��
��ϵͳ����Ϊ____________��
��2��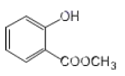 �к��й����ŵ�����Ϊ____________��
�к��й����ŵ�����Ϊ____________��
��3��2������1����ϩ�Ľṹ��ʽ____________��
��4����Է�������Ϊ72��һ�ȴ���ֻ��һ�ֵ������Ľṹ��ʽ____________��
��5�� �����ʽΪ____________��
�����ʽΪ____________��
��6��д��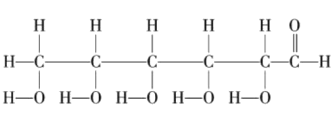 �����������ŵĵ���ʽ��____________��____________��
�����������ŵĵ���ʽ��____________��____________��
��7������ʽΪC2H6O���л��������ͬ���칹�壬�Ҵ�(CH3CH2OH)������(CH3OCH3)����ͨ�����з����������ܽ���������������____________��
A.������� B.�˴Ź������� C.Ԫ�ط����� D.���Ʒ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ��������������� ��
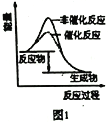


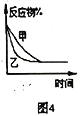
A. ͼ1��ʾ�ֱ����С������������ij���ȷ�Ӧ�����е������仯
B. ͼ2��ʾ�����£�����п���������ĵ�Ũ�ȵ����ᷴӦ(�μ�CuSO4��Һ��Ϊ����)
C. ͼ3��ʾmg�������ˮϡ��������Һ���������ı仯�����д���ĵ����c>b>a
D. ͼ4��ѹǿ�Ժϳɰ���Ӧ��Ӱ�죬�ҵ�ѹǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ͭ��Ũ���ᷴӦ��ʵ��װ��ͼ��

(1)�����ٵ�������_____________��
(2)ʵ������У��Թܢ��з���������Ϊ____________________________________��
(3)�Թܢ���ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ _______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��¡����ݵ��ܱ������н��з�Ӧ A��g���TB��g��+C��g��������Ӧ���Ũ����2molL-1 ���� 0.8molL-1 ��Ҫ 20s����ô��Ӧ��Ũ������ 0.8molL-1 ���� 0.2molL-1 ����Ҫ��ʱ��Ϊ
A.10sB.���� 10sC.С�� 10sD.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯��![]() ����������Ԫ����
����������Ԫ����![]() �ۣ�NaH��ˮ��Ӧ�ų�
�ۣ�NaH��ˮ��Ӧ�ų�![]() ������������ȷ����( )
������������ȷ����( )
A.��NaH�е������Ӱ뾶������Ӱ뾶��
B.��NaH�е������ӵĵ��Ӳ��Ų���![]() ����ͬ
����ͬ
C.NaH��ˮ��Ӧ����Һ������
D.NaH�е������ӱ���ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��830 Kʱ�����ܱ������з������п��淴Ӧ: CO(g)+H2O(g) ![]() CO2(g)+H2(g)����H<0 ����ش���������:
CO2(g)+H2(g)����H<0 ����ش���������:
��1������ʼʱc(CO) =2 mol��L-1��c(H2O) =3 mol��L-1��4 s��ﵽƽ�⣬��ʱCO��ת����Ϊ60%�����ڸ��¶��£��÷�Ӧ��ƽ�ⳣ��K=____����H2O��ʾ�Ļ�ѧ��Ӧ����Ϊ_____��
��2������ͬ�¶��£�����ʼʱc(CO) =1 mol��L-1��c(H2O) =2 mol��L-1����Ӧ����һ��ʱ����H2��Ũ��Ϊ0.5 mol��L-1����ʱv(��)______ v(��) (������������С��������������)��
��3���������¶ȣ��÷�Ӧ��Kֵ����Ϊ______��
a.1 b.2 c.0.5
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com