


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���þƾ�����ȡ����ȡ��ˮ�еĵ� |
| B���÷�Һ�ķ�������������Ȼ�̼ |
| C��������ķ�����ȥˮ�е�Na+���� |
| D���ù��˵ķ�����ȥˮ�е���ɳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������������Һ֮����кͷ�Ӧ | ||||
B��CO2+C
| ||||
C������þȼ�գ�2Mg+O2
| ||||
| D����ʯ������ˮ��CaO+H2O=Ca��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
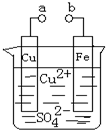
| A��a��b������ʱ����Ƭ�ϻ��н���ͭ���� |
| B��a��b�õ�������ʱ����Һ�е�SO42-�����缫�ƶ���ͭƬ�Ϸ����ķ�ӦΪ��Cu2++2e-=Cu |
| C������a��b�Ƿ����ӣ���Ƭ�����ܽ⣬��Һ����ɫ���dz��ɫ |
| D��a��b�ֱ�����ֱ����Դ������������Һ�е�Cu2+��ͭ�缫�ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
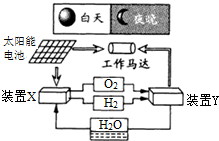
| A����ϵͳ��ֻ����3����ʽ������ת�� |
| B��װ��Y�е���ת��Ϊ��ѧ�� |
| C��װ��X��ʵ��ȼ�ϵ�ص�ȼ�Ϻ����������� |
| D��װ��X��Y�γɵ���ϵͳ��ʵ�����ʵ����ŷţ�����ʵ�ֻ�ѧ������ܼ����ȫת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ϡ������0.1 mol/LNaOH��Һ��Ӧ��H+��aq��+OH-��aq��=H2O��l����H=-57.3 kJ?mol-1 |
| B����101KPa�������ı�ȼ���ȡ�H=-285.5 kJ?mol-1����ˮ�ֽ���Ȼ�ѧ����ʽ 2H2O��l��=2H2��g��+O2��g����H=+285.5 kJ?mol-1 |
| C���ܱ������У�9.6 g�����11.2 g���ۻ�ϼ�������������17.6 gʱ���ų�19.12 kJ������ ��Fe��s��+S��s��=FeS��s����H=-95.6 kJ?mol-1 |
| D����֪2C��s��+O2��g��=2CO��g����H=-221 kJ?mol-1�����֪C�ı�ȼ����Ϊ110.5 kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��1��1 |
| B��6��3��2 |
| C��3��2��1 |
| D��9��3��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com