
【题目】恒温、容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示[已知:2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJ/mol]. 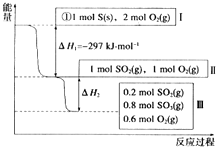
请回答下列问题:
①写出能表示硫的燃烧热的热化学方程式: .
②△H2= kJ/mol.
③在相同条件下,充入1mol SO3和0.5mol O2 , 则达到平衡时SO3的转化率为;此时该反应(填“放出”或“吸收”) kJ的能量.
【答案】S(s)+O2(g)═SO2(g)△H=﹣297KJ?mol﹣1;﹣78.64;20%;吸收;19.66
【解析】解:(1)燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物放出的热量,所以,硫的物质的量为1mol.由图1可知1molS(s)完全燃烧放出的热量为297KJ,所以,硫的燃烧热的热化学方程式S(s)+O2(g)═SO2(g)△H=﹣297 KJmol﹣1,
所以答案是:S(s)+O2(g)═SO2(g)△H=﹣297 KJmol﹣1;(2)由由图1可知,参加反应的n(SO2)=1mol﹣0.2mol=0.8mol,根据热化学方程式:2SO2(g)+O2(g)2SO3(g)△H=﹣196.6KJmol﹣1;可知,△H2=0.4△H=0.4×(=﹣196.6KJmol﹣1)=﹣78.64KJmol﹣1.
所以答案是:﹣78.64KJmol﹣1;(3)根据图象所给的信息可知,反应2SO2(g)+O2(g)2SO3(g)的平衡常数K= ![]() =
= ![]() =
= ![]() ,在相同条件下,充入1molSO3和0.5molO2,设反应达到平衡时SO3转化了Xmol,则有:
,在相同条件下,充入1molSO3和0.5molO2,设反应达到平衡时SO3转化了Xmol,则有:
2SO2(g)+ | O2(g) | 2SO3(g) | |
起始(mol/L) | 0 | 0.5 | 1 |
转化(mol/L) | x | 0.5x | x |
平衡(mol/L) | x | 0.5+0.5x | 1﹣x |
根据温度不变,平衡常数K的值不变可知:K= ![]() =
= ![]() ,解得:X=0.2mol,
,解得:X=0.2mol,
故反应达到平衡时SO3的转化率为 ![]() ×100%=20%.
×100%=20%.
由热化学方程式2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1可知,2SO3(g)2SO2(g)+O2(g)△H=﹣196.6kJmol﹣1即1molSO3分解吸收98.3KJ的热量,则0.2molSO3分解吸收的热量Q=98.3KJ×0.2=19.66KJ.
所以答案是:20%;吸收;19.66.
【考点精析】认真审题,首先需要了解化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%).


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.在一定条件下,苯分别与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
B.己烷有4种同分异构体,它们的熔点、沸点各不相同
C.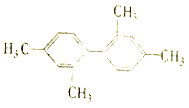 分子中至少有11个碳原子处于同一平面
分子中至少有11个碳原子处于同一平面
D.聚合物 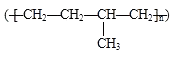 可由单体CH3CH=CH2和CH2=CH2加聚制得
可由单体CH3CH=CH2和CH2=CH2加聚制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物I是重要有机中间体,其合成路线(部分反应条件已略去)如下图所示:

已知:
R — CN![]() R — COOH
R — COOH
回答下列问题:
(1)A的结构简式是______________。
(2)B中含有的官能团是______________。
(3)D是一种合成高分子,它的结构简式是______________。
(4)I发生缩聚反应的化学方程式是______________。
(5)G→H的反应类型是______________。
(6)E→F反应的化学方程式是______________。
(7)下列说法正确的是________。
①物质I能发生消去反应
②F→G过程产生的副产物 物质G互为同分异构体
物质G互为同分异构体
③B、D均存在顺反异构
(8)结合题给信息,以乙烯、HBr为起始原料制备丙酸,设计合成路线(其他试剂任选)________。(合成路线常用的表示方式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸的消费量是衡量一个国家化工生产水平的重要标志。在硫酸的生产中,最关键的一步反应为2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
(1)一定条件下,SO2与O2反应10min后,若SO2和SO3的物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为____________________;10min内生成SO3的平均反应速率v(SO3)为____。
(2)下列关于该反应的说法正确的是_________(填选项字母)。
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
(3)在反应过程中,若某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1 mol/L、0.2mol/L。当反应达到平衡时,可能存在的数据是___________(填选项字母)。
A.O2为0.2mol/L B. SO2为0.25mol/L
C.SO3为0.4mol/L D. SO2、SO3均为0.15mol/L
(4)FeS2焙烧产生的SO2可用于制硫酸。已知25℃、101KPa时:
2 SO2(g)+ O2(g)2SO3(g)△H1=-197kJmol-1;
H2O(g)═H2O(l)△H2=-44kJmol-1;
2SO2(g)+O2(g)+2H2O(g)═2H2SO4(l)△H3=-545kJmol-1
则SO3(g)与H2O(l)反应生成H2SO4(l)的热化学方程式是____________________。
(5)工业制硫酸,用过量的氨水对SO2进行尾气处理,该反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图所示装置进行实验,并回答下列问题:

(1)判断装置A和B的能量转化形式:A池为______________,B池为_________________。
(2)锌电极发生 _________反应;铜极发生__________________________反应;石墨棒C1为____极,电极反应式为_________;石墨棒C2附近发生的实验现象___________。
(3)当C2极析出44.8 L气体(标准状况下),锌的质量变化为(增加或减少)________g。CuSO4溶液的质量变化为(增加或减少)________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源,海水综合利用的流程图如图1: 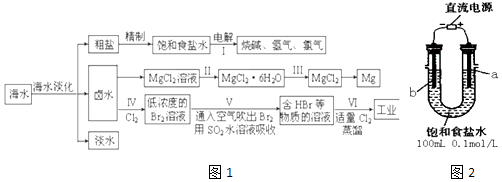
(一)某化学研究小组用图装置2模拟步骤I电解食盐水 (用铁和石墨做电极).
(1)a电极材料是(填铁、石墨),其电极反应式为 .
(2)当阴极产生11.2mL气体时(标准状况),该溶液的pH为(忽略反应前后溶液体积的变化). (二)卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+ . 表是生成氢氧化物沉淀的pH:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
(3)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+ , 最适宜选用的物质是(填序号,下同),加入调节溶液的pH,充分反应后过滤,可得MgCl2溶液. a.KMnO4 b.H2O2 c.MgO d.NaOH
(4)步骤Ⅲ由MgCl2H2O获得MgCl2的操作是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是生产硝酸、尿素等物质的重要原料。
(1)氨催化氧化法是工业制硝酸的主要方法。已知:
2NO(g)+3H2(g) ![]() 2NH3(g)+02(g) △H1=-272.9kJ/mol
2NH3(g)+02(g) △H1=-272.9kJ/mol
2H2(g)+02(g)![]() 2H2O(g) △H2=-483.6kJ/mol
2H2O(g) △H2=-483.6kJ/mol
则4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H3=__________
4NO(g)+6H2O(g) △H3=__________
(2)恒容密闭容器中进行合成知反应:N2(g)+3H2(g)![]() 2NH3(g) △H4==-92.4kJ/mol,其化学平衡常数(K)与温度的关系如下表:
2NH3(g) △H4==-92.4kJ/mol,其化学平衡常数(K)与温度的关系如下表:
温度/K | 298 | 398 | 498 | … |
平衡常数(K) | 4.1×106 | K1 | K2 | … |
K1____K2(填“>”或“<”),其判断理由是_____________。
(3)向氨合成塔中充入10molN2和40molH2合成氨,一定温度(T)下平衡混合物中氨气的体积分数与压强(p)的关系如图1所示。

①下列说法正确的是______(填字母)。
A.由图1可知增大体系压强(p)有利于增大氨气在混合气体中的体积分数
B.若图1中T=500℃,则温度为450℃时对应的曲线是b
C.工业上采用500℃温度的主要目的是提高氮气的转化率
D.当3v正(H2)=2v逆(NH3)时,反应达到平衡状态
②当温度为T、氨气的体积分数为25%时,N2的转化率为__________。
(4)工业上用NH3生产硝酸时,将NH3和O2按体积比1:2混合通入某特定条件的密闭容器中进行反应,所有物质不与外界交换,最后得到溶液中溶质的质量分数为_______。
(5)氮碳比[![]() ]对合成尿素的反应:2NH3(g)+CO2(g)
]对合成尿素的反应:2NH3(g)+CO2(g)![]() CO(NH2)2(g)+H2O(g)有影响。T℃时,在2L的恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2成NH3的转化率,c表示平衡体系中尿素的体积分数,当
CO(NH2)2(g)+H2O(g)有影响。T℃时,在2L的恒容密闭容器中,将物质的量之和为3mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2成NH3的转化率,c表示平衡体系中尿素的体积分数,当![]() =_______时,尿素的产量最大,该条件下反应的平衡常数K=________。
=_______时,尿素的产量最大,该条件下反应的平衡常数K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列各图曲线表征的信息,得出的结论不正确的是


A. 图1表示常温下向体积为10 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-)
B. 图2表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a
C. 图3表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ·mol-1
D. 由图4得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com