
【题目】铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体在不同温度下转化的图示。下列有关说法中正确的是
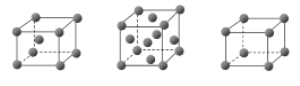
δ-Fe![]() γ-Fe
γ-Fe![]() α-Fe
α-Fe
A.δ、γ、α三种晶体互为同分异构体
B.γ-Fe晶体为面心立方体紧密堆积
C.α-Fe晶体与每个Fe原子距离相等且最近的Fe原子有8个
D.将Fe加热到1500℃分别急速冷却和缓慢冷却,得到的晶体类型相同
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】某温度下,在一个1L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

(1)从开始至2min,X的平均反应速率为__________;
(2)该反应的化学方程式为_______________________;
(3)1min时,正逆反应速率的大小关系为:v(正)_____v(逆),2min时,v(正)_____v(逆)。(填“>”或“<”或“=”)
(4)若X、Y、Z均为气体,在2min时,向容器中通入氩气,增大体系压强,X的化学反应速率将______,若加入适合的催化剂,Y的化学反应速率将______。(填“变大”或“不变”或“变小”)
(5)若X、Y、Z均为气体,下列能说明反应已达平衡的是_____________。
a.X、Y、Z三种气体的浓度相等
b.气体混合物物质的量不再改变
c.反应已经停止
d.反应速率v(X)︰v(Y)=2:1
e.(单位时间内消耗X的物质的量):(单位时间内消耗Z的物质的量)=3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A.天然油脂都是混合物,没有恒定的熔点和沸点
B.用饱和Na2CO3溶液可以除去乙酸乙酯中的乙酸
C.![]() 的名称为2-乙基丙烷
的名称为2-乙基丙烷
D.有机物![]() 分子中所有碳原子不可能在同一个平面上
分子中所有碳原子不可能在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B.[实验化学]
丙炔酸甲酯(![]() )是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
![]()
实验步骤如下:
步骤1:在反应瓶中,加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置见下图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。

(1)步骤1中,加入过量甲醇的目的是________。
(2)步骤2中,上图所示的装置中仪器A的名称是______;蒸馏烧瓶中加入碎瓷片的目的是______。
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是____;分离出有机相的操作名称为____。
(4)步骤4中,蒸馏时不能用水浴加热的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可再生能源是我国重要的能源资源,在满足能源需求、改变能源结构、减少环境污染、促进经济发展等方面具有重要作用。应用太阳能光伏发电技术是实现节能减排的一项重要措施。下列有关分析不正确的是( )
A.风能、太阳能等属于可再生能源
B.推广可再生能源有利于经济可持续发展
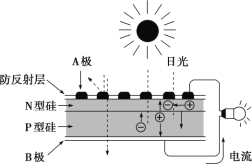
C.如图是太阳能光伏电池原理图,图中 A 极为正极
D.光伏电池能量转化方式是太阳能直接转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓(GaAs)灯泡寿命是普通灯泡的100倍,而耗能即为10%,推广砷化镓(GaAs)、 氮化镓(GaN)等发光二极管(LED)照明,是节能减排的有效举措。请回答下列问题:
(1)基态N原子核外电子排布图为 _____________________ ;Ga与Al同主族,且位于Al的下一周期,则基态Ga原子的价电子排布式为 ________________。
(2)Ga的电负性比As______(填“大”或“小”);Ga逐级失去电子的电离能 (单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知Ga的主要化合价为__和+3。
(3)比较下列Ga的卤化物的熔点和沸点, GaCl3、GaBr3、GaI3的熔、沸点依次升高, 分析其变化的原因是:_____________________________________________________。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3的熔点超过1000℃,可能的原因是____________________________。
(4)GaAs是将(CH3)3Ga和AsH3用金属有机物化学气相淀积方法制备得到,该反应在700℃下进行
①则该反应的化学方程式为:____________________________________________。
②反应物AsH3分子的几何构型为________________,(CH3)3Ga中镓原子杂化方式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的基态原子的核外电子有3种能量状态、5种空间状态,X是其中第一电离能最小的元素;元素Y的M层电子运动状态与X的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。
(1)X基态原子的电子排布式为___________。
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是___________。
(3)在Y的氢化物(H2Y分子中,Y原子轨道的杂化类型是___________。
(4)Y与X可形成YX32-。
①YX32-的立体构型为___________(用文字描述)。
②写出一种与YX32-互为等电子体的分子的化学式___________。
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4(H2O)2]Cl2,该配合物加热时,首先失去配离子中的配体是___________(写化学式)。

(6)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为___________。其晶胞边长为540.0pm,密度为___________g·cm-3(列式并计算),a位置Y与b位置Z之间的距离为___________pm(列式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C6H6O)是一种重要的化工原料,广泛用于制造树脂、医药等。
Ⅰ.以A、B为原料合成扁桃酸衍生F的路线如下。
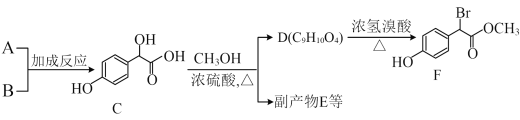
(1)A的名称是____;B的结构简式是____。
(2)C(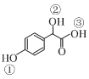 )中①~③羟基氢原子的活性由强到弱的顺序是____。
)中①~③羟基氢原子的活性由强到弱的顺序是____。
(3)D的结构简式是____。
(4)写出F与过量NaOH溶液反应的化学方程式:___________。
(5)若E分子中含有3个六元环,则E的结构简式是________。
Ⅱ.以A为原料合成重要的医药中间体K的路线如下。
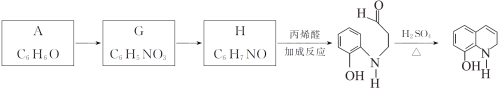
(6)G→H的反应类型是__________。
(7)一定条件下,K与G反应生成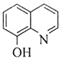 、H和水,化学方程式是__________。
、H和水,化学方程式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下8种化合物中,不能通过化合反应直接生成的有
①Fe3O4 ②Fe(OH)3 ③FeCl2 ④Cu2(OH)2CO3 ⑤Al(OH)3 ⑥Na2CO3 ⑦NaHCO3 ⑧Na2O2
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com