
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
(1)300℃时,该反应的平衡常数表达式为K=______________,已知K300℃<K350℃,则ΔH____0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”)。
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】下列分离或提纯物质的方法正确的是( )
A.用蒸馏的方法制取蒸馏水
B.用过滤的方法除去NaCl溶液中含有的少量淀粉胶体
C.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
D.用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜矿石又叫孔雀石。已知碱式碳酸铜粉末不溶于水和醇,用CuSO4溶液与Na2CO3溶液反应可以得到碱式碳酸铜,为了探究该反应得到的碱式碳酸铜的化学式,某班同学设计了如下实验:
【碱式碳酸铜的制备】
称取12.5g胆矾,研细,滴加4滴稀硫酸,溶于适量蒸馏水中,充分搅拌后得到CuSO4溶液。向其中加入适量Na2CO3溶液,充分振荡,将所得蓝绿色悬浊液静置后过滤,依次用蒸馏水、无水乙醇洗涤所得蓝绿色固体,最后低温烘干备用。
(1)配制CuSO4溶液时,滴加稀硫酸的作用是__________________________________。
(2)用无水乙醇洗涤蓝绿色固体的目的是_____________________________________。
【实验探究】
同学们设计了如下装置,用制得的蓝绿色固体进行实验。
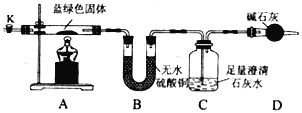
请按要求答下列问题:
(3)检查完该装置的气密性,装入药品后,实验开始前需通入一段时间气体N2,然后关闭弹簧夹K,再点燃A处酒精灯加热,控制C中导管均匀地产生气泡。通入N2的作用是____________,N2的电子式为____________。
(4)点燃A处酒精灯后,能观察到的现象是_________________________________。
(5)装置C中所发生反应的离子方程式为_____________________________________。
(6)同学们查阅文献得知:Ksp[CaCO3]=2.8×10-9,Ksp[BaCO3]=5.1×10-9,经讨论认为用Ba(OH)2代替Ca(OH)2来定量测定蓝绿色固体的化学式会更好,其原因是_________________(选填下列字母代号)。
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2,能充分吸收 CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3,测量误差小
(7)若蓝绿色固体的组成为xCuCO3·yCu(OH)2。取干燥后的蓝绿色固体10.84g,煅烧至完全分解后得到8.00g固体及1.08gH2O。则该蓝绿色固体的化学式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系如下图所示(反应条件均已略去)。 请回答下列问题:

(1)D的化学式为_______________ 。
(2)反应③的离子方程式为________________________ 。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. s能级的能量一定比p能级低 B. 电子云图中小黑点多的区域表示电子多
C. 3p2表示第三能层上有两个电子 D. 同一原子中,2p、3p、4p能级的轨道数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.葡萄糖、果糖和蔗糖都能发生水解反应
B.糖类、油脂、蛋白质都是由C、H、O三种元素组成的
C.糖类、油脂、蛋白质都是高分子化合物
D.油脂有油和脂肪之分,但都属于酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究物质制备是化学学科的任务之一。
(1)请从Cl2、H2、CO2、NO、NH3五种气体中选择一种气体,该气体在实验室可用如图装置制取、净化、收集(可以含水蒸气),制取该气体的化学方程式为____________。

(2)已知: +4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O,可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点分别为9.79℃、131.4 ℃,不溶于水);试管d中装有液溴(表面覆盖少量水)。
+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O,可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点分别为9.79℃、131.4 ℃,不溶于水);试管d中装有液溴(表面覆盖少量水)。

①e装置的作用是_________;当观察到_________现象时,试管d中反应基本结束;
②若用冰水代替烧杯中的冷水,可能引起的不安全后果是_________;
③实验后,需通过水洗、________、水洗、用干燥剂干燥、蒸馏等操作对试管d中的粗产品进行精制:
④实验消耗40%乙烯利(摩尔质量为M)溶液50g,制得产品m g,则乙烯利合成1,2-二溴乙烷的产率为____________(用含M、m的代数式表示);
⑤设计实验证明,反应后烧瓶中的混合溶液含有C1-、PO43-。简述实验方案:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物的用途非常广泛,回答下列问题:
(1)基态铜原子有种不同运动状态的电子,二价铜离子的电子排布式为________。
(2)铜能与类卤素(CN)2反应生成Cu(CN)2 1mol(CN)2分子中含有π键的数目为___________。
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),结构如图所示,
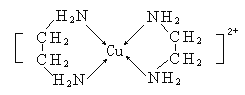
则Cu2+的配位数为_________,该配离子中所含的非金属元素的电负性由大到小的顺序是________;乙二胺分子中氮原子轨道的杂化类型为______,乙二胺和三甲胺[N(CH3)3]均属于胺,但相对分子质量相近,但乙二胺比三甲胺的沸点高的多,原因是__________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子数目为________。
(5)某M原子的外围电子排布是为3s23p5,铜与M形成化合物的晶胞如图所示(黑球代表铜原子)。
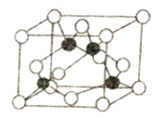
①已知铜和M的电负性分别为1.9和3.0,则铜与M形成的该种化合物属于________ (填“离子”或“共价”)化合物。
②已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为______pm(只写计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com