
����Ŀ���о������Ʊ��ǻ�ѧѧ�Ƶ�����֮һ��
��1�����Cl2��H2��CO2��NO��NH3����������ѡ��һ�����壬��������ʵ���ҿ�����ͼװ����ȡ���������ռ�(���Ժ�ˮ����)����ȡ������Ļ�ѧ����ʽΪ____________��

��2����֪�� +4NaOH��NaCl+CH2=CH2��+Na3PO4+3H2O����������װ����ȡ1��2-��������(��ɫҺ�壬�ܶ�2.18g��cm-3���ۡ��е�ֱ�Ϊ9.79�桢131.4 ����������ˮ)���Թ�d��װ��Һ��(���渲������ˮ)��
+4NaOH��NaCl+CH2=CH2��+Na3PO4+3H2O����������װ����ȡ1��2-��������(��ɫҺ�壬�ܶ�2.18g��cm-3���ۡ��е�ֱ�Ϊ9.79�桢131.4 ����������ˮ)���Թ�d��װ��Һ��(���渲������ˮ)��

��eװ�õ�������_________�����۲쵽_________����ʱ���Թ�d�з�Ӧ����������
�����ñ�ˮ�����ձ��е���ˮ����������IJ���ȫ�����_________��
��ʵ�����ͨ��ˮϴ��________��ˮϴ���ø�����������Ȳ������Թ�d�еĴֲ�Ʒ���о��ƣ�
��ʵ������40����ϩ��(Ħ������ΪM)��Һ50g���Ƶò�Ʒm g������ϩ���ϳ�1��2-��������IJ���Ϊ____________(�ú�M��m�Ĵ���ʽ��ʾ)��
�����ʵ��֤������Ӧ����ƿ�еĻ����Һ����C1-��PO43-������ʵ�鷽����_____________________________��
���𰸡� CaCO3+2HCl=CaCl2+CO2��+H2O ���������� �Թ�����Һ��Ϊ��ɫ �Թ�d�г����ܶ��� ��ϡNaOH��Һϴ ![]() ȡ���������Һ�����������Ba(NO3)2��Һ,������ɫ����,֤����Һ�д���PO43-������ȡ�����ϲ���Һ���Թ������������ϡ�����AgNO3��Һ,������ɫ������֤����Һ�д���Cl-
ȡ���������Һ�����������Ba(NO3)2��Һ,������ɫ����,֤����Һ�д���PO43-������ȡ�����ϲ���Һ���Թ������������ϡ�����AgNO3��Һ,������ɫ������֤����Һ�д���Cl-
����������1������ͼ�е�װ�ÿ�֪�����������ȡʹ�ò�����������װ�ã�����ʹ�������ſ����ռ�����֪��������ܶȱȿ�����H2��NH3���ܶȱȿ���С�����������ſ���������ȡCl2Ҫ���ȣ�NO�������ſ������ռ�������ֻ����CO2�����Է�Ӧ�ķ���ʽΪ��CaCO3+2HCl=CaCl2+CO2��+H2O��
��2�������ж�����Ҫʹ��β������װ�ã�����������Һ�ܹ����巴Ӧ������d�������������ջӷ�������������ֹ��Ⱦ���������۲쵽�Թ�����Һ��Ϊ��ɫʱ���Թ�d�з�Ӧ�����������ʴ�Ϊ���������������Թ�����Һ��Ϊ��ɫ��
�����ñ�ˮ�����ձ��е���ˮ���¶�̫��������ɵ�1��2-�������飨�۵�Ϊ9.79�������̻����d�г����ܣ��ʴ�Ϊ���Թ�d �г����ܶ�����
��������������Һ����ϴȥ�ֲ�Ʒ��δ��Ӧ����嵥�ʡ�
��1��2-������������ʵ���Ϊ![]() ����ϩ�������ʵ���Ϊ
����ϩ�������ʵ���Ϊ![]() �����Լ��������Ϊ
�����Լ��������Ϊ 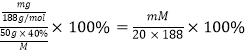
��ȡ���������Һ�����������Ba(NO3)2 ��Һ,������ɫ����,֤����Һ�д���PO43-������ȡ�����ϲ���Һ���Թ������������ϡ�����AgNO3��Һ,������ɫ������֤����Һ�д���Cl-��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и���ԭ����������ʾ������Ԫ�أ����γ�AB2�����ӻ��������
A.6��8��B.11��8��C.11��16��D.12��17
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300 ��ʱ����2 mol A��2 mol B������������2 L�ܱ������У��������·�Ӧ��3A(g)��B(g)![]() 2 C(g)��2D(g) ��H��Q, 2 minĩ�ﵽƽ�⣬����0.8 mol D��
2 C(g)��2D(g) ��H��Q, 2 minĩ�ﵽƽ�⣬����0.8 mol D��
(1)300��ʱ���÷�Ӧ��ƽ�ⳣ������ʽΪK��______________����֪K300��<K350��������H____0(����>������<��)��
(2)��2 minĩʱ��B��ƽ��Ũ��Ϊ________��D��ƽ����Ӧ����Ϊ________��
(3)���¶Ȳ��䣬��С�����ݻ�����A��ת����________(��������������С������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У������ڻ���Ӫ�����ʵ��ǣ� ��
A.������B.������C.֬��D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ�ý���ʵ�飬��Һ��A��μ��뵽����B�У����������в���ȷ����(����)

A. ��AΪ���ᣬBΪ����(��״)��CΪ����ʯ��ˮ��Һ����C����Һ�����
B. ��AΪŨ���ᣬBΪп����C��ʢ���з�̪��NaOH��Һ����C����Һ��ɫ
C. ��AΪ˫��ˮ��BΪMnO2��C��ΪNaOH��Һ��DΪ������װ��
D. ʵ��������D��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������80 g��������Ϊ10%������������Һ����ͼ�����Ƹ�����������Һ��ʵ�����ʾ��ͼ��
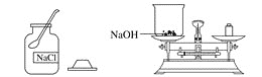
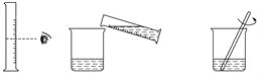
ʵ�鲽��
(1)���㣺��Ҫ�������ƹ���__________g��ˮ__________mL(ˮ���ܶ�Ϊ1 g��mL��1)��
(2)��������������ƽ��ȡ�������ƹ��壬�ù��Ϊ__________(�10mL����50mL����100mL��)����Ͳ��ȡ����Ҫ��ˮ������ʢ���������Ƶ��ձ��С�
(3)�ܽ⣺�ò��������裬ʹ�������ƹ�����ȫ�ܽ⡣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���۱�ϩ�Ǻϳ���ά��˿��ԭ�ϣ�������һ����ƷҲʹ���˺ϳ���ά�����
A.������B.��ֽC.������D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ���ܹ��γɶ��ֻ������ش��������⣺
��1������(N2H4)������ΪҺ̬���ڿ�����Ѹ����ȫȼ������N2��ͬʱ�������ȣ���������������ɴ��������ȼ�ϡ�
��֪��H2(g)+1/2O2(g) = H2O(l) ��H1= ��285.8kJ/mol
N2(g)+2H2(g) = N2H4(l) ��H2= + 50.6kJ/mol
��N2H4(l)�ڿ���ȼ������Һ̬ˮ���Ȼ�ѧ����ʽΪ_______________________��
��2�����ð�������������(HCN)�ķ�ӦCH4(g)+NH3(g)=HCN(g)+3H2(g)��H>0
��һ���¶��£���2L���������г���1molCH4(g)��2molNH3(g)����������Ӧ��4min�ﵽƽ��ʱ�����CH4ƽ��ת����Ϊ66.67%��0~4min�ڣ���H2��ʾ�ĸ÷�Ӧ����v(H2)=___________�������¶Ⱥ��ݻ����䣬����ƽ���������г���2molNH3��2molH2����ʱv�� ___v��(ѡ����>����<������=��)��
��ƽ����ϵ��HCN�����ʵ���(n)��ij�������仯������ͼ��ʾ(ͼ��x��L�ֱ��ʾ�¶Ȼ�ѹǿ)��
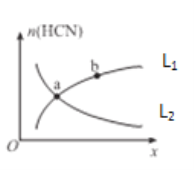
��xΪ�¶ȣ������ߣ�____(ѡ����L1������L2��)����ȷ��ʾn(HCN)���¶ȵĹ�ϵ��
��xΪѹǿ��������____(ѡ����L1������L2��)����ȷ��ʾn(HCN)��ѹǿ�Ĺ�ϵ��
��3��NH3�ܹ��γ�Ag(NH3)2+��
��֪��Һ�д���Ag+(aq)+2NH3(aq)==Ag(NH3)2+(aq)�������¸÷�Ӧƽ�ⳣ��K1=1.10��107����ӦAgCl(s)+2NH3(aq) ![]() Ag(NH3)2+(aq) +Cl-(aq)�Ļ�ѧƽ�ⳣ��K2=1.936��10-3����Ksp(AgCl)=____________��
Ag(NH3)2+(aq) +Cl-(aq)�Ļ�ѧƽ�ⳣ��K2=1.936��10-3����Ksp(AgCl)=____________��
��4����������͵��������dz����Ĵ�����Ⱦ�������ͼ��ʾװ��(�缫��Ϊ���Ե缫)������SO2�����������ų�����Һ����NO2��
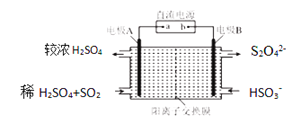
���缫A�ĵ缫��ӦʽΪ__________________________________��
���ڼ��������£��������ų�����Һ����NO2��ʹ��ת��Ϊ�����壬ͬʱ��SO32-���ɡ��÷�Ӧ���ӷ���ʽΪ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķ��뷽������ȷ���ǣ�������
A.�ù��˵ķ�����ȥʳ��ˮ�е���ɳ
B.������ķ���������ˮ�Ƴ�����ˮ
C.�þƾ���ȡ��ˮ�еĵ�
D.����ϴ�ķ�����ɳ���Խ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com