
【题目】【化学——选修3:物质结构与性质】在研究金矿床物质组分的过程中,通过分析发现了Cu-Ni-Zn-Sn-Fe多金属互化物。
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于 (填“晶体”或“非晶体”),可通过 方法鉴别。
(2)基态Ni2+的核外电子排布式 ;配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体;Ni2+和Fe2+的半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”)。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为 ;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的沸点,其原因是 ;写出一种与SCN—互为等电子体的分子 (用化学式表示)。
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为 。
![]()
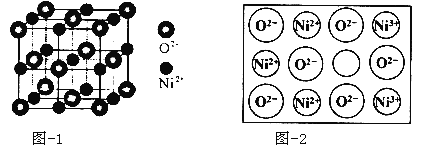
(5)立方NiO(氧化镍)晶体的结构如图所示,其晶胞边长为apm,列式表示NiO晶体的密度为 g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。人工制备的NiO晶体中常存在缺陷(如图):一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。已知某氧化镍样品组成Ni0.96O,该晶体中Ni3+与Ni2+的离子个数之比为 。
【答案】(1)晶体(1分) x~射线衍射(1分)
(2)【Ar】3d8(1分) 分子(1分) >(2分)
(3)5NA(或5×6.02×1023或3.01×1024) 异硫氰酸中H-N键极性强,分子间存在氢键,而硫氰酸分子间只存在分子间作用力,所以异硫氰酸的沸点高于硫氰酸(2分) CO2(1分,合理即可)
(4)sp3 sp2 (2分)
(5)![]() 1:11(1分)
1:11(1分)
【解析】
试题分析:(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该计算互化物属于晶体,可通过X-射线衍射实验进行鉴别;
(2)Ni元素原子核外电子数为28,核外电子排布式为1s22s22p63s23p63d84s2,失去4s能级2个电子形成Ni2+,故Ni2+离子核外电子排布为:1s22s22p63s23p63d8,Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂,固态Ni(CO)4属于分子晶体;Ni2+和Fe2+的离子所带电荷相同,Ni2+离子半径较小,NiO中离子键更强,NiO晶体的熔点更高;
(3)(SCN)2的结构式为N≡C-S-S-C≡N,根据[(SCN)2]的结构可知分子中有3个单键和2个碳氮三键,单键为σ键,三键含有1个σ键、2个π键,(SCN)2分子含有5个σ键,故1mol(SCN)2分子中含有σ键的数目为 5NA;由于异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键,所以硫氰酸(H-S-C≡N)的沸点低于异硫氰酸;一种与SCN-互为等电子体的分子有CO2等,原子数相同,价电子数均为16;
(4)分子中连接氨基的C原子形成2个C-H键、1个C-N、1个C-O键,没有孤电子对,杂化轨道数目为4,采取sp3杂化,而碳氧双键中的C原子形成3个σ键,没有孤电子对,杂化轨道数目为3,采取sp2杂化;
(5)晶胞中Ni原子数目为1+12×1/4=4,氧原子数目为8×1/8+6×1/2=4,晶胞质量为4×![]() g,晶胞边长为apm,晶胞体积为(a×10-10 cm)3,NiO晶体的密度为为4×
g,晶胞边长为apm,晶胞体积为(a×10-10 cm)3,NiO晶体的密度为为4×![]() g÷(a × 10-10 cm)3 =
g÷(a × 10-10 cm)3 = ![]() g/cm3;设1mol Ni0.96O中含Ni3+xmol,Ni2+为(0.96-x)mol,根据晶体仍呈电中性,可知 3x+2×(0.96-x)=2×1,x=0.08mol Ni2+为(0.96-x)mol=0.88mol,即离子数之比为Ni3+:Ni2+=0.08:0.88=1:11。
g/cm3;设1mol Ni0.96O中含Ni3+xmol,Ni2+为(0.96-x)mol,根据晶体仍呈电中性,可知 3x+2×(0.96-x)=2×1,x=0.08mol Ni2+为(0.96-x)mol=0.88mol,即离子数之比为Ni3+:Ni2+=0.08:0.88=1:11。


科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A.涤纶、纤维素、酚醛树脂都是合成材料
B.汽油和植物油都是混合物,主要成份是烃和酯
C.甲酸与乙酸是有机酸,都不能被酸性高锰酸钾溶液氧化
D.葡萄糖、蔗糖、淀粉在一定条件下都可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别物质的方法能达到目的的是
A用氨水鉴别用氨水鉴别MgCl2溶液和AlCl3溶液
A. 用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液
B. 用KSCN溶液鉴别FeCl3溶液和FeCl2溶液
C. 用淀粉溶液鉴别加碘盐和未加碘盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种气体的质量是14.2 g,体积是4.48 L(标准状况),该气体的摩尔质量是( )
A. 28.4 B. 28.4 g·mol-1 C. 71 D. 71 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的叙述正确的是
A.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-)
B.在pH=3的溶液中,Na+、Cl-、Fe2+、ClO-可大量共存
C.常温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有HCO3﹣、SO32﹣、CO32﹣、CH3COO﹣种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是( )
A.CH3COO﹣
B.SO32﹣
C.CO32﹣
D.HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | … |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | … |
A. C6H14 B. C6H12 C. C7H12 D. C7H14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com