
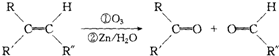
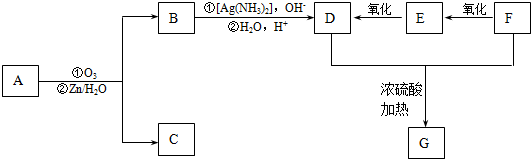
 +2H2O,反应类型是酯化反应.D与碳酸氢钠反应的化学方程式是HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O.
+2H2O,反应类型是酯化反应.D与碳酸氢钠反应的化学方程式是HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O.分析 A具有酸性,物质的量为0.0002mol的A需用20.0 mL 0.0100mol/L氢氧化钠水溶液来滴定达到滴定终点,说明A中有一个羧基,化合物中碳、氢、氧的质量比为7.5:1.125:3,所以氧元素的质量分数为$\frac{3}{7.5+1.125+3}$=0.258,假设分子中有2个氧原子,则相对分子质量为$\frac{32}{0.258}$=124,分子中有3个氧原子,则相对分子质量为$\frac{48}{0.258}$=186,有机化合物A的相对分子质量大于150且小于200,所以分子中含有3个氧原子,符合题意,分子中碳原子数为$\frac{7.5×48}{3×12}$=10,氢原子数为$\frac{1.125×48}{3}$=18,所以A的分子式为C10H18O3,A能使溴的四氯化碳溶液褪色,说明A中有碳碳双键,A发生臭氧化还原水解反应生成B和C,B能发生银镜反应,且能与金属钠或氢氧化钠溶液反应,说明B中有羧基和醛基,B氧化得D,1molD与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),说明D中有两个羧基,F经两步氧化得D,说明F为醇,D与F在浓硫酸作用下加热,可以生成一个化学式(分子式)为C4H4O4的六元环G,则G应为 ,所以可以推得F为HOCH2CH2OH,E为OHCCHO,D为HOOCCOOH,B为OHCCOOH,有机化合物C没有支链,分子中没有-CH3,结合题中信息可知,C为OHC(CH2)6CH2OH,则A为HOOCCH=CH(CH2)6CH2OH,据此答题.
,所以可以推得F为HOCH2CH2OH,E为OHCCHO,D为HOOCCOOH,B为OHCCOOH,有机化合物C没有支链,分子中没有-CH3,结合题中信息可知,C为OHC(CH2)6CH2OH,则A为HOOCCH=CH(CH2)6CH2OH,据此答题.
解答 解:A具有酸性,物质的量为0.0002mol的A需用20.0 mL 0.0100mol/L氢氧化钠水溶液来滴定达到滴定终点,说明A中有一个羧基,化合物中碳、氢、氧的质量比为7.5:1.125:3,所以氧元素的质量分数为$\frac{3}{7.5+1.125+3}$=0.258,假设分子中有2个氧原子,则相对分子质量为$\frac{32}{0.258}$=124,分子中有3个氧原子,则相对分子质量为$\frac{48}{0.258}$=186,有机化合物A的相对分子质量大于150且小于200,所以分子中含有3个氧原子,符合题意,分子中碳原子数为$\frac{7.5×48}{3×12}$=10,氢原子数为$\frac{1.125×48}{3}$=18,所以A的分子式为C10H18O3,A能使溴的四氯化碳溶液褪色,说明A中有碳碳双键,A发生臭氧化还原水解反应生成B和C,B能发生银镜反应,且能与金属钠或氢氧化钠溶液反应,说明B中有羧基和醛基,B氧化得D,1molD与适量的碳酸氢钠溶液反应可放出二氧化碳44.8L(标准状况),说明D中有两个羧基,F经两步氧化得D,说明F为醇,D与F在浓硫酸作用下加热,可以生成一个化学式(分子式)为C4H4O4的六元环G,则G应为 ,所以可以推得F为HOCH2CH2OH,E为OHCCHO,D为HOOCCOOH,B为OHCCOOH,有机化合物C没有支链,分子中没有-CH3,结合题中信息可知,C为OHC(CH2)6CH2OH,则A为HOOCCH=CH(CH2)6CH2OH,
,所以可以推得F为HOCH2CH2OH,E为OHCCHO,D为HOOCCOOH,B为OHCCOOH,有机化合物C没有支链,分子中没有-CH3,结合题中信息可知,C为OHC(CH2)6CH2OH,则A为HOOCCH=CH(CH2)6CH2OH,
(1)有机化合物A的相对分子质量(分子量)是186,该化合物的化学式(分子式)为C10H18O3,A的不饱和度=$\frac{10×2+2-18}{2}$=2,羧基的不饱和度是1,所以该分子中含碳碳双键,
故答案为:186;C10H18O3;碳碳双键;
(2)HOOCCOOH与HOCH2CH2OH在浓硫酸作用下发生酯化反应生成 ,反应的方程式为HOOCCOOH+HOCH2CH2OH$→_{△}^{浓硫酸}$
,反应的方程式为HOOCCOOH+HOCH2CH2OH$→_{△}^{浓硫酸}$ +2H2O,HOOCCOOH与碳酸氢钠反应的化学方程式为HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O,
+2H2O,HOOCCOOH与碳酸氢钠反应的化学方程式为HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O,
故答案为:HOOCCOOH+HOCH2CH2OH$→_{△}^{浓硫酸}$ +2H2O;酯化反应;HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O;
+2H2O;酯化反应;HOOCCOOH+2NaHCO3=NaOOCCOONa+2CO2↑+2H2O;
(3)根据上面的分析可知,A为HOOCCH=CH(CH2)6CH2OH,故答案为:HOOCCH=CH(CH2)6CH2OH.
点评 本题考查有机物推断,侧重考查学生分析判断能力,正确判断A结构简式是解本题关键,结合反应条件、某些物质性质来分析判断,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
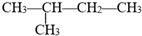 用系统命名法命名的名称是2-甲基丁烷,它的一氯代物有4种,若它是用烯烃和氢气加成而得到,则烯烃可能的结构简式是:CH2=(CH3)C-CH2-CH3;(CH3)2C=CH-CH3;(CH3)2CH-CH=CH2.
用系统命名法命名的名称是2-甲基丁烷,它的一氯代物有4种,若它是用烯烃和氢气加成而得到,则烯烃可能的结构简式是:CH2=(CH3)C-CH2-CH3;(CH3)2C=CH-CH3;(CH3)2CH-CH=CH2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 形成酸雨的主要物质是硫的氧化物和氮的氧化物 | |
| B. | 海洋元素--溴的提取常用“空气吹出法”,该制备方法中溴元素依次经过被氧化、被还原、被氧化的三过程 | |
| C. | 绿色化学的核心就是如何对被污染的环境进行无毒无害的治理 | |
| D. | 水华、赤潮等水体污染主要是由含氮、磷的生活污水任意排放造成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -Y kJ/mol | B. | -(5X-0.5Y)kJ/mol | C. | -(10X-Y)kJ/mol | D. | +(10X-Y)kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
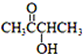 )有如下转化关系,且 1mol B反应生成了2mol C.
)有如下转化关系,且 1mol B反应生成了2mol C.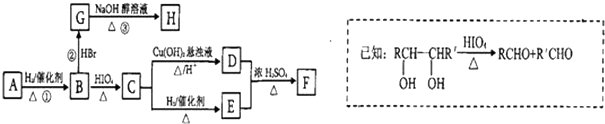
 .
.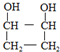 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
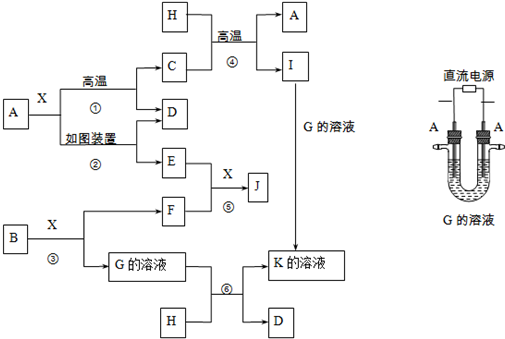
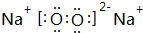 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com