
【题目】向容积为2 L的密闭容器中充人2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g)![]() 3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
⑤其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
A. ①②③B. ①③⑤C. ②④⑤D. ①④⑤
【答案】B
【解析】
根据题意知2 s后达到平衡,测得C气体的浓度为0.6mol·L-1,根据方程式可知,转化的A和B 的浓度分别是0.4mol·L-1和0.2mol·L-1,则A和B的反应速率分别是0.4mol·L-1÷2s=0.20.2 mol·L-1·s-1和0.20.2 mol·L-1÷2s=0.10.2 mol·L-1·s-1,所以①正确,②不正确;由于A和B的物质的量物质的量之比是2︰1,恰好等于相应的化学计量数之比,所以二者的转化率是相等的,③正确;平衡时物质B的浓度为0.3 0.2 mol·L-1,④不正确,该反应为反应前后气体物质的量不变的反应,其它条件不变,向容器中再加入1 molC气体,相当于增大压强,平衡不移动,故达到新平衡时,C的体积分数不变,⑤正确,选B。


科目:高中化学 来源: 题型:
【题目】有氯化钠和碘化钠的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为 17.55 g。
(1)原混合物中碘化钠的质量是________。
(2)原混合物中氯化钠的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】橡皮筋在拉伸和收缩状态时结构如图:在其拉伸过程中有放热现象,反之吸热。25℃、101kPa时,下列化学反应的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是

A.2Na+2H2O=2NaOH+H2↑
B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
C.2H2+O2=2H2O
D.CaCO3=CaO+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验过程中,若一种气体极易溶于一种液体,则容易发生倒吸现象,给实验造成危险。现有4位同学分别设计了一个实验,希望通过观察到的明显现象来说明二氧化碳极易溶于氢氧化钠溶液,设计的装置如下:

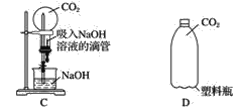
其中一位同学向充满二氧化碳的塑料瓶D中加入氢氧化钠溶液,盖紧瓶塞后振荡,如果看到瓶子变瘪了,说明二氧化碳与氢氧化钠溶液发生了反应。对装置A~C,将能达到实验目的的装置、操作方法和实验现象填入下表(可不填满):
_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以电石渣为原料制备KClO3的流程如图:
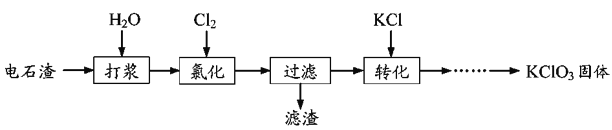
(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为________。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有________(填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O,氯化完成后过滤。
①滤渣的主要成分为_______(填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]:n(CaCl2)___1:5(填“>”、“<”或“=”)。
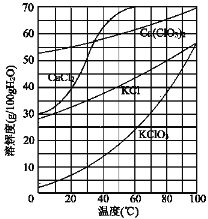
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100 gL-1,从该溶液中尽可能多地析出KClO3固体的方法是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组在做过氧化钠与水反应实验时,发现过氧化钠与水反应后的溶液中滴加酚酞溶液溶液呈现红色,但红色很快褪色,甲、乙、丙三同学对此现象分别做了如下推测:
甲:因为反应后试管很热,所以可能是溶液温度较高使红色褪去;
乙:因为所加水的量较少,红色褪去可能是生成的氢氧化钠溶液浓度较大的影响;
丙:过氧化钠具有强氧化性,生成物中氧气、过氧化氢(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质 。
(1)验证甲同学的推测是否正确的方法是____________________,验证乙同学的推测是否正确的方法是______________________;当出现____________现象时,即可说明丙同学的推测正确。
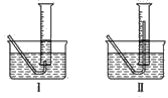
(2)有同学提出用定量的方法探究丙同学方案中是否含有过氧化氢,其实验方法为:称取2.6 g过氧化钠固体,使之与足量的水反应,测量产生氧气的体积,与理论值比较可得出结论。测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用如图装置中的_____________,理由是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质钛(Ti)抗腐蚀能力强(放在大海中几周后仍金光闪闪),机械强度高,有“未来金属”之称。又因用它制的“骨头”置入人体后可以在上面长肉,所以又有“亲生物金属”之美誉。工业上常用硫酸分解钛铁矿(FeTiO3,铁为+2价)的方法来制取TiO2,再由TiO2制金属钛。主要反应有:
①FeTiO3+3H2SO4=Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O=H2TiO3↓+2H2SO4
③H2TiO3![]() TiO2+H2O
TiO2+H2O
④TiO2+2C+2Cl2![]() TiCl4↑+2CO↑
TiCl4↑+2CO↑
⑤TiCl4+2Mg![]() 2MgCl2+Ti
2MgCl2+Ti
上述反应中,属于氧化还原反应的有( )
A.①②
B.①⑤
C.③④
D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g);△H<0.上图表示该反应的速率(v)随时间
(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中不正确的是( )

A. ![]() 时加入了催化剂B.
时加入了催化剂B. ![]() 时降低了温度
时降低了温度
C. ![]() 时增大了压强D.
时增大了压强D. ![]() 时间内转化率最高
时间内转化率最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com