


科目:高中化学 来源: 题型:
| A、NaOH═Na++OH- |
| B、2H2O═O2↑+2H2↑ |
| C、H2SO4═H2++SO42- |
| D、Na2CO3═2Na++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H2 |
| B、C2H4 |
| C、CH2=C(CH3)2 |
| D、CH≡C-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
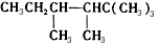
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
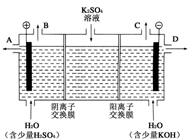 电化学知识是化学反应原理的重要部分,以下是常见的电化学装置:
电化学知识是化学反应原理的重要部分,以下是常见的电化学装置:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,水电离出的c(H+)=1×10-12mol/L,某无色溶液中不可能大量存在:Al3+、NH4+、Cl-、S2- |
| B、pH=2的溶液中,可能大量存在:Na+、Fe2+、ClO-、SO42- |
| C、常温下某溶液中KW/c(H+)=1×10-12,溶液中可能大量存在:Na+、NH4+、Cl-、HCO3- |
| D、某溶液中加入少量Al 有气体生成,溶液中可能大量存在:Na+、K+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当NH3、O2、NO、H2O浓度比为4:5:4:6时达到平衡 | ||
B、平衡时v正(O2)=
| ||
| C、平衡后减小压强,混合气体平均摩尔质量增大 | ||
| D、平衡后升高温度,混合气体中NO含量降低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com