
| A�������£�ˮ�������c��H+��=1��10-12mol/L��ij��ɫ��Һ�в����ܴ������ڣ�Al3+��NH4+��Cl-��S2- |
| B��pH=2����Һ�У����ܴ������ڣ�Na+��Fe2+��ClO-��SO42- |
| C��������ij��Һ��KW/c��H+��=1��10-12����Һ�п��ܴ������ڣ�Na+��NH4+��Cl-��HCO3- |
| D��ij��Һ�м�������Al ���������ɣ���Һ�п��ܴ������ڣ�Na+��K+��Cl-��NO3- |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0 | B��1 | C��2 | D��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
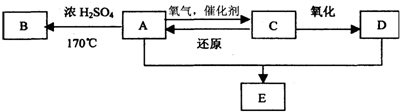
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4+��NO3-��Mg2+��SO42- |
| B��Na+��OH-��K+��NO3- |
| C��MnO4-��K+��SO42-��Na+ |
| D��K+��SO42-��HCO3-��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �ࡡ�� | A | B | C | D |
| ǿ����� | KNO3 | H2SO4 | Ba��OH��2 | BaSO4 |
| ������� | CH3COOH | CaCO3 | H2S | NH3?H2O |
| �ǵ���� | SO2 | CO2 | Cl2 | C2H5OH��Һ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0�桢101 kPa�����£�ij��������Ϊ22.4 L�������������ʵ���ԼΪ1 mol |
| B��1 molij�������Ϊ22.4 L�������������״̬һ��Ϊ��״�� |
| C����״���£�1 mol H2O�����Ϊ22.4 L |
| D��1 mol CO2��25���101KPaʱ�����ԼΪ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
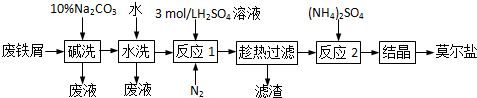
| 4.9 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com