
(19分)晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等,.以下是工业上制取纯硅的一种方法.

已知:在一定条件下可发生反应:Si(s)+3HCl(g)  SiHCl3(g)+H2(g) ΔH<0
SiHCl3(g)+H2(g) ΔH<0
I.反应②、③均需要加热,有如下两个温度区间分别供两反应选择,你认为反应②应选择_______(填序号字母),原因是_______________;
a .520~530K B.1350~1360K
II.现在实验室模拟工业上粗硅提纯的过程,已知SiHCl3遇水强烈水解,其他相关数据如下表所示:
物质 | SiCl4 | SiHCl3 | AlCl3 | FeCl3 |
沸点/℃ | 57.7 | 33.0 | - | 315 |
升华温度/℃ | - | - | 180 | 300 |
(1)现用如下装置进行模拟反应②的过程。实验室制HCl的反应原理为:
2NaCl(s) + H2SO4(浓) 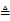 2HCl↑ + Na2SO4
2HCl↑ + Na2SO4
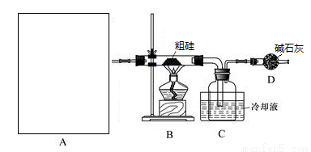
A中是HCl的发生装置,你认为应选择下列哪套装置?____________(填装置的序号字母),装置D中碱石灰的作用为__________________、___________________;
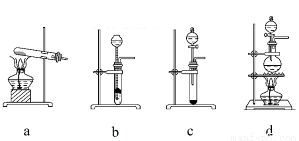
(2)已知液态粗品SiHCl3中含有杂质SiCl4、AlCl3、FeCl3等,则流程中操作①为_____________(填操作名称),下列不是该操作所需的仪器是____________________(填装置序号字母);
a.冷凝管 b. 圆底烧瓶 c. 蒸馏烧瓶 d. 分液漏斗 e.温度计 f. 接受器
(3)用SiHCl3与H2反应制备纯硅的装置如下:
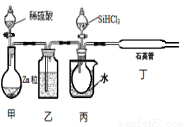
①按图示组装好仪器后,下列实验步骤的正确顺序为____________(填步骤的序号字母),
A.打开甲装置分液漏斗旋塞,滴加稀硫酸,反应生成H2;
B.向装置中添加药品;
C.打开丙装置分液漏斗的旋塞,滴加SiHCl3,并加热相应装置;
D.检查装置气密性;
e.停止向丙装置滴加SiHCl3,并停止加热相应装置;
f.停止通H2;
步骤c中需要加热的装置为____________(填装置序号“甲”、“乙”、“丙”、“丁”)
②该套装置的设计缺陷是________________________。
科目:高中化学 来源:2016届陕西省高三上学期10月月考化学试卷(解析版) 题型:推断题
(10分)化合物F是一种调香剂,结构为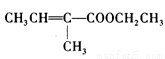 ;以化合物A为原料合成F的工艺流程如下:
;以化合物A为原料合成F的工艺流程如下:

根据上述信息回答下列问题:
(1)化合物F不能发生的反应类型有 (填序号)。
A.加成反应 B.醋化反应 C.水解反应 D.加聚反应
(2)化合物A的结构简式为 ;分子中不同化学环境的氢核磁共振谱峰面积比为
(3)反应④的化学方程式为
(4)化合物F反式异构体结构简式为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期半期考试化学试卷(解析版) 题型:选择题
甲、乙两种固体物质的溶解度曲线如右图所示。下列说法正确的是
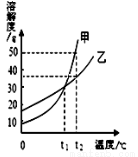
A.甲的溶解度大于乙的溶解度
B.升高温度可使甲的不饱和溶液变为饱和溶液
C.t1℃时,甲、乙两种饱和溶液的溶质质量分数相等
D.t2℃时,50g乙加入100g水中得到乙的不饱和溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省泰州市姜堰区高二上学期期中必修化学试卷(解析版) 题型:选择题
中共十八大报告中提出:“加强生态文明宣传教育,增强全民节约意识、环保意识、生态意识,形成合理消费的社会风尚,营造爱护生态环境的良好风气。”下列行为不利于“生态文明”建设的是
A.在化学反应中要考虑“原子经济性”以提高效率
B.资源的开发和利用,要考虑可持续发展的原则
C.将废弃的塑料袋回收进行露天焚烧,以解决“白色污染”问题
D.要加强对工业“三废”的治理,以保护环境
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三上学期10月月考化学试卷(解析版) 题型:选择题
某可逆反应为2X(g)  3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示: 下列推断正确的是
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示: 下列推断正确的是

A.升高温度,该反应平衡常数K减小
B.压强大小有P3>P2>P1
C.平衡后加入高效催化剂使Mr增大
D.在该条件下M点X平衡转化率为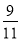
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆市高一上学期第一次月考化学试卷(解析版) 题型:选择题
某10% NaOH溶液,加热蒸发掉100 g水后得到80 mL 20%的溶液,则该20% NaOH溶液的物质的量浓度为
A.6.25 mol/L B.12.5 mol/L C.7 mol/L D.7.5 mol/L
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:填空题
(12分)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平,不考虑 2NO2  N2O4)。
N2O4)。
(1)硝酸在该反应中体现的性质有__________________。
(2)如果参加反应的Cu和HNO3的物质的量之比是3:10,写出并配平该反应的离子方程式_________________________。
(3)0.004molCu被硝酸完全溶解后,Cu失去的电子数是______________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是______________,在标准状况下若将收集NO和NO2的集气瓶倒立于水中,通入一定量的氧气充分反应后发现无气体剩余,则通入O2的体积为________ mL;所得溶液(假设溶质不扩散)的物质的量浓度是______________________。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省绥化市高三上学期期中测试化学试卷(解析版) 题型:选择题
下列物质的使用不涉及化学变化的是
A.明矾用作净水剂 B.生石灰作干燥剂
C.氢氟酸刻蚀玻璃 D.液氨用作制冷剂
查看答案和解析>>
科目:高中化学 来源:2016届湖南省益阳市高三上学期第三次模拟化学试卷(解析版) 题型:选择题
下列图示与对应叙述相符合的是
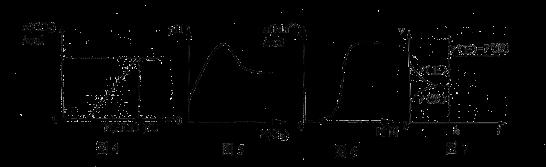
A.图4表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol·L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系
B.图5表示Cl2通入H2S溶液中pH的变化
C.图6表示10 mL 0.01 mol·L-1KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4
溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用)
D.图7表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com