
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:
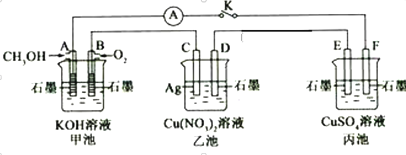
(1)甲池为__________(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为______________。
(2)丙池中E电极为_________(填“正极”、“负极”、“阴极”或“阳极”),电极的电极反应式为_____________。该池总反应的化学方程式为___________________。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_____mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使丙池恢复到反应前浓度的是___(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
【答案】原电池 CH3OH - 6e-+ 8OH-= CO32-+ 6H2O 阳极 2H2O-4e-= O2↑+4H+ 2CuSO4 + 2H2O![]() 2Cu +O2↑+2H2SO4 560 B
2Cu +O2↑+2H2SO4 560 B
【解析】
由图可知甲图为原电池是一甲醇燃料电池,通甲醇的A为负极、B为正极;乙池为电解池,C为阳极电极反应为:Ag-e-=Ag+,D为阴极,电极反应为Cu2++2e-=Cu;丙池为电解池,E为阳极,电极反应为:2H2O-4e-=O2↑+4H+,F电极为阴极,电极反应为:Cu2++2e-=Cu,总反应方程式为:2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑,一段时间后,断开电键K,要使丙池恢复到反应前浓度需加入CuO或者CuCO3,据此分析解答。
2H2SO4+2Cu+O2↑,一段时间后,断开电键K,要使丙池恢复到反应前浓度需加入CuO或者CuCO3,据此分析解答。
(1)由图可知甲图为原电池,A电极通入甲醇,为负极,电极反应式为:CH3OH+8OH--6e-=CO32-+6H2O;
(2)丙池为电解池,其中E电极连接电源正极,为阳极,电极反应式为:2H2O-4e-=O2↑+4H+,F电极连接电源负极,为阴极,发生反应:Cu2++2e-=Cu,总反应方程式为:2CuSO4+2H2O![]() 2H2SO4+2Cu+O2↑;
2H2SO4+2Cu+O2↑;
(3)乙池中C为阳极电极反应为:Ag-e-=Ag+,D为阴极,电极反应为Cu2++2e-=Cu;n(Ag)=10.8g÷108g/mol=0.1mol,由于Ag是+1价的金属,所以转移电子的物质的量为0.1mol,由于在同一闭合回路中电子转移数目相等,所以甲池中反应消耗O2的物质的量n(O2)=![]() ×0.1mol=0.025mol,则消耗氧气在标准状况下的体积V(O2)=0.025mol×22.4L/mol=0.56L=560mL;
×0.1mol=0.025mol,则消耗氧气在标准状况下的体积V(O2)=0.025mol×22.4L/mol=0.56L=560mL;
(4)一段时间后,断开电键K,根据少什么加什么,丙池一个电极产生Cu单质,另一个电极产生O2,相当于从溶液中出去的物质为Cu与O2反应产生的CuO。
A.Cu与硫酸不能反应,不能达到目的,A错误;
B.CuO与硫酸反应,产生硫酸铜和水,能达到目的,B正确;
C.Cu(OH)2比CuO多一个水的组成,相当于对溶液进行了稀释,不能使丙池恢复到反应前浓度,C错误;
D.Cu2(OH)2CO3与硫酸生成硫酸铜、二氧化碳和水,比等物质的量的CuO多一个水的组成,相当于对溶液进行了稀释,不能使丙池恢复到反应前浓度,D错误;
故合理选项是B。


 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】过氧化氢是用途很广的绿色氧化剂,它的水溶液俗称双氧水,常用于消毒、杀菌、漂白等。试回答下列问题:
(1)写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:____________。
(2)Na2O2、K2O2以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。则上述最适合的过氧化物是________。
(3)甲酸钙[Ca(HCOO)2]广泛用于食品工业生产上,实验室制取甲酸钙的方法之一是将氢氧化钙和甲醛溶液依次加入到质量分数为30%~70%的过氧化氢溶液中,则该反应的化学方程式为________,过氧化氢比理论用量稍多,其目的是________。反应温度最好控制在30 ~70℃,温度不易过高,其主要原因是________。
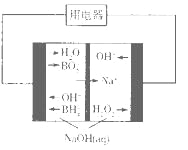
(4)下图是硼氢化钠一过氧化氢燃料电池示意图。该电池工作时,正极附近溶液的pH________(填“增大”、“减小”或“不变”)。
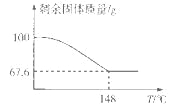
(5)Na2CO3·xH2O2可消毒、漂白。现称取100 g的Na2CO3·xH2O2晶体加热,实验结果如图所示,则该晶体的组成为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
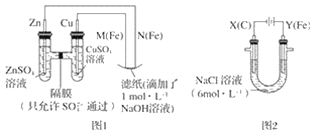
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__(填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__(填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院长春应化所张新波团队提出了一种独特的锂-氮电池(Li-N2),该电池在放电过程中消耗氮气,充电过程中释放氮气,实现氮气的循环,并对外提供电能。该电池在充电时发生反应:2Li3N![]() N2↑+6Li。现以该电池为电源进行如图所示实验,下列说法正确的是( )
N2↑+6Li。现以该电池为电源进行如图所示实验,下列说法正确的是( )
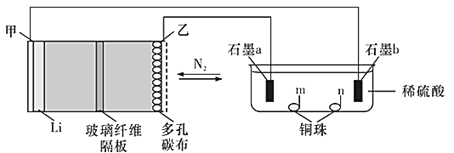
A.乙电极上的反应为2Li3N-6e-=N2↑+6Li+
B.充电过程中Li+由甲电极迁移向乙电极,并在多孔碳布表面生成Li3N
C.电极“石墨a”和m、n处均可能有铜析出
D.锂氮电池为绿色固氮提供了一种可能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究小组设计用含氯的有机物A合成棉织物免烫抗皱整理剂M的路线如下(部分反应试剂和条件未注明):

已知:①E的分子式为C5H8O4,能发生水解反应,核磁共振氢谱显示E分子内有2种不同化学环境的氢原子,其个数比为3∶1;

(R、R′、R″代表相同或不相同的烃基)。
(1)A分子中的含氧官能团的名称是________________。
(2)D→E反应的化学方程式是____________。
(3)A→B反应所需的试剂是________________。
(4)G→H反应的化学方程式是____________。
(5)已知1 mol E与2 mol J反应生成1 mol M,则M的结构简式是________。
(6)E的同分异构体有下列性质:①能与NaHCO3反应生成CO2;②能发生水解反应,且水解产物之一能发生银镜反应,则该同分异构体共有________种,其中任意1种的结构简式是________。
(7)J可合成高分子化合物,该高分子化合物的结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】交警用三氧化铬(CrO3)硅胶可以查酒驾。元素Cr的几种化合物转化关系如图所示。下列判断正确的是
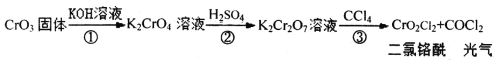
A.反应①表明CrO3有酸性氧化物的性质
B.CrO42-在碱性溶液中不能大量存在
C.只有反应③为氧化还原反应
D.基态铬原子的价电子排布式为3d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】杂志Joule中题为“Li—CO2 Electrochemistry:A New Strategy for CO2 Fixation and Energy Storage”的文章,阐述关于电化学技术固定CO2新的反应途径。下图是采用新能源储能器件将CO2转化为固体产物,实现CO2的固定和储能灵活应用的装置。储能器件使用的Li—CO2电池组成为钌电极/CO2—饱和LiClO4—DMSO电解液/锂片。下列说法错误的是

A.钌电极为负极,其电极反应式为:2Li2CO3+C—4e-=== 3CO2+4Li+
B.Li—CO2电池电解液由LiClO4—DMSO溶于水得到
C.这种电化学转化方式不仅减少CO2的排放,还可将CO2作为可再生能源载体
D.CO2的固定中,每生成1.5mol气体,可转移2mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示化学过程的化学用语书写正确的是
A.用中和热表示氢氧化钠和醋酸的稀溶液反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l) △H=57.3kJ·mol-1
B.AlCl3溶液与NaAlO2溶液混合:A13++A1O2-+3H2O![]() 2Al(OH)3↓
2Al(OH)3↓
C.HCO3-的电离:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D.Na2SO3的水解:SO32-+2H2O![]() H2SO3+2OH-
H2SO3+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种神经类药物,其合成路线如下:
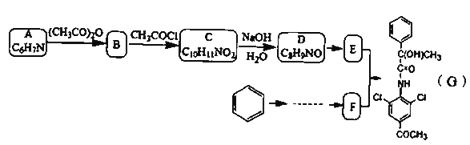
已知信息: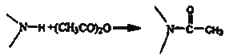 ;
;

![]()
(1)下列说法正确的是__________。
A.化合物G的分子式为![]()
B.化合物A到B的反应类型为取代反应
C.1mol化合物D最多可以与![]() 发生加成反应
发生加成反应
D.化合物D生成E的反应试剂和条件:浓氯水和铁屑
(2)A中官能团的名称是_________ C的结构简式:_________。
(3)写出E+F→G的化学方程式:__________________。
(4)写出化合物E同时符合下列条件的所有同分异构体的结构简式__________________。
①红外光谱显示含有三种官能团,其中无氧官能团与E相同,不含甲基。
②分子中含有苯环,![]() 谱显示苯环上只有一种化学环境的氢原子。
谱显示苯环上只有一种化学环境的氢原子。
③苯环上有4个取代基,能发生银镜反应。
(5)根据题中信息,设计以苯和![]() 为原料制备F的合成路线。(无机试剂任选,用流程图表示)__________
为原料制备F的合成路线。(无机试剂任选,用流程图表示)__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com